
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Укажите, какие атомы окисляются, а какие восстанавливаются в указанных схемах, и определите, как изменяется их степень окисления:
8.2.1. PbO → PbO2; NH3 → N2; V3+ → VO2+ 8.2.2. N2O → N2; S2O32– → S4O62–; MnO4– → MnO2 8.2.3. Cu2O → CuO; Cu2+ → CuI; CuO → Cu 8.2.4. NO3– → NO2–; NH3 → NO; NO → NO2 8.2.5. IO3– → I–; 2I– → I2; IO3– → I2 8.2.6. MnO2 → MnO4–; MnO42– → Mn2+; MnO42– → MnO4– 8.2.7. SnO → SnO2; Sn → Sn(OH)2; SnCl4 → Sn 8.2.8. Cl2 → 2Cl–; ClO3– → Cl–; Cl2 → ClO– 8.2.9. PH3 → P2O5; PCl5 → PCl3; PO33– → PO43– 8.2.10. TiCl4 → Ti; S → SO2; PH3 → P2O5 8.2.11. LiH → H2; H2O2 → H2O; CrO2– → CrO42– 8.2.12. CO → CO2; HNO3 → NO; Cu2S → CuO 8.2.13. FeO → Fe3O4; FeO42– → Fe3+; Fe → Fe(OH)3 8.2.14. H2S → S; SO32– → SO42–; SO32– → S 8.2.15. H2S → SO2; Tl(OH)3 → TlOH; Hg2Cl2 → HgCl2 8.2.16. H2O2 → O2; NO2 → HNO3; S22– → 2S 8.2.17. Fe(OH)2 → Fe(OH)3; ClO– → Cl–; POCl → POCl3 8.2.18. MnO2 → Mn3O4; SO2 → SO3; Br2 → 2Br– 8.2.19. CrO42– → Cr3+; Cr(OH)2 → Cr(OH)3; 2Cr3+ → Cr2O72– 8.2.20. Al2O3 → Al; Co(OH)2 → Co(OH)3; MnO4– → Mn2+ 8.3. Расставьте коэффициенты в уравнениях окислительно-восстановительных реакций ионно-электронным способом: 8.3.1. а) Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O 8.3.2. а) HClO3 + H2SO3 → H2SO4 + HCl 8.3.3. а) PbO2 + HCl → PbCl2 + Cl2 + H2O 8.3.4. а) Br2 + HClO + H2O → HBrO3 + HCl 8.3.5. а) CaH2 + H2O → Ca(OH)2 + H2 8.3.6. а) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 +H2O 8.3.7. а) BiCl3 + SnCl2 → Bi + SnCl4 8.3.8. а) Zn + HNO3 → Zn(NO3)2 + NH4NO3 8.3.9. а) Al + HNO3 → Al(NO3)3 + NH4NO3 + H2O 8.3.10. а) I2 + Cl2 + H2O → HIO3 +HCl 8.3.11. а) S + HNO3 → H2SO4 + NO 8.3.12. а) H2S + HIO3 → S + I2 + H2O 8.3.13. а) Zn + HNO3 → Zn(NO3)2 + NH4NO3 + H2O 8.3.14. а) KOH + Br2 → KBrO3 + KBr + H2O 8.3.15. а) S + KOH → K2S + K2SO3 + H2O 8.3.16. а) Fe + HNO3 → Fe(NO3)3 + H2O + NO 8.3.17. а) CuS + HNO3 → Cu(NO3)2 + H2SO4 + NO2 8.3.18. а) Ca(OH)2 + Cl2 → Ca(OCl)2 + CaCl2 + H2O 8.3.19. а) Ca + HNO3 → Ca(NO3)2 + NH4NO3 + H2O 8.3.20. а) Ag + HNO3 → AgNO3 + NO2 + H2O 8.4. Определите, в каком направлении протекает реакция в системе,
8.4.1. а) Mn2+ +S2O82– 8.4.2. а) Cr3+ + NO3– 8.4.3. а) SO32– + Br2 8.4.4. а) PbO2 + Mn2+ 8.4.5. а) MnO2 + Fe2+ 8.4.6. а) H3PO3 + H2O2 8.4.7. а) SO32– + I2 8.4.8. а) Cr3+ + SO42– 8.4.9. а) Fe3+ + I– 8.4.10. а) MnO4– + SO42– 8.4.11. а) MnO4– + NO2– 8.4.12. а) MnO4– + Cr3+ 8.4.13. а) Cr2O72– + Br– 8.4.14. а) Fe2+ + Br2 8.4.15. а) MnO4– + H2O2 8.4.16. а) MnO4– + Br– 8.4.17. а) Cr3+ + H2O2 8.4.18. а) MnO2 + I– 8.4.19. а) Mn2+ + S 8.4.20. а) Mn2+ + Cl2 Напишите полные ионные, сокращенные ионные и молекулярные уравнения реакций, описывающих поведение следующих металлов в водных растворах соляной и азотной кислот, в воде и растворе щелочи (при необходимости пользуйтесь диаграммой электрохимической устойчивости воды и таблицей стандартных потенциалов восстановления):
|
|||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 393; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.15.210.12 (0.017 с.) |
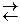 MnO2 + SO42–; б) MnO4– + Fe2+
MnO2 + SO42–; б) MnO4– + Fe2+ 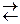 Fe3+ + Br–; б) Cr3+ + S
Fe3+ + Br–; б) Cr3+ + S 


