Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теоретические основы процесса
Большое число важнейших химических соединений (циклогексан, циклогексанол, высшие спирты, амины, стирол, изобутилен, бутадиен-1,3 и др.) в промышленности получают при помощи процессов гидрирования и дегидрирования. Реакции гидрирования и дегидрирования тесно связаны друг с другом, протекают в противоположных направлениях и в большинстве случаев находятся в термодинамическом равновесии:
АН2
Реакция гидрирования сопровождается уменьшением объема реакционной массы и выделением тепла, а реакция дегидрирования — увеличением объема реакционной массы и поглощением тепла. Поэтому сдвиг равновесия в сторону гидрирования или дегидрирования зависит от условий процесса. Так, низкие температуры и высокие давления благоприятствуют реакции гидрирования, а высокие температуры и низкие давления — реакции дегидрирования. Процессы гидрирования и дегидрирования, как правило, проводят в присутствии катализаторов, которые значительно повышают скорость процесса и его селективность. В качестве катализаторов применяют металлы и их сплавы (Pt, Pd, Ni, Cu, Zn и др.), оксиды металлов и их смеси (Fe2O3, Сr3О3,ZnO, MgO и др.), сульфиды металлов и их смеси (NiSi, WS3, MoS3 и др.). Металлы являются наиболее активными катализаторами, поэтому их чаще всего используют в процессах гидрирования, которые проводят при температурах до 220 °С и давлении до 6 МПа. В процессах дегидрирования применяют преимущественно оксидные катализаторы, которые по сравнению с металлами хотя и менее активны, но при 500—650 °С обладают большей селективностью, стабильностью и легко регенерируются. Циклогексан и циклогексанол являются важными промежуточными продуктами в процессе получения циклогексанона, капролактама и адипиновой кислоты. Кроме того, они широко используются как растворители. В промышленности циклогексан и циклогексанол получают гидрированием бензола и фенола соответственно. Процесс проводят под давлением при мольном отношении гидрируемого вещества к водороду, равном 1: (10÷30). Например, бензол гидрируют на никелевом катализаторе при 180—200 °С и 1,5—2,0 МПа или на сульфидных катализаторах при л;300°С и 20—30 МПа:
При гидрировании бензола на никелевом катализаторе повышение температуры выше 220 °С приводит к частичному распаду циклогексана на углерод, метан и другие побочные продукты и к. быстрой дезактивации катализатора.
Фенол гидрируют на никелевом катализаторе при температурах не выше 150°С и давлении 1,5—2,0 МПа в газовой фазе. При более высокой температуре значительная часть фенола гидрируется до циклогексанона и расходуется на образование других побочных продуктов:
Циклогексанон можно гидрировать в циклогексанол, но условия гидрирования более жесткие. Селективность гидрирования бензола и фенола составляет 98% и выше. Цель работы Изучение реакции гидрирования бензола в циклогексан в газовой фазе при атмосферном давлении, определение степени конверсии бензола и составление материального баланса. Методика выполнения работы Реактивы Бензол, свободный от соединений серы 39 г Водород (из баллона) 130 л Катализатор — Ni/Сг2О3 (в таблетках) 100см3 Бензол гидрируют на установке, схема которой приведена на рисунке 12.
Рисунок 12 - Установка для гидрирования бензола в газовой фазе: 1 – игольчатый вентиль; 2 – гидравлический затвор; 3 – склянка Тищенко с концентрированной кислотой; 4 – трубка с хлоридом кальция безводным; 5 – милливольтметр; 6 – реометр; 7, 24 – ледяные бани; 8 – термометр; 9 - переходник с карманом; 10, 19 – предохранительный кожух; 11 – реактор; 12 - электропечь; 13 – термопара; 14 – карман для термопары; 15 – контактный термометр; 16 – испаритель; 17 – барботер с краном; 18 – электроспираль; 20, 26 - автотрансформаторы; 21 – съемный кран; 22 – обратный холодильник; 23 – приемная колба; 25 – реле-регулятор
Установка состоит из игольчатого вентиля 1, гидравлического затвора 2, склянки Тищенко 3, трубки с безводным хлоридом кальция 4, милливольтметра 5, реометра 6, ледяных бань 7 и 24, термометра 8, переходника с карманом 9, реактора 11, электроспиралей 12 и 18, термопары 13, контактного термометра 15, испарителя 16, автотрансформаторов 20 и 26, съемного кармана 21, обратного холодильника 22, приемной колбы 23 и реле-регулятора 25. Перед началом опыта проверяют правильность сборки, герметичность всех соединений установки и убеждаются в надежной работе системы автоматического поддержания в испарителе заданной температуры.
Реактор изготовлен из термостойкой стеклянной трубки внутренним диаметром 22 мм и длиной 300 мм, снабжен карманом 14 для термопары, выступами для удерживания катализатора и предохранительным кожухом 10. Испаритель 16 объемом реакционной зоны 60 мл также изготовлен из термостойкого стекла и снабжен барботером 17 для водорода, электроспиралью 18 для нагрева реакционной массы, съемным карманом 21 для контактного термометра и предохранительным кожухом 19. Отсоединяют переходник 9 от обратного холодильника и присоединяют его через колбу (емкостью 100 мл) к линии сброса водорода в атмосферу. Подают водород в установку со скоростью 50 мл/мин и включают обогрев реактора. По достижении температуры в реакторе 200—210 °С увеличивают скорость подачи водорода до 800 мл/мин и при этой температуре восстанавливают катализатор до прекращения выделения воды и очистки стенок переходника 9 от влаги. Во время восстановления катализатора готовят ледяную баню 7. После прекращения выделения воды уменьшают скорость подачи водорода до 50 мл/мин, переходник 9 снова присоединяют к обратному холодильнику, а линию сброса водорода — к приемной колбе 23. Условия проведения опыта следующие: температура в реакторе 200—210 °С, температура в испарителе 35 °С (при гидрировании фенола в реакторе 148—160°С, в испарителе 135°С), скорость подачи водорода 800 мл/мин. Через горло для съемного кармана 21 наливают в испаритель 39 г бензола и включают обогрев испарителя. По достижении в испарителе заданной температуры (35°С) увеличивают скорость подачи водорода до 800 мл/мин. Момент увеличения скорости подачи водорода принимают за начало опыта. Гидрирование ведут до полного испарения бензола из испарителя и прекращения конденсации циклогексана в холодильнике. Затем уменьшают скорость подачи водорода до 50 мл/мин, выключают обогрев реактора и испарителя. Момент уменьшения скорости подачи водорода принимают за конец опыта. После охлаждения реактора до комнатной температуры прекращают подачу водорода, закрывают кран на барботере и выход из реактора после переходника 9. Вход и выход из реактора должны быть плотно закрыты, чтобы в него не мог проникнуть воздух. Продукты реакции из колбы 23 переносят в предварительно взвешенную на технических весах колбу, определяют массу и показатель преломления. Зная показатель преломления чистого бензола и циклогексана и исходя из того, что для показателя преломления в смеси сохраняется правило аддитивности, вычисляют концентрацию образовавшегося циклогексана С, степень конверсии бензола X и потери У (в % масс.):
где Рассчитывают объем пропущенного водорода и степень его полезного использования.
Контрольные вопросы 1. Влияние катализаторов на протекание реакций гидрирования. 2. Температурный режим процесса. 3. Как определяют показатель преломления чистого бензола?
Литература 1. Одабашян Г.В. Лабораторный практикум по химии ТООНХС. М., Химия, 1982, с. 138-142. 2. Воскресенский П.И. Техника лабораторных работ. 10-е изд. М.. Химия, 1973, 717 с.
Лабораторная работа 13
|
||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 144; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.226.82.78 (0.009 с.) |
 А + Н2
А + Н2 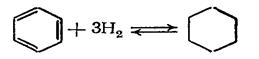



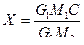
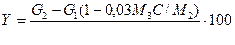
 (б),
(б),