Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Этапы биосинтеза: фотобиогенез и метаболизм
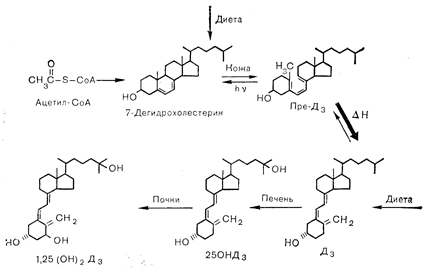
Схема стадий биосинтеза витамина D3 (холекальциферол) приведена на рис. 3—21. Субстратом синтеза 7-дегидрохолестерина — «провитамина» служит ацетил-СоА. Ультрафиолетовый фотолиз провитамина приводит к образованию 6,7-цис изомера, называемого «провитамин D3» (преD3). Этот изомер под действием температуры превращается в коже в витамин D3. Аналогичная группа реакций наблюдается и при образовании витамина D2 (эргокальциферол) из провитамина эргостерола. Витамины В3 и Da затем транспортируются на специфических, связывающих витамин D, белках плазмы в печень, где карбоксилируются по 25-му углеродному атому (С-25) с образованием одного из главных циркулирующих в крови метаболитов — 25-оксивитамина D (25-OHD). Хотя именно печень является главным местом 25- гидроксилирования витамина D, однако в некоторой степени оно происходит и в других органах. Витамин D3 25-гидроксилаза локализуется в микросомах печени (и других органов), причем ферментативная реакция в качестве кофакторов требует восстановленного НАДФ и молекулярного кислорода. В физиологических концентрациях ни витамин D, ни 25-OHD не способны стимулировать транспорт кальция в кишечнике или мобилизацию кальция из костей. Конечной активной формой витамина является 1,25(ОН)2D. Этот дважды гидроксилированный метаболит образуется в почках путем гидроксилирования 25-OHD, синтезируемого в печени и транспортируемого белковыми переносчиками плазмы в почки. Считается, что почки являются главным, если не единственным местом локализации la-гидроксилазы 25-OHD. В отличие от 25-гидроксилазы витамина D, которая присутствует в печеночных микросомах, 1a-гидроксилаза 25-OHD локализуется в митохондриях почечных клеток, и реакция гидроксилирования требует присутствия НАДФ-Н, молекулярного кислорода и ионов магния. Кроме того, этот фермент представляет собой оксидазу со смешанными функциями, зависимую от цитохрома Р-450. 1,25(OH)2D транспортируется белками-переносчиками плазмы в специфические клетки-мишени кишечника и скелета, где и оказывает свое биологическое действие. О точной природе белков плазмы, участвующих в транспорте витамина D и его метаболитов, известно мало. По-видимому, они являются a-глобулинами, но не ясно, один или несколько белков выполняют эту транспортную функцию.
Рис. 3 — 21. Начальные этапы биосинтеза витамина D. 7-Дегидрохолестерин (провитамин D), образующийся из ацетил-СоА, накапливается в коже, где в ответ на солнечное или ультрафиолетовое излучение вследствие фотометаболизма превращается в витамин В3 (холекальциферол) через промежуточные стадии, включающие образование превитамина D.
Механизм действия 1,25(OH)2D, очевидно, сходен с механизмом действия надпочечниковых и половых стероидов тем, что в нем участвует связывание дигидроксилированного витамина с цитозольными рецепторными белками. Витаминорецепторный комплекс затем транслоцируется в ядро, в котором он стимулирует синтез РНК и в результате синтез связывающих и/или транспортирующих кальций белков. Современные данные убедительно свидетельствуют о том, что 1,25(OH)2D является конечной активной формой витамина и что она представляет собой конечный продукт последовательных реакций гидроксилирования. Через несколько часов после введения животным меченого 1,25 (ОН)2D, когда уже отчетливо виден транспорт кальция в кишечнике и скелете, большую часть меченого вещества удается обнаружить в неизмененном виде; это свидетельствует о том, что для проявления биологической активности дальнейший метаболизм не требуется. Некоторые исследователи, однако, в экстрактах кишечника идентифицировали небольшие количества трижды гидроксилированного метаболита — 1,24,25-триоксивитамина D, — причем кишечник содержит, по-видимому, и фермент, способный гидроксилировать 1,25 (ОН)2D в 24-м положении. Таким образом, возможно, хотя и не доказано, что определенная часть биологической активности 1,25(OH)2D в кишечнике обусловлена его гидроксилированием в 1,24,25 (ОН)2D. Помимо уже описанных реакций гидроксилирования, в почках и, вероятно, в других тканях присутствуют активности, гидроксилирующие 25-OHD в 24-м положении, что приводит к образованию 24,25 (ОН)2D. Биологические эффекты этого особого дважды гидроксилированного метаболита выяснены неполностью. По крайней мере, одна из его функций могла бы заключаться в ингибировании секреции паратиреоидного гормона (см. далее).
Биосинтетический путь образования биологически активного витамина D через последовательные реакции гидроксилирования отличается от пути образования стероидных гормонов надпочечников по крайней мере одним интересным аспектом. Все ферментативные стадии, необходимые для гидроксилирования и синтеза стероидных гормонов надпочечников, происходят в одном и том же органе — коре надпочечников, и в одной и той же клетке коры, хотя и в разных субклеточных органеллах. В отличие от этого, различные этапы гидроксилирования на пути синтеза ди- и тригидроксилированных метаболитов витамина D происходят по крайней мере в трех разных органах (кожа, печень и почки), что делает необходимым существование высоко избирательных процессов захвата, ферментативной модификации и выделения метаболитов, равно как и транспорта промежуточных метаболитов из органа в орган через кровоток. Факт столь разительного отличия путей биосинтеза, происходящего в ходе последовательного гидроксилирования этих двух видов стероидных гормонов безусловно интересен. Хотя причины таких различий не известны, можно было бы предположить, что они связаны с эволюцией механизма, обеспечивающего существование множества пунктов, в которых происходит регуляция образования активной формы витамина D. РЕГУЛЯЦИЯ Главная регулируемая стадия биосинтеза витамина D локализуется на уровне превращения 25-OHD в 1,25 (ОН)2D под влиянием 1a-гидроксилазы 25-OHD в почках. Биосинтез витамина может в какой-то степени регулироваться и на уровне 25-гидроксилирования в печени, а также на уровне превращения провитамина D в витамин D в коже, но общее значение этих регуляторных этапов не выяснено.
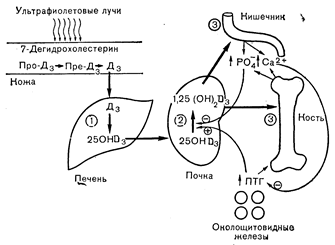
Рис. 3—22. Схематическое изображение предполагаемых пунктов регуляции в процессе метаболизма витамина D. 1 — 25-гидроксилирование в печени; 2 — 1-гидроксилирование в почках: паратиреоидный гормон стимулирует, а гиперфосфатемия подавляет превращение 25-оксивигамина D3 в 1,25-диоксивитамина D3: 3 — действие 1,25-диоксивитамина D3 на цитозольные рецепторы в кишечнике и кости — главных органах-мишенях (НаЬег J.F., Mahaffey J.E., Ann. Rev. Med., 1978, 29, 327).
С физиологической точки зрения важно, что активность почечной 1a-гидроксилазы 25-OHD находится в обратной зависимости от уровня ионизированного кальция во внеклеточной жидкости. Так, снижение уровня ионизированного кальция в плазме приводит к усилению образования 1,25 (ОН)2D из его предшественника 25-OHD и, наоборот, повышение уровня кальция подавляет образование дигидроксилированного метаболита. В первом случае всасывание кальция в кишечнике и резорбция его из скелета стимулируются, тогда как во втором случае эти процессы тормозятся и, таким образом, происходит обратный сдвиг уровня кальция во внеклеточной жидкости в направлении его нормализации. Однако кальций, вероятно, изменяет активность 1a-гидроксилазы не непосредственно. Он осуществляет свое влияние опосредованно путем регуляции высвобождения паратиреоидного гормона в кровь, а паратиреоидный гормон уже действует на почки, регулируя степень гидроксилирования в 1-м положении (рис. 3—22). По-видимому, это действие паратиреоидного гормона на процесс 1-гидроксилирования также не прямое, а опосредуется влиянием гормона на трансмембранные потоки фосфатного иона в клетках почечных канальцев. Активность la-гидроксилазы, очевидно, непосредственно зависит от окружающей концентрации фосфатного иона; гипофосфатемия стимулирует, а гиперфосфатемия угнетает образование 1, 25(OH)2D. Помимо фосфатных ионов, оказывающих сильное влияние на. скорость образования 1,25 (ОН)2D, другие факторы могут регулировать или модулировать активность 1a-гидроксилазы и в результате—количество 1,25 (ОН)2D, продуцируемое почками. К таким факторам относятся пролактин, половые стероиды, глюкокортикоиды и инсулин. Относительное значение этих гормонов в регуляции биосинтеза витамина D в настоящее время не известно, по возможность участия некоторых гормонов гипофиза половых желез и поджелудочной железы в регуляции биосинтеза и метаболизма витамина D открывает новые интересные области исследования сложных взаимоотношений гормональных эффектов в регуляции метаболизма кальция в костях скелета.
|
||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 236; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.54.63 (0.007 с.) |