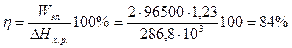Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методика измерения ЭДС и электродных потенциалов ⇐ ПредыдущаяСтр 6 из 6
1. Принцип компенсационного метода Поггендорфа (1848)
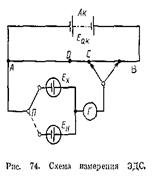
2. Схема измерения, 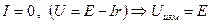
3. Расчет ЭДС:
Диффузионный потенциал и механизм его возникновения 1.Природа возникновения потенциала в: а) Схема: б) Образование ДЭС на границе раздела фаз из-за в) установление стац-ного режима переноса ионов: г) г) уравнение Гендерсона-Планка (1907) для 1-1-ного электролита: Методы устранения диффузионного скачка потенциала а) солевой мостик, принцип действия – 2 противоположно направленных скачка потенциала, компенсирующих друг друга б) введение в контактирующие р-ры индифферентного эл-та в) элементы с одним эл-том
Зависимость ЭДС гальванического эл-та от температуры 1. Уравнение, определяющее зависимость а) б) анализ: 2. Электрохимическая форма основного уравнения т-ки
3. Анализ работы гальванического элемента а) б) в) 1) 2) 3) Влияние давления на ЭДС гальванического элемента 1. б) Применение измерений ЭДC 1. Расчет т/д функций химических реакций, протекающих в г.э.
Определение констант равновесия химических реакций
Определение активностей и коэфф. активностей эл-тов а) обычно – элементы без жидкостного контакта 1) элемент: 2) реакция: 3) ур-ние Нернста:
б) случай, когда величина
4. Определение а) электроды, используемые для определения б) схема цепи: индикаторный электрод –электрод сравнения
в) стеклянный электрод 1) схема стеклянного электрода,
2) природа возникновения потенциала – ионный обмен, т.е. обмен между ионами щелочного металла, содержащимися в стекле, и ионами водорода раствора:
3) условная запись и потенциал электрода,
4)
5) линейная зависимость 6) достоинство - потенциал не искажается присутствием в растворах окислителей и восстановителей, электродных ядов) 5. Определение 1) а) 2 подхода к электроду: б)
2) Если левый электрод рассматривать как эл-д 1-го рода, то:
6. Потенциометрическое титрование а) суть потенциометрического метода определения эквивалентной точки. Cнятие зависимости
в) дифференциальная кривая титрования г) применение в случае мутных и окрашенных растворов г) другие области применения метода потенциометрического титрования (осаждение, комплексообразование) Химические источники тока 1. Любой хим. г. э. – источник электрического тока а) гальванич. элементы. - автономные источники электропитания б) нет мех частей, бесшумны, способны к длит. эксплуатации б) от карм. фонариков до энергоустановок космич. кораблей 2. Первичные (одноразового действия) источники тока Элемент Лекланше (1868):
Длительность эксплуатации ограничивается - запасом активной массы отрицательного электрода 3. Вторичные источники тока – многократно используемые а) Свинцовый кислотный аккумулятор,
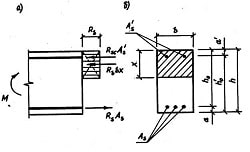
б) в процессе разряда – оба электрода покрываются в) Принцип работы аккумулятора: 4. Топливные элементы а) современные теплосиловые установки:
б) определение топливного эл-та как устройства, в котором химическая энергия топлива путем электрохимического окисления непосредственно преобразуется в электрическую в) водородно-кислородный элемент,
г) в отличие от обычных гальванических элементов восстановитель (топливо) и окислитель (кислород) не являются его составной частью, а подаются извне и энергия вырабатывается, пока в него поступают топливо и окислитель. Электроды т.э. не вступают в токообразующие реакции и не расходуются в процессе работы. Ресурс работы т.э. определяется запасом топлива и окислителя и не зависит от активной массы анода. д) недостаток – малая скорость процесса: необходим электрокат ализатор!
|
||||||||
|
Последнее изменение этой страницы: 2017-01-25; просмотров: 245; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.221.172.50 (0.029 с.) |
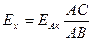 ,
, 
 , где
, где 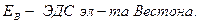
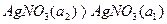
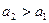
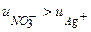

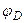 не явл. т/д величиной, но стационарной (
не явл. т/д величиной, но стационарной (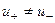 )
)
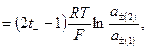
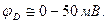
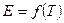
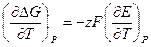
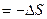
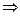
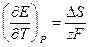 ,
, 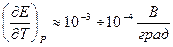
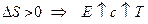 ,
, 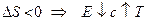 ,
, 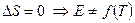
 , где
, где 

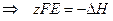
 ,
, 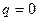
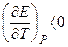
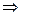

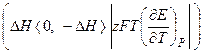 ,
, 
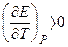
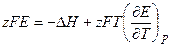 ,
, 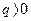
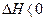
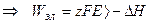


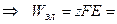
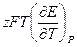
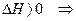
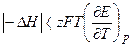

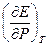

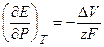
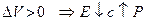 . Величина
. Величина 
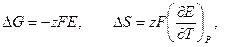
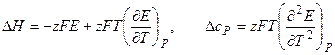
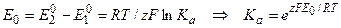
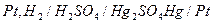
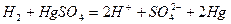
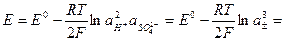
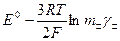
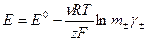
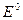 неизвестна
неизвестна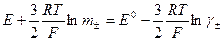 ,
, 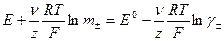
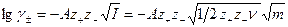
 , график
, график 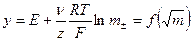

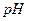 раствора
раствора
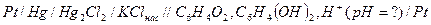

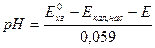
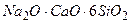 , стекл. шарик,
, стекл. шарик, 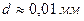


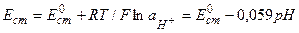
 - находят используя буферные растворы с известным значением
- находят используя буферные растворы с известным значением 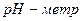 :
: 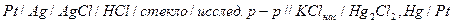

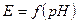 выполняется для
выполняется для 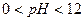 ,
,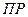 малорастворимых соединений
малорастворимых соединений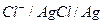 ,
, 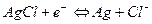
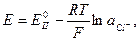


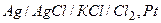
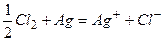
 ,
, 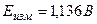
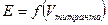 .
.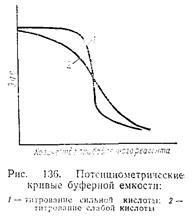 б) титрование кислоты щелочью с использованием стеклянного электрода. Характер кривой
б) титрование кислоты щелочью с использованием стеклянного электрода. Характер кривой 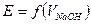 .
.
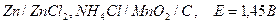
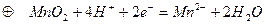 ,
, 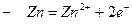
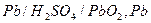

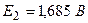
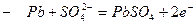

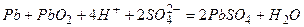
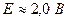


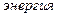 ,
, 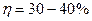 .
.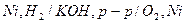 :
: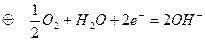


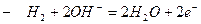
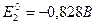
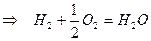
 (реакция горения водорода)
(реакция горения водорода)