Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Качественные цветные реакции на функциональные группы белков и аминокислот
При взаимодействии белка с отдельными химическими веществами возникают окрашенные продукты реакции. Образование их обусловлено присутствием в молекуле белка той или иной аминокислоты, имеющей в своем составе определенную химическую группировку. Значение качественных цветных реакций на функциональные группы белков и аминокислот в том, что они дают возможность обнаружить присутствие белка в биологических жидкостях, растворах, лекарственных препаратах и идентифицировать индивидуальные аминокислоты. Эти реакции применяют как для качественного, так и для количественного определения белка и содержащихся в нем аминокислот.
v Биуретовая реакция на пептидную связь (Пиотровского). Биуретовая реакция открывает пепетидную связь Её способны давать вещества, которые содержат не менее двух пептидных связей. Положительную биуретовую реакцию отдельные аминокислоты не дают, за исключением гистидина (His), серина (Ser), треонина (The) и аспарагина (Asn), с которыми биуретовая реакция получается при условии больших концентраций их в растворе. При добавлении сернокислой меди к сильнощелочному раствору белка или полипептида образуются соединения меди с пепетидной группировкой, окрашенные в красно-фиолетовый или сине-фиолетовый цвет в зависимости от длины полипептидной цепи. Раствор белка даёт сине-фиолетовое окрашивание, а продукты неполного гидролиза (пептоны) – розовое или красное окрашивание. Принцип метода. В сильно щелочной среде пептидные группы полипептидных цепей переходят в енольную форму, которая, взаимодействуя с ионами Cu2+, образует окрашенный (фиолетового цвета) биуретовый комплекс. При этом енольная форма полипептида, образованная в сильнощелочной среде, дает отрицательный заряд, и ее кислород, взаимодействуя с медью, образует ковалентную связь, а медь, взаимодействуя с атомами азота, образует координационные связи.
Енольная форма пептидной связи (
Комплекс фиолетового цвета Исследуемый материал и реактивы 1. Раствор яичного белка (1%). 2. Гидроксид натрия(10%). 3. Сернокислая медь (1%). Ход работы К 5 каплям раствора белка прибавляют 3 капли 10% раствора едкого натра и 1 каплю 1% раствора сернокислой меди и перемешивают. Содержимое пробирки приобретает сине-фиолетовый цвет.
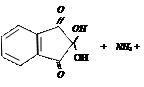
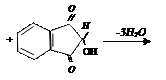
Нельзя добавлять избыток сернокислой меди, так как синий осадок гидрата окиси меди маскирует характерное фиолетовое окрашивание биуретового комплекса белка. v Нингидриновая реакция. Нингидриновая реакция характерна для аминогрупп, находящихся в альфа-положении. Растворы белка, альфа-аминокислот и пептидов при нагревании с нингидрином дают синее или фиолетовое окрашивание. Принцип метода. В этой реакции альфа-аминокислоты и пептиды окисляются нингидрином и подвергаются окислительному дезаминированию и декарбоксилированию с образованием аммиака, альдегида и СО2. Нингидрин восстанавливается и связывается со второй молекулой нингидрина посредством молекулы аммиака, образуя продукты конденсации, окрашенные в синий, фиолетовый, красный, а в случае пролина – в желтый цвет. Нингидриновая реакция используется для количественного определения альфа-аминокислот в аминокислотных анализаторах, а также широко используется в хроматографическом анализе и для колориметрического количественного определения аминокислот.
1.
окисленный восстановленный (гидриндантин (бесцветный))
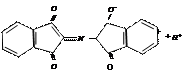
2. нингидрин нингидрин продукт конденсации окисленный восстановленный пурпур Роумэна (сине-фиолетовый)
|
|||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 1614; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.143.239.231 (0.005 с.) |
 в белке.
в белке.
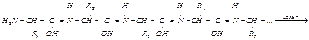
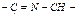 )
)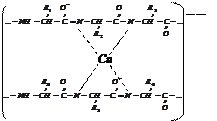

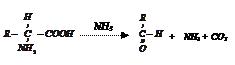
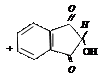
 нингидрин аминокислота альдегид нингидрин
нингидрин аминокислота альдегид нингидрин