

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Второй закон (начало) термодинамики
Содержание книги
- Закон Авогадро ди Кваренья (1811 Г. )
- Типы и номенклатура неорганических веществ
- Кислотные и основные гидроксиды
- Характеристика состояния электронов в атоме квантовыми числами
- Заполнение электронных орбиталей многоэлектронных атомов
- Структура периодической системы элементов Д.И. Менделеева
- Ковалентной называется связь, которая образуется между двумя атомами за счет одной или нескольких общих электронных пар, одновременно принадлежащих им обоим.
- Связь между всеми положительно заряженными ионами и свободно перемещающимися в междоузлиях кристаллической решетки электронами называется металлической
- Гибридизация – это прием построения одинаковых по энергии и форме гибридных валентных орбиталей путем линейной комбинации (суммы) АО в методе валентных связей
- Метод Гиллеспи (метод отталкивания электронных пар валентной оболочки)
- Метод молекулярных орбиталей (МО)
- Молекулярные орбитали двухатомных молекул элементов второго периода
- Связь атома водорода, связанного полярной ковалентной связью с атомом высоко электроотрицательного элемента с другим атомом высокоэлектроотрицательного элемента называется водородной.
- Дисперсионное взаимодействие
- Структура некоторых молекул и ионов
- Количество теплоты, полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил.
- Второй закон (начало) термодинамики
- Направление протекания реакций
- Факторы, влияющие на скорость химической реакции
- Скорость реакции и равновесие
- Факторы, влияющие на величину константы равновесия.
- Связь различных способов выражения концентрации растворов
- Масса газа, растворяющегося при постоянной температуре в данном объеме жидкости, прямо пропорциональна парциальному давлению газа.
- Относительное понижение парциального давления пара растворителя над раствором не зависит от природы растворённого вещества и равно его мольной доле в растворе.
- Явление электролитической диссоциации
- Сущность явления электролитической диссоциации
- На ионы и равна отношению числа распавшихся молекул (формульных единиц)
- Растворы сильных электролитов. Активная концентрация
- В зависимости от ионности раствора при 298 К
- Электролита (произведение растворимости)
- Произведение растворимости некоторых малорастворимых
- Ионов водорода, моль/л; б – водородного показателя рН
- Константы диссоциации некоторых слабых электролитов
- Меняется рН раствора, называется гидролизом.
- Реакции без и с изменением степени окисления
- Определение стехиометрических коэффициентов в уравнениях окислительно-восстановительных реакций.
- Стандартные потенциалы окислительно-восстановительных реакций
- Li, Rb, К, Ва, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H, Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au.
- Соединения, в которых каждый лиганд связан с комплексообразователем двумя ковалентными связями, одна из которых образована по обменному, а другая по донорно-акцепторному механизму.
- Диссоциация комплексных соединений
- Квантовомеханические теории строения комплексных соединений
- Гибридизация орбиталей и структура комплексов
- Константы устойчивости комплексных соединений
Второй закон определяет направление самопроизвольного протекания процессов, в том числе и химических реакций.
Самопроизвольным называется процесс, который протекает самостоятельно без воздействия внешних факторов (без затраты энергии из окружающей среды и совершения работы внешней средой над системой). Такие процессы называются положительными. Они идут без затраты работы. Более того, с помощью этих процессов можно получить работу.
Например, если соединить два сосуда — заполненный газом и пустой, то газ самопроизвольно заполнит весь объем. Переход теплоты от горячего тела к холодному, диффузия вещества из концентрированного раствора в разбавленный, равно как и любой другой процесс, приближающий систему к состоянию термодинамического равновесия. Взаимодействие металлического натрия с водой при н. у. также происходит самопроизвольно. Обратные самопроизвольным процессы, которые можно осуществить, оказав внешнее воздействие на систему в виде тепла, работы и других видов воздействия называются отрицательными. Они могут идти только при затрате энергии извне или в сопряжении с положительными процессами внутри системы. В результате отрицательного процесса система удаляется от состояния равновесия.
Для исследователя необходимо иметь критерий, с помощью которого можно было бы предсказать направление самопроизвольного протекания процесса.
Существует еще одна функция состояния, которая с учетом первого начала термодинамики позволяет предсказать направление протекания процесса в изолированных системах. Такой функцией состояния является энтропия (S).
Интерпретировать энтропию можно как с точки зрения макроскопического состояния системы, так и с точки зрения микроскопического (статистического).
Если рассматривать систему в целом, то в обратимом процессе, протекающем при постоянной температуре, изменение энтропии будет равно:
D S = 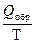
Для необратимого процесса это равенство превращается в неравенство:
D S >  , ,
Где Q – количество теплоты поглощенное (отданное) системой, Т – абсолютная температура процесса, ΔS – увеличение (уменьшение) энтропии системы.
Обратимыминазываются процессы перехода из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний.
При этом в исходное состояние возвращается не только система, но и среда.
Обратимые и необратимые процессы, пути изменения состояния термодинамической системы. Обратимый процесс возможен, если и в системе, и в окружающей среде он протекает равновесно. При этом предполагается, что равновесие существует между отдельными частями рассматриваемой системы и на границе с окружающей средой. Обратимый процесс - идеализированный случай, достижимый лишь при бесконечно медленном изменении термодинамических параметров.
Пример:
Если дистиллированную воду поместить в холодильник, температура в котором меньше нуля, то возможно получить переохлажденную воду (а не лед), температура которой будет ниже нуля. Встряхивания достаточно, чтобы произошла кристаллизация и превращение в лед воды. Обратно превратить лед в воду при этой (отрицательной) температуре не удастся, так как при нагревании он расплавится только при нуле градусов Цельсия. Это пример необратимого процесса.
Процессы, наблюдаемые в природе, протекают самопроизвольно в одном направлении. Это необратимые процессы.
Поскольку энтропия является функцией состояния, то ее изменение не зависит от пути перехода системы из одного состояния в другое, а определяется только значениями энтропии для системы в исходном и конечном состояниях. Размерность энтропии [S]=Дж/моль·К.
Существует много формулировок второго начала термодинамики. Приведем одну из них.
|