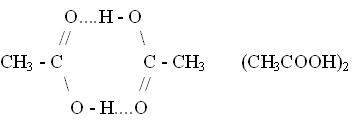Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Связь атома водорода, связанного полярной ковалентной связью с атомом высоко электроотрицательного элемента с другим атомом высокоэлектроотрицательного элемента называется водородной.
Механизм образования водородной связи – донорно-акцепторный. Донор – молекула или ион, имеющий неподеленную пару электронов. Акцептор – протон (Н+). Очевидно, что водородная связь легко становится ковалентной при сближении атомов (ионов) водорода и высокоэлектроотрицательного элемента и наоборот, так как постоянно происходит перемещение ионов в растворе, их сближение и удаление друг от друга. Деление на ковалентную связь протона с одним и водородную с другим высокоэлектроотрицательным ионом условно. Стабильность системы определяется положением протона в поле действия двух анионов. В системе FHF- в и некоторых других соединениях атом водорода находится приблизительно посредине между двумя электроотрицательными атомами, образуя половину связи с каждым из них. Большинство же водородных связей несимметричны, одно межатомное расстояние больше другого на 50-80 пм. Энергия более слабой связи обычно составляет около 10-40 кДж×моль-1, что и называется энергией водородной связи. H - O....H - O....H - O....H - O....H - O....H - O....H - O....H - O....H - O....H - O | | | | | | | | | | H H H H H H H H H H (H2O) n
Многие особые свойства неорганических и органических молекул, например димеризация жирных кислот, объясняются образованием водородных связей. Водородная связь - особенно важная структурная особенность белков и нуклеиновых кислот.
енаминокетоне (Б) (Рис.5.15.). Один атом водорода аминогруппы (NH2) cвязан внутримолекулярной водородной связью с кислородом соседней карбонильной группы, а второй может быть связан межмолекулярной водородной связью с кислородом соседней молекулы ацетилацетона (Б) (Рис. 5.15.).
Рис.5.15. Образование внутримолекулярной и межмолекулярной водородной связи в ацетилацетоне (А) и енаминокетоне (B).
Если бы водородные связи отсутствовали, то вода плавилась бы при –100°С, а кипела при –80°С. Взаимодействие между молекулами воды оказывается достаточно сильным, таким, что даже в парах воды присутствуют димеры и тримеры состава (H2O)2, (Н2O)3 и т. д. В растворах же могут возникать длинные цепи ассоциатов поскольку атом кислорода имеет две неподеленные пары электронов.
Внутримолекулярные водородные связи играют основную роль в образовании пептидных цепей, которые определяют строение белков. По-видимому, наиболее важным и, несомненно, одним из наиболее известных примеров влияния внутримолекулярной водородной связи на структуру является дезоксирибонуклеиновая кислота (ДНК). Молекула ДНК свернута в виде двойной спирали. Две нити этой двойной спирали связаны друг с другом водородными связями.
|
||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-30; просмотров: 274; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.199.51 (0.005 с.) |