Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема: Определение степени и химизма засоления почв лабораторными и расчетными методамиСодержание книги
Поиск на нашем сайте К категории засолённых почв относятся солончаки, солонцы, солоди. Отличительная их агроэкологическая особенность- содержание в составе токсичных солей, превышающие допустимые пределы для роста и развития растений. Водно-растворимые соединения (органические, минеральные, органо-минеральные) при обработке почвы водой переходят в раствор, т.е. в в водную вытяжку. Из водно-растворимых солей в почвах наиболее часто встречаются сульфаты, хлориды и бикарбонаты кальция, магния, натрия. Более токсичными солями для растении являются: Na2CO3, все хлориды, а из сульфатов Na2SO4, MgSO4.
Задание к выполнению работы: 1. Определить степень и химизм засоления почв. 2. Разработать мероприятия по рациональному использованию и повышению плодородия засолённых почв. : Ход анализа а) приготовление водной вытяжки 1. 100 г сухой почвы помещают в коническую колбу и заливают ее пятикратным количеством дистиллированной воды.
б) определение общей суммы воднорастворимых веществ (сухого остатка) Сухой остаток представляет собой сумму всех водно-растворимых веществ перешедших в вытяжку. С помощью пипетки берут 50 мл вытяжки и помещают ее в предварительно взвешенный стеклянный бюкс или фарфоровую чашку. Содержимое выпаривают на водяной бане и высушивают в термостате при1500 до постоянного веса. Охлаждают в эксикаторе и взвешивают. Вычисляют по формуле: m = а*10* КГ, где m- общее содержание воднорастворимых солей, % к почве а - масса осадка после выпаривания и высушивания, г 10- коэффициент для перевода в % так как вся навеска 100 г Кг – коэффициент гигроскопичности
в) определение рН водной вытяжки Берут 5 мл вытяжки и определяют рН потенциометрически или колориметрически по шкале образцовых растворов. г) определение хлор-ионов В пробирку наливают 5 мл водной вытяжки и подкисляют ее двумя каплями 10% раствора H2SO4. К фильтрату прибавляют 5-7 капель 5% раствора AgNO3 и содержимое перемешивают. При присутсвии солей хлора образуется осадок AgCI.
д) определение сульфат иона Наличие иона SO4 в водной вытяжке можно установить действием на ее раствора хлористого бария. Если вытяжке содержатся в заметных количествах сульфата, то они, вступая во взаимодействие с BaCI2 образуют нерастворимую соль BaSO4. Наливают в пробирку около 5 мл водной вытяжки. Затем приливают в пробирку 1 мл 10% раствора BaCI2 и кипятят жидкость в течение 1 минуты. По количеству выпавшего осадка или характера помутнения вытяжки отмечают: отсутствует, мало, много, очень много. е) определение кальций иона Присутствие кальция в водной вытяжке устанавливается с помощью раствора щавелевокислого аммония, т.к. соединения кальция с этой солью образует нерастворимый осадок. Реакция происходит по следующей схеме:
В пробирку собирают около 5 мл вытяжки, добавляют в нее 5 мл щавелевокислого аммония (4% р-р) и подкисляют ее несколькими каплями 10% раствора уксусной кислоты. Содержимое пробирки доводят до кипения. По количеству осадка щавелевокислого кальция отмечают: соединения кальция отсутствуют, мало, много, очень много. По преобладанию тех или иных ионов определяют тип (химизм) засоления, а по характеру осадки степень засоления. Результаты определения степени и химизма засоления почв
Оборудование: пробирки, колбы, воронки, фильтры, спиртовки. Реактивы 1.10% раствор H2SO4 – (61 мл на 1 л воды); 2. 5% AgNO2 (5 г AgNO3 на 100 мл воды); 3. 10% раствор BaCI2 (10 г BaCI2 на 100 мл воды); 4. 4% раствор (NH4)2C2O4 – (4 г (NH4)2C2O4 на 100 мл воды); 5. 10% раствор СН3СООН – (97 мл СН3СООН на 1 л воды).
Вопросы для самоконтроля
1. Условия, факторы, способствующие процессам соленакопления в почве. 2. Актуальность изучения засолённых почв. 3. Влияние токсичных солей на свойства почв, физиологические процессы роста и развития растений. 4. Какие соли относятся к токсичным? Ряд токсичности солей. 5. Приёмы регулирования солевого режима почв и рационального использования засолённых почв. 6. Как определяется химизм (тип) засоления почв?
|
|||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-28; просмотров: 632; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.5 (0.009 с.) |


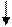 NaCI+AgNO3 = AgCI +NaNO3 По количеству выпавшего осадка или характера помутнения отмечают: хлориды отсутствуют, мало, много, очень много.
NaCI+AgNO3 = AgCI +NaNO3 По количеству выпавшего осадка или характера помутнения отмечают: хлориды отсутствуют, мало, много, очень много. Na2SO4 + BaCI2 = BaSO4 +2 NaCI
Na2SO4 + BaCI2 = BaSO4 +2 NaCI