Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теория растворов слабых электролитов.Содержание книги Поиск на нашем сайте Процесс диссоциации слабых электролитов является обратимым: KtnAnm ⇄ nKtm+ + mAnn- и характеризуется константой равновесия, которая в данном случае называется константой диссоциации:
Величина Слабые одноосновные кислоты типа HA диссоциируют по общему уравнению: HA ⇄ H+ + A-. Константа диссоциации равна:
Здесь индекс a (acidum) указывает на кислотный тип диссоциации. Например, для слабой кислоты HNO2 можно записать: HNO2 ⇄ H+ + NO2-,
Аналогичным образом записывают константы диссоциации оснований: NH3×H2O ⇄ NH4+ + OH-.
Индекс b (basicum) обозначает основный тип диссоциации. Диссоциация многоосновных кислот (многокислотных осно-ваний) происходит в несколько ступеней, каждая из которых характе-ризуется своей константой. Например, для фосфорной кислоты имеем:
Видно, что Суммарная константа диссоциации определяется соотношением:
Несложно видеть, что суммарная константа диссоциации
На практике вместо величин
На основании значений чем больше значение чем меньше значение Величины констант диссоциации для некоторых слабых электролитов представлены в таблице 1. Таблица 1. Константы диссоциации некоторых слабых электро-литов при 298 К.
Таким образом, при постоянной температуре сравнительную силу слабых электролитов определяют две величины: степень диссо-циации a и константа диссоциации Действительно, для бинарного электролита, диссоциирующего по уравнению: KtAn ⇄ Kt+ + An- можно записать:
Представив
где С0(KtAn) – общая концентрация электролита, получим:
Данное соотношение выражает закон разведения Оствальда. Для слабых электролитов a << 1, поэтому можно записать:
или:
Таким образом, закон Оствальда можно сформулировать следующим образом: Степень диссоциации слабого электролита возрастает с разбавлением раствора.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 356; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.151 (0.008 с.) |


 зависит от природы электролита и растворителя, а также от температуры, но не зависит от концентрации раствора.
зависит от природы электролита и растворителя, а также от температуры, но не зависит от концентрации раствора.

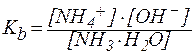



 . Данное неравенство соблюдается для всех без исключения случаев ступенчатой диссоциации. Последовательное снижение величин констант диссоциации легко объяснимо: с увеличением отрицательного заряда иона отщепление каждого последующего протона становится все более энергоемким.
. Данное неравенство соблюдается для всех без исключения случаев ступенчатой диссоциации. Последовательное снижение величин констант диссоциации легко объяснимо: с увеличением отрицательного заряда иона отщепление каждого последующего протона становится все более энергоемким.
 равна произведению констант диссоциации отдельных ступеней:
равна произведению констант диссоциации отдельных ступеней:
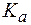 и
и  часто используют значения
часто используют значения  и
и  , которые рассчитываются следующим образом:
, которые рассчитываются следующим образом:














 .
.