
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Коэффициент перед восстановителем в уравнении ⇐ ПредыдущаяСтр 4 из 4
AsH3 + AgNO3 + H2O ® H3AsO4 + Ag ¯ + HNO3 равен
1) 1; 2) 2; 3) 3; 4) 4
10. Укажите формулу негорючего вещества. 1) CH4 2) CH≡CH 3) CH3—CH2OH 4) CCl2F2
Смесь двух неорганических солей разложили при нагревании без остатка. Выделившийся при этом газ для удаления паров воды пропустили через склянку с концентрированной серной кислотой. Полученный газ А имел объем 11,2 л и относительную плотность по водороду 22. Если газ А пропускать через трубку с твердой щелочью, то объем уменьшается в 2 раза, а плотность не изменяется. При пропускании газа А через трубку с раскаленной медной стружкой его объем не изменяется, а плотность уменьшается. Взаимодействие газа А с раскаленным углем приводит к увеличению объема и уменьшению плотности. Определите качественный и количественный состав исходной смеси солей. Запишите уравнения химических реакций. Найдите ошибку в проведении эксперимента. Все объемы газов приведены к нормальным условиям
54. Смесь двух неорганических солей разложили при нагревании без остатка. Выделившийся при этом газ для удаления паров воды пропустили через склянку с концентрированной серной кислотой. Полученный газ А имел объем 11,2 л и относительную плотность по водороду 22. Если газ А пропускать через трубку с твердой щелочью, то объем уменьшается в 2 раза, а плотность не изменяется. При пропускании газа А через трубку с раскаленной медной стружкой его объем не изменяется, а плотность уменьшается. Взаимодействие газа А с раскаленным углем приводит к увеличению объема и уменьшению плотности. Определите качественный и количественный состав исходной смеси солей. Запишите уравнения химических реакций. Найдите ошибку в проведении эксперимента. Все объемы газов приведены к нормальным условиям. (IX—зон.—89.)
Решение: При нагревании без остатка разлагаются соли аммония. Т.к. при поглощении щелочью половины объема газа плотность газа не изменяется, это значит, что газ А – это смесь газов с одинаковыми молярными массами и одинаковыми объемами. М(А) = 22∙2 = 44 г/моль. Такую массу имеет СО2 и N2O, что соответствует условию задачи: 1) NH4HCO3 2) (NH4)2CO3 3) NH4NO3 Т.е. исходная смесь содержит 0,25 моль гидрокарбоната аммония (или 0,125 моль карбоната аммония) и 0,25 моль нитрата аммония.
Уравнения реакций: СО2 + 2NaOH = Na2CO3 + H2O (объем уменьшается в 2 раза, а плотность не изменяется, т.к. остается ½ N2O) 1V 1V N2O + Cu = CuO + N2 (объем не изменяется, а плотность уменьшается D(Н2) = 28/2 = 14 г/моль или для смеси газов:
1V 1V + 1V N2O + C = CO2 + N2 1V 2V CO2 + C = 2CO CO2 + C = 2CO (увеличение объема и уменьшение плотности, т.к. в смеси остается азот и угарный газ). Ошибка эксперимента: H2SO4 (неизвестного состава) поглощает NH3. Например, H2SO4 + 2NH3 = (NH4)2SO4
|
|||||
|
Последнее изменение этой страницы: 2019-12-15; просмотров: 143; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.186.173 (0.007 с.) |
 NH3↑ + H2O↑ + CO2↑
NH3↑ + H2O↑ + CO2↑ ;
; 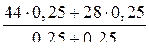 = 36 г/моль; D(Н2) = 36/2 = 18 г/моль
= 36 г/моль; D(Н2) = 36/2 = 18 г/моль


