
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Вычислить константу равновесия для гомогенной системы
4NH3(г) +3O2(г) <=> 2N2(г) + 6H2O(г), если исходные концентрации NH3(г) и O2(г) соответственно равны 6,0 и 5,0 моль/л, а равновесная концентрация N2(г) равна 1,8 моль/л.
Равновесная концентрация исходных веществ равна разности исходной концентрации и концентрации прореагировавших исходных веществ. Равновесная концентрация продуктов реакции равна количеству образовавшихся продуктов реакции. Обозначим через х количество моль прореагировавших или образовавшихся веществ. Тогда с учетом коэффициентов в уравнении реакции отношения концентраций во второй строке под уравнением реакции равны Последовательность расчетов равновесных концентраций веществ, участвующих в реакции, показана ниже
По условию задачи равновесная концентрация N2 равна 1,8 моль/л. [NH3] = 6,0 – 4 · 0,9 = 2,4 моль/л; [O2] = 5,0 – 3 · 0,9 = 2,3 моль/л; [N2] = 1,8 моль/л. [H2O] = 6,0·0,9 = 5,4 моль/л; Ответ: Kс = 198,95.
6. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА РАСТВОРОВ УРОВЕНЬ А 1. Написать формулы закона Рауля для водных растворов неэлектролитов и электролитов (давление насыщенного пара). Ответ:
2. Написать формулы закона Рауля для водных растворов неэлектролитов и электролитов: а) изменения температур кипения растворов; б) изменения температур замерзания растворов. Ответ:
а)
б)
Написать формулы закона Вант-Гоффа для водных растворов неэлектролитов и электролитов. Ответ:
УРОВЕНЬ В 1. Вычислить температуры кипения и замерзания водного раствора, содержащего 0,1 моль сахарозы (
cm (
где
cm (
где М ∆ t кип = 0,52 ∙ 0,21 = 0,109 ºС;
t кип р-ра = 100 ºС + 0,109 ºС = 100,109 ºС;
∆ t зам = 1,86∙0,21 = 0,391 ºС;
t зам р-ра = 0 ºС – 0,391 ºС = –0,391 ºС.
Ответ: t кип р-ра = 100,109 ºС; t зам р-ра = – 0,391 ºС. 2. В 100 г воды содержится 2,3 г неэлектролита. Раствор обладает при 25 ºС осмотическим давлением, равным 618,5 кПа. Определить молярную массу неэлектролита. Плотность раствора принять равной 1 г/см3.
с в =
где m в – масса растворенного неэлектролита, г; М в – молярная масса растворенного неэлектролита, г/моль.
π =
М в =
Ответ: молярная масса растворенного вещества равна 90,06 г/моль.
3. Определить давление насыщенного пара воды над 1,0 %-м раствором карбамида (CO(NH2)2) при 298 К, если давление насыщенного пара над водой при той же температуре равно 2,34 кПа.
где р – давление насыщенного пара воды над раствором, кПа, р o – давление насыщенного пара воды, кПа;
В 100 г 1 %-го раствора карбамида содержится 1 г карбамида и 99 г воды.
р =
Ответ: давление насыщенного пара воды над 1 %-м раствором CO(NH2)2 составляет 2,33 кПа.
УРОВЕНЬ С
1. Определить давление насыщенного пара воды над 0,05 М раствором хлорида кальция (ρ = 1,041 г/см3) при 301 К, если давление насыщенного пара над водой при этой температуре равно 3,78 кПа. Кажущаяся степень диссоциации хлорида кальция равна 0,85.
где
i – изотонический коэффициент.
α =
где α – кажущаяся степень диссоциации CaCl2; к – общее количество ионов, образующихся при полной диссоциации одной молекулы CaCl2.
CaCl2 = Сa2+ + 2Cl-
к = 3, i = 0,85(3 – 1) + 1 = 2,7,
oткуда
Для расчета берем 1 л раствора.
р = 3,78 ∙
Ответ: давление насыщенного пара над раствором равно 3,77 кПа. 2. Определить осмотическое давление 1,5 %-го раствора карбоната натрия при 25 ºС. Плотность раствора равна 1,015 г/см3. Кажущаяся степень диссоциации карбоната натрия равна 0,9.
где α – кажущаяся степень диссоциации; к – общее количество ионов, образующихся при полной диссоциации одной молекулы Na2CO3:
Na2CO3 = 2Na+ + CO32-;
к = 3, тогда i = 0,9(3 – 1)+1 = 2,8
В 100 г 1,5 % раствора содержится 1,5 г Na2CO3 и 98,5 г воды
V р-ра =
π = 2,8 ∙ 0,144 ∙ 8,314 ∙ 298 = 998,96 кПа.
Ответ: осмотическое давление 1,5 %-го раствора Na2CO3 равно 998,96 кПа. 3. Определить кажущуюся степень диссоциации соли, если водный раствор хлорида алюминия с массовой долей 1,5 % кристаллизуется (замерзает) при температуре (–0,69) ºС.
AlCl3 = Al3+ + 3Cl-
к = 4
∆ t зам = i ∙
где сm (AlCl3) = В 100 г 1,5 %-го раствора содержится 1,5 г AlCl3 и 98,5 г воды.
сm (AlCl3) =
α =
Ответ: кажущаяся степень диссоциации AlCl3 равна 0,75(75%).
ИОННО-МОЛЕКУЛЯРНЫЕ УРАВНЕНИЯ УРОВЕНЬ А 1. Написать выражение ПР и привести их табличное значение для следующих соединений PbCl2 и Ag2S.
Ответ: PbCl2(к) <=> Pb ПР Ag2S(к) <=> 2Ag ПР
т.е. растворимость Ag2S значительно меньше растворимости PbCl2. 2. Написать уравнения диссоциации, выражения констант диссоциации и привести их табличное значение для H2S. Ответ: поскольку H2S – слабый электролит, то процесс диссоциации является обратимым и протекает ступенчато:
Поскольку 3. Определить силу электролитов и написать уравнения диссоциации сильных электролитов: Zn(OH)2; HCl; H3PO4; NaOH; HCN.
Ответ: поскольку к сильным относятся кислоты HCl, HBr, HJ, HNO3, H2SO4, HClO4, а к сильным основаниям относятся LiOH, NaOH, KOH, RbOH, CsOH, Ca(OH)2, Sr(OH)2, Ba(OH)2, то Zn(OH)2 – слабый электролит; HCl – сильный электролит; H3PO4 – слабый электролит; NaOH – сильный электролит, HCN – слабый электролит. Диссоциация сильных электролитов на ионы протекает нацело:
HCl = H+ + Cl-;
NaOH = Na+ + OH-. УРОВЕНЬ В 1. Вычислить рН следующих водных растворов: а) 0,02 М HCl, б) 0,2 М KOH.
HCl – сильный электролит, α = 1,
n рН = -lg2·10-2 = -lg2 + (-lg10-2)= – 0,3 + 2 = 1,7. б) KOH = К+ + ОН-; рН = 14 – рОН; рОН = -lg c c КОН – сильный электролит, α = 1, n
рОН = –lg(2·10-1) = –lg2 + (–lg10-1) = – 0,3 + 1 = 0,7.
рН = 14 – 0,7 = 13,3.
Ответ: рН 0,02 М HCl равно 1,7; рН 0,2 М КОН равно 13,3.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-21; просмотров: 350; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.195.249 (0.101 с.) |
 = 6,0 моль/л
= 6,0 моль/л
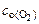 = 5,0 моль/л
[N2] = 1,8 моль/л
= 5,0 моль/л
[N2] = 1,8 моль/л
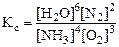 Расчет количеств прореагировавших и образовавшихся при установлении равновесия веществ производится по уравнению реакции.
Расчет количеств прореагировавших и образовавшихся при установлении равновесия веществ производится по уравнению реакции.
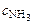 :
:  :
:  :
: 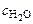 = 4: 3: 2: 6).
= 4: 3: 2: 6). =198,95.
=198,95.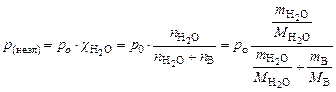 , кПа
, кПа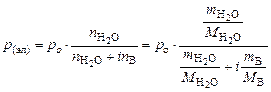 , кПА.
, кПА.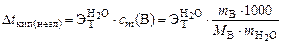 ;
;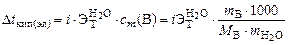 ;
; ;
;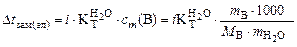
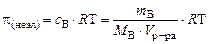 , кПа;
, кПа; , кПа.
, кПа.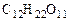 ) в 500 г раствора.
) в 500 г раствора.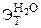 = 0,52 кг·К/моль,
= 0,52 кг·К/моль, 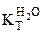 = 1,86 кг·К/моль.
= 1,86 кг·К/моль.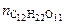 = 0,1 моль
m р-ра = 500 г
= 0,1 моль
m р-ра = 500 г
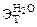 = 0,52 кг·к/моль
= 0,52 кг·к/моль
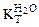 = 1,86
= 1,86
 ),
∆tзам =
),
∆tзам = 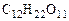 ) – моляльность сахарозы в растворе, моль/кг.
) – моляльность сахарозы в растворе, моль/кг.
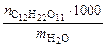 ,
,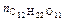 – количество растворенной сахарозы, моль.
– количество растворенной сахарозы, моль.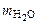 =
= 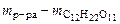 , г;
, г;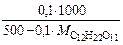
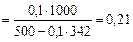 моль/кг,
моль/кг,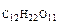 = 342 г/моль
= 342 г/моль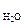 )/ρр-ра , см3.
V р-ра =
)/ρр-ра , см3.
V р-ра = 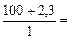 102,3 см3 = 0,102 л.
102,3 см3 = 0,102 л.
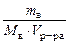 , моль/л,
, моль/л,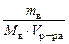 ∙ R ∙ T, кПа;
∙ R ∙ T, кПа;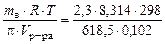 = 90,33 г/моль.
= 90,33 г/моль.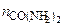 = 1,0 %
Т = 298 К
p o = 2,34 кПа
= 1,0 %
Т = 298 К
p o = 2,34 кПа
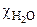
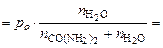 =
=  ,
,
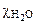 – молярная доля воды;
– молярная доля воды;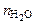 – количество воды, моль;
– количество воды, моль;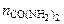 – количество CO(NH2)2, моль;
– количество CO(NH2)2, моль;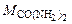 = 60 г/моль,
= 60 г/моль, 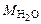 = 18 г/моль.
= 18 г/моль.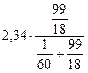 = 2,33 кПа.
= 2,33 кПа.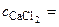 0,05 моль/л
T = 301 К
ρ = 1,041 г/см3
α = 0,85
р o = 3,78 кПа
0,05 моль/л
T = 301 К
ρ = 1,041 г/см3
α = 0,85
р o = 3,78 кПа
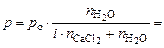
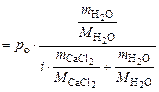 ,
,
 – количество CaCl2, моль
– количество CaCl2, моль , i = α (к – 1) + 1,
, i = α (к – 1) + 1,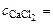
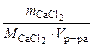 , моль/л,
, моль/л, , г
, г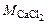 = 111 г/моль.
= 111 г/моль. m р-ра = 1000∙1,041 = 1041г.
m р-ра = 1000∙1,041 = 1041г.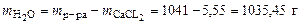 .
.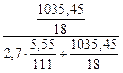 = 3,77 кПа.
= 3,77 кПа.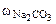 = 1,5 %
t = 25 ºС
ρ = 1,015 г/см3
α = 0,9
= 1,5 %
t = 25 ºС
ρ = 1,015 г/см3
α = 0,9
 ∙ R ∙ T, кПа;
α =
∙ R ∙ T, кПа;
α =  ; i = α(к – 1) + 1,
; i = α(к – 1) + 1,
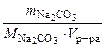 , моль/л.
, моль/л.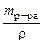 =
=  = 98,5 см3 = 0,0985 л.
= 98,5 см3 = 0,0985 л.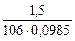 = 0,144 моль/л.
= 0,144 моль/л. = 1,86 кг·к/моль.
= 1,86 кг·к/моль.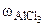 = 1,5 %
t зам р-ра = –0,69 ºС
= 1,5 %
t зам р-ра = –0,69 ºС
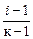 ,
где к – общее количество ионов, образующихся при полной диссоциации одной молекулы AlCl3.
,
где к – общее количество ионов, образующихся при полной диссоциации одной молекулы AlCl3.
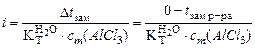
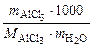 , моль/кг.
, моль/кг. = 0,114 моль/кг,
= 0,114 моль/кг,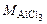 = 133,5 г/моль,
= 133,5 г/моль,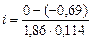 = 3,25,
= 3,25,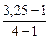 = 0,75 (75 %).
= 0,75 (75 %). 7. РАСТВОРЫ СИЛЬНЫХ И СЛАБЫХ ЭЛЕКТРОЛИТОВ. ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ.
7. РАСТВОРЫ СИЛЬНЫХ И СЛАБЫХ ЭЛЕКТРОЛИТОВ. ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ.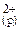 + 2Cl
+ 2Cl 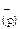 ;
; = 2 ∙ 10-5;
= 2 ∙ 10-5;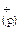 +S
+S 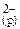 ;
;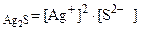 = 5,7 ∙ 10-51,
= 5,7 ∙ 10-51,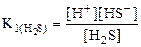 =6,0·10-8.
=6,0·10-8.
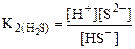 =1,0·10-14.
=1,0·10-14.
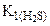 больше
больше 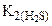 в 6∙106 раз, то можно считать, что диссоциация H2S протекает в основном по первой ступени.
в 6∙106 раз, то можно считать, что диссоциация H2S протекает в основном по первой ступени.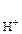 ;
;
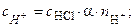
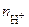 – число Н+, образовавшихся при диссоциации одной молекулы НСl,
– число Н+, образовавшихся при диссоциации одной молекулы НСl,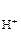 = 1, тогда
= 1, тогда 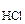 = 0,02 моль/л = 2 · 10-2 моль/л.
= 0,02 моль/л = 2 · 10-2 моль/л.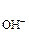 ,
, · α · n
· α · n 


