
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Выберите правильный ответ на поставленный вопрос
Работа газа. Круговой процесс. КПД кругового процесса При изобарном процессе газ с силой F двигает поршень на расстояние где
Рисунок 17. Работа газа при давлении
Работа расширения газа при изобарном процессе равна произведению давления газа на изменение его объема. Эта работа положительна при расширении газа, поскольку сила давления и перемещение поршня направлены одинаково. Если же газ сжимается, то работа силы, с которой газ действует на поршень, отрицательна. Работа газа численно равна площади заштрихованного прямоугольника, изображенного на графике (рисунок 17). При изобарном процессе Выражение для внутренней энергии
  + +  = = 
При любом числе атомов в молекуле:
Работа газа при адиабатном расширении меньше, чем при изотермическом расширении, т.к. при адиабатном процессе происходит охлаждение газа.
Процессы изменения состояния газа, в результате которых газ возвращается в исходное состояние, называются круговыми или циклическими (рисунок 19).
Если за цикл совершается положительная работа А > 0 (цикл протекает по часовой стрелке), то цикл называется прямым. Если за цикл совершается отрицательная работа А < 0 (цикл протекает против часовой стрелки), то цикл называется обратным. Прямой цикл используется в тепловых двигателях, совершающих работу за счет получения теплоты извне. Обратный цикл используется в холодильных машинах, в которых за счет работы внешних сил теплота переносится к телу с более высокой температурой. Термодинамический процесс называется обратимым, если он может происходить как в прямом, так и в обратном направлении. В результате кругового процесса система возвращается в исходное состояние и полное изменение внутренней энергии газа Поэтому первое начало термодинамики для кругового процесса:
Термодинамический КПД для кругового процесса:
Контрольные вопросы: 1. Расскажите о работе совершаемой газом при постоянном давлении. 2. Как вычислить работу газа при изменяющемся давлении? 3. Что такое круговой процесс? Как вычислить работу газа при круговом процессе? 4. Как вычислить КПД кругового процесса? 5. Что такое обратимый термодинамический процесс?
|
||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-09; просмотров: 403; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.189.2.122 (0.006 с.) |
 3. PVg = const, P1 T2 = P2 T1,
3. PVg = const, P1 T2 = P2 T1,  4. P = nkT, V1 T2 = V2 T1,
PV =
4. P = nkT, V1 T2 = V2 T1,
PV =  , PVg = const, PV = const
2.
, PVg = const, PV = const
2. 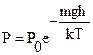 , PV = const,
V1 T2 = V2 T1
3.
, PV = const,
V1 T2 = V2 T1
3. 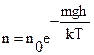 , V1 T2 = V2 T1, PVg = const
4.
, V1 T2 = V2 T1, PVg = const
4.  , PVg = const,
V1 T2 = V2 T1
, PVg = const,
V1 T2 = V2 T1
 1 3
2 4
1 3
2 4
 (рисунок 17). Тогда работа, совершаемая газом:
(рисунок 17). Тогда работа, совершаемая газом:  ,
,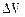 – изменение объема,
– изменение объема,  - площадь сечения цилиндра.
- площадь сечения цилиндра.
 =
= 
 . Применяя уравнение Клапейрона - Менделеева для каждого из состояний идеального газа при Т
. Применяя уравнение Клапейрона - Менделеева для каждого из состояний идеального газа при Т  и Т
и Т  , можно записать, что работа газа:
, можно записать, что работа газа:  , где
, где 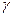 - количество молей газа.
- количество молей газа. одноатомного идеального газа:
одноатомного идеального газа:  , тогда:
, тогда: 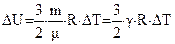 .
.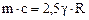

 , а
, а  , где
, где 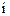 – число степеней свободы молекулы.
– число степеней свободы молекулы.  - коэффициент Пуассона
- коэффициент Пуассона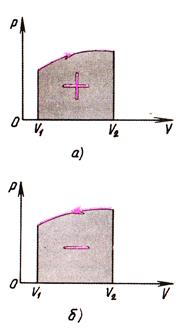
 Работа, совершаемая газом в адиабатном процессе:
Работа, совершаемая газом в адиабатном процессе:  = gСVDТ, или
= gСVDТ, или 
 Если процесс не изобарный, то можно взять малые изменения объема
Если процесс не изобарный, то можно взять малые изменения объема  дает полную работу расширяющегося газа (рисунок 18).
дает полную работу расширяющегося газа (рисунок 18).
 На диаграмме цикл изображается замкнутой кривой ВСДЕВ. Цикл можно разбить на процесс расширени я газа ВСД и процесс сжатия газа ДЕВ. Работа расширения - положительная, а работа сжатия - отрицательная. Следовательно, работа, совершаемая газом за цикл, определяется площадью, охватываемой замкнутой кривой ВСДЕВ.
На диаграмме цикл изображается замкнутой кривой ВСДЕВ. Цикл можно разбить на процесс расширени я газа ВСД и процесс сжатия газа ДЕВ. Работа расширения - положительная, а работа сжатия - отрицательная. Следовательно, работа, совершаемая газом за цикл, определяется площадью, охватываемой замкнутой кривой ВСДЕВ. равно нулю.
равно нулю. , т.е. работа, совершаемая за цикл, равна количеству полученной извне теплоты. Этим соотношением запрещается вечный двигатель первого рода.
, т.е. работа, совершаемая за цикл, равна количеству полученной извне теплоты. Этим соотношением запрещается вечный двигатель первого рода. , где
, где - количество теплоты, полученное системой;
- количество теплоты, полученное системой; - количество теплоты, отданное системой.
- количество теплоты, отданное системой.


