
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы исследования биомембран: метод дифракции рентгеновского излучения. Люминесцентные методы исследования мембран. Ямр и эпр исследования.
МЕТОД ДИФРАКЦИИ РЕНТГЕНОВСКОГО ИЗЛУЧЕНИЯ. Использование рентгеновского излучения для анализа мембранных структур обусловлено тем обстоятельством, что одним из главных условий проявления дифракции является сопоставимость размеров объекта, на который направляется излучение, и длины волны этого излучения. Для анализа объектов нанометрового диапазона необходимо рентгеновское излучение (диапазон длин его волн от 10-5 до 80 нм). Чтобы понять принцип использования рентгеновского излучения для анализа структуры вещества, рассмотрим кристаллическую структуру, на два соседних атома которой падают параллельные лучи (рис.5), которые отражаются от соседних атомов кристаллической решетки, а затем интерферируют, собираясь в одну точку на некотором экране. Вводя значение межатомного расстояния d, угла скольжения Условием того, что в некоторой точке экрана две волны будут усиливать друг друга, является равенство этой разности хода целому числу длин волн: Наблюдая картину дифракции на экране, можно установить, под каким углом максимум первого порядка (n=1). Зная длину волны, можно найти важнейший параметр структуры исследуемого вещества – межатомное расстояние При анализе структуры мембран реальная исследовательская методика намного сложнее, но основана на том, что изложено выше. С помощью рентгеноструктурного анализа были подтверждены бислойное расположение фосфолипидов и присутствие в мембранах белков, вычислены важные структурные параметры мембраны. ЛЮМИНЕСЦЕНТНЫЕ МЕТОДЫ ИССЛЕДОВАНИЯ МЕМБРАН. Эти методы связаны с использованием флуоресцентных меток флюоресцирующих молекулярных групп, тем или иным способом связываемых с исследуемыми молекулами и позволяющих визуализировать многие процессы. Флуоресцентный анализ дает возможность исследовать подвижность фосфолипидных молекул в мембране, оценить вязкость липидной фазы мембраны (так называемую микровязкость мембран). Микровязкость мембраны можно оценить по изменениям спектров флюоресценции, а также по степени поляризации флюоресцентного излучения при освещении мембраны поляризованным светом. Связь степени поляризации и микровязкости мембраны выражается формулой Перрена и Яблонского, из которой следует, что чем менее поляризовано люминесцентное излучение (возникшее в ответ на внешнее облучение мембраны), тем более подвижны молекулы в исследуемом участке и тем меньше там микровязкость. Наоборот, чем выше степень поляризации люминесцентного света, тем меньше подвижность и больше микровязкость.
ЯМР и ЭПР исследования. Наиболее полные сведения об агрегатном состоянии липидных бислоев дают методы радиоспектроскопии ЭПР и ЯМР. Электронный парамагнитный резонанс – это явление резкого возрастания поглощения энергии электромагнитной волны системой парамагнитных частиц (электронов с некомпенсированными спинами), помещенных во внешнее магнитное поле при резонансной частоте волны. Использование ЭПР заключается в исследовании спектров ЭПР. Спектром ЭПР называется зависимость мощности поглощения электромагнитной волны от величины магнитной индукции внешнего поля. Чем сильнее взаимодействие между атомами и молекулами образца, тем спектры ЭПР шире. Чем слабее взаимодействие между частицами (подвижность молекул больше), тем уже спектр ЭПР. По ширине спектров ЭПР можно судить о подвижности молекул веществ. Так как молекулы фосфолипидов диамагнитные, для ЭПР-исследований биомембран используются спин-зонды и спин-метки – молекулы или молекулярные группы с неспаренными электронами. Парамагнитные спин-зонды вводятся в липидную мембрану, спектры поглощения спин-зондами электромагнитной волны дают информацию о свойствах липидного окружения, в частности о подвижности липидных молекул в мембране. Этот метод обладает существенным недостатком – внесение в биологический объект чужеродных молекул-зондов может изменять структуру объекта. От этого недостатка свободен метод ЯМР. Ядерный магнитный резонанс – это явление резкого возрастания поглощения энергии электромагнитной волны системой атомных ядер, обладающих магнитным моментом, помещенных во внешнее магнитное поле при резонансной частоте волны. Как и в случае ЭПР, спектры ЯМР тем шире, чем больше вязкость и меньше молекулярная подвижность исследуемого объекта.
Потенциал покоя. Экспериментально установлено, что между поверхностями биомембраны невозбужденной клетки существует разность потенциалов, часто называемая для краткости потенциалом покоя: Э. Бернштейн по праву считается основателем мембранной теории биопотенциалов (первая его статья была опубликована в 1902 г.). Разберем, что такое потенциал покоя и как он возникает. Представим себе, что внутри клетки имеется много свободных ионов какого-нибудь элемента (рис. XII.1.) и клеточная мембрана пропускает только эти ионы. Естественно, они начнут двигаться наружу и вместе с ними наружу будет выноситься положительный заряд. В результате между внутренней и наружной поверхностями мембраны возникает разность потенциалов (рис. XII.2.). Потенциал наружной поверхности будет больше, чем потенциал внутренней (при этом разность концентраций ионов внутри и снаружи будет к этому моменту еще довольно значительной). Эта разность потенциалов будет тормозить движение наружу новых положительных ионов и увеличивать их поток внутри клетки. В конце концов эти потоки станут равными по величине (установится динамическое равновесие), а суммарный поток будет равным нулю. Установившаяся при этом между поверхностями биомембраны разность электрических потенциалов и есть потенциал покоя. Его величину можно вычислить из условия равенства электрохимических потенциалов внутри и снаружи клетки
После несложных преобразований получим: Разность
Однако даже после выхода в 1912 г. в свет фундаментальной книги Э. Бернштейна «Электробиология» мембранная теория не вызывала особого доверия ученых, так как не было ее прямых подтверждений. Наиболее интенсивным нападкам подвергалось само существование мембраны (ее увидели при использовании электронной микроскопии лишь во второй половине XX века). Еще одной экспериментальной проблемой было определение ионного состава внутренней среды. Ученые пытались использовать для определения этого состава самые разные методы, но все полученные данные были лишь приблизительными: клетки слишком малы, а между ними всегда имеются межклеточное вещество и жидкость. Кроме того, сторонникам мембранной теории надо было показать не просто присутствие калия внутри клеток, а присутствие именно свободных, несвязанных ионов калия. Эта проблема была решена с разработкой новых методов измерения и подбором подходящего объекта. В 1936 г. английский специалист по головоногим моллюскам Дж.Юнг обнаружил у кальмаров нервное волокно, диаметр которого доходит до 1 мм, т.е. гигантское по клеточным масштабам, хотя сам моллюск вовсе не был гигантом. Такое волокно, выделенное из организма и помещенное в морскую воду, не погибало. Появилась живая клетка, в которую можно было проникнуть и с которой можно было работать. В 1939 г. английский ученый А.Ходжкин и его ученик А. Хаксли впервые измерили разность потенциалов на мембране животной клетки. Удалось также доказать, что внутри этого волокна действительно много ионов калия и эти ионы представляют собой «ионный газ», т.е могут участвовать в создании мембранного потенциала. Расчетное значение потенциала покоя неплохо совпадало с непосредственно измеренным (около 60 мВ). Распространить эти данные с уникальной клетки – гигантского аксона – на обычные клетки стало возможным в 1946 г., когда американские ученые Джерард и Линг разработали новую методику – методику микроэлектродов. Микроэлектрод – это вытянутая из нагретой стеклянной трубочки тоненькая пипетка с диаметром кончика менее 1 мкм (тысячной доли миллиметра), заполненная раствором электролита. Стекло играет роль изолятора, а электролит – проводника. Такой электрод можно ввести в любую клетку, практически ее не повреждая.
Новая техника эксперимента быстро получила широкое распространение в самых разных исследованиях и за несколько лет буквально завоевала мир. Вскоре были получены достаточно полные данные о величие потенциала покоя различных клеток (в том числе и эритроцитов, клеток кожи, печени и др.). Использование ионочувствительных электродов в сочетании с методом меченных атомов и другими методами позволило определить и ионный состав внутриклеточного содержимого. Оказалось, что, как и предсказывала мембранная теория, внутри клеток концентрация ионов калия в 30-40 раз выше, чем в наружной среде. В 1961 г. А. Ходжкин, Бейкер и Шоу поставили интересный опыт: они брали гигантский аксон кальмара, выдавливали из него протоплазму и получали пустую трубку из одной мембраны. Появилась возможность работать на мембране нервного волокна, произвольно меняя концентрацию вещества и внутри, и снаружи. Оказалось, что при заполнении аксона раствором, содержащим такую же концентрацию калия, как и в протоплазме, в аксоне возникал потенциал покоя Еще один важный момент, который следует обсудить: когда методы измерения потенциала покоя достигли высокой точности, обнаружилось, что на самом деле измеряемый потенциал покоя всегда ниже, чем теоретически вычисленный по формуле Нернста. Ясно, что существует какой-то возмущающий фактор, не учтенный теорией Бернштейна.
Найти причину расхождения эксперимента и теории помог опять- таки кальмар. Работая с гигантским аксоном, А. Ходжкин и Б. Катц установили, что потенциал покоя, измеряемый в опыте, оказывается ближе всего к теоретическому в одном особом случае: если из наружной среды исключен натрий. Однако если, как считал Бернштейн, мембрана проницаема только для калия, то натрий вообще не должен влиять на потенциал покоя. Что будет, если, посягнув на основу основ мембранной теории, предположить, что натрий тоже проходит через мембрану? Легко понять, что тогда ионы натрия, которых снаружи клетки гораздо больше, чем внутри, будут идти внутрь, создавая нернстовский потенциал, Противоположный по знаку тому, который создается калием, и, значит, будут снижать потенциал покоя. Ходжкин и Катц проверяют свое предположение экспериментально, меняя концентрацию натрия во внешней среде и сравнивая значения потенциала покоя с теоретическими. Оказалось, что для совпадения экспериментальных данных с расчетными приходится принять, что сопротивление, которое «преодолевают» ионы натрия, в 25 раз больше, чем для калия. Это означает, что проницаемость мембраны для ионов натрия хотя и в 25 раз меньше, чем для калия, но все же не равна нулю. Вскоре предположение, что ионы натрия могут проходить через мембрану гигантского аксона, было прямо доказано в опытах с радиоактивным изотопом натрия. В ходе этих работ ученые открыли особое вещество тетродотоксин (яд рыбы-шара), блокирующее движение натрия через мембрану. Теперь удалось показать, что если добавить в морскую воду, окружающую гигантский аксон, тетродотоксин, натрий перестает идти через мембрану, потенциал покоя начинает нарастать и достигает значения, в точности равного тому, которое предсказывается формулой Нернста. Роль натрия в формировании потенциала покоя была полностью доказана. Учтя влияние на величину потенциала покоя и ионов натрия и хлора, в 1949г. Гольдман, Ходжкин и Катц вывели для величины потенциала покоя уравнение (оно называется уравнением Гольдмана):
Оно было получено из того предположения, что в невозбужденном состоянии через поверхность мембраны проходят потоки ионов калия, натрия и хлора, алгебраическая сумма которых должна быть равна нулю: Очевидно, если в этом уравнении вновь пренебречь проницаемостью мембраны для ионов натрия и хлора по сравнению с проницаемостью для иона калия, оно автоматически станет уравнением Нернста. Потенциал действия. Еще Э. Бернштейн изучал процесс возбуждения клеточной мембраны и предсказал измерение ее проницаемости для различных ионов. Однако завершить изучение этого вопроса он не успел. Примерно в 1939 г. Коул и Кертис (США) и Ходжкин и Хаксли (Великобритания) измеряли потенциалы невозбужденной и возбужденной клеток на гигантском аксоне кальмара: оказалось, что в состоянии покоя разность потенциалов была примерно равна 80 мВ (отрицательная), а максимальная разность потенциалов при возбуждении + 40мВ (положительная). Далее Ходжкин и Хаксли сформулировали гипотезу о том, что при возбуждении меняется характер проницаемости мембраны для разного типа ионов: из проницаемой главным образом для калия она превращается в проницаемую для натрия и, следовательно, поток ионов натрия внутрь клетки увеличивается.
Разносность потенциалов между поверхностями мембраны поднимается до нуля, а затем становится положительной – наступает деполяризация мембраны. Далее процесс развивается в обратном направлении: поток ионов натрия внутрь клетки постепенно уменьшается и возвращается к «невозбужденному» значению; разность потенциалов также возвращается к значению На рис.XII.4. изображены конденсатор емкости С, два переменных резистора, которым соответствуют проводимости Согласно этой модели полный ток, протекающий через мембрану, равен сумме 4 слагаемых: где Iк – ток ионов калия; INa –ток ионов натрия; I’ – ток ионов хлора и остальных ионов, иногда называемый током утечки; Рассмотрим сначала ток калия. Ионы калия идут через мембрану всегда, причем в обе стороны. Когда потенциал на мембране ( Аналогичной формулой определяется и сила натриевого тока:
Где Зависимости проводимостей gк и gNa от времени при некотором неизменном мембранном потенциале изучали в опытах Ходжкина – Хаксли (опыты с фиксацией напряжения). За очень короткое время на мембране устанавливали фиксированную разность потенциалов и долго поддерживали ее. Это позволяло, в частности, избавиться от емкостных токов: если
Рис. 5. позволяет, во-первых, сделать важный вывод о том, что проводимость gNa зависит от времени – ведь при постоянной разности потенциалов ток Во-вторых, оценивая по формуле Нернста равновесный натриевый потенциал, получим около + 40 мВ. Тогда в случае 3, когда фиксированное значение потенциала было равно – 30 мВ, разность В – третьих, можно сделать вывод о том, что проводимость Эксперименты подтвердили также то, что первая фаза потенциала действия связана с потоком ионов натрия внутрь клетки, а вторая – с потоком ионов калия наружу В дальнейшем Ходжкин и Хаксли предложили математическую модель, которая описывала изменения проводимостей, а следовательно, и токов ионов натрия и калия через мембрану в процессе возбуждения. Один из основных постулатов этой модели: в мембране существуют отдельные каналы для переноса ионов натрия и калия. Основные свойства каналов: - селективность- способность пропускать в большинстве случаев ионы только одного типа; - независимость работы отдельных каналов – ток через тот или иной канал не зависит от того, протекает ли ток через другой канал или нет; - дискретный характер проводимости ионных каналов: в первом приближении можно утверждать, что ионный канал может находиться в двух состояниях – открытом или закрытом, переходы между этими состояниями происходят в случайные моменты времени и подчиняются статистическим закономерностям. Несмотря на то, что сила тока через каждый одиночный канал меняется скачком, зависимость суммарного тока от времени есть плавная кривая, это обусловлено огромным числом одновременно функционирующих каналов (например, подсчитано, что на аксоне кальмара длиной 1 см и диаметром 1 мм примерно 1010 каналов). На рис. 8. представлена связь между токами в одиночных натриевых каналах и суммарным натриевым током; - зависимость параметров канала от мембранного потенциала. Это проявляется в том, что после начала деполяризации мембраны соответствующие токи начинают изменяться с той или иной кинетикой. Исходя из гипотезы об ионных каналах, этот процесс происходит следующим образом. Ионоселективный канал имеет так называемый сенсор – элемент конструкции, чувствительной к действию электрического поля. При изменении мембранного потенциала меняется величина действующей на него силы, в результате эта часть ионного канала перемещается и меняет вероятность открывания или закрывания ворот – своеобразных заслонок, действующих по закону «все или ничего». Примерно в 1952 г. Хаксли, исходя из разработанной математической модели, рассчитал, как меняется мембранная разность потенциалов со временем. Результаты этого расчета с большой точностью совпали с потенциалом действия, зарегистрированным экспериментально.
Модель Ходжкина – Хаксли довольно хорошо воспроизводила такие явления, как рефрактерность, порог возбуждения и др., позволяя теоретически объяснить наблюдаемые в эксперименте свойства потенциала действия: - пороговое значение деполяризующего потенциала; - закон «все или ничего»: если деполяризующий потенциал больше порогового, то развивается потенциал действия, амплитуда которого не зависит от амплитуды возбуждающего импульса; если амплитуда деполяризующего потенциала меньше пороговой, то потенциала действия не возникает; - наличие периода рефрактерности (невозбудимости) мембраны во время развития потенциала действия и остаточных явлений после снятия возбуждения. Как показано выше, потенциал покоя создается в основном в результате разности концентраций ионов калия внутри и снаружи клетки. Однако после нескольких потенциалов действия, сопровождающихся потоком ионов натрия внутрь на первой фазе и ионов калия наружу на второй, разности концентраций этих ионов внутри и снаружи клетки должны меняться. В связи с этим, например, в результате уменьшения помещенного под знаком логарифма в формуле Нернста отношения внутренней и наружной концентраций ионов калия величина потенциала покоя должна постепенно приближаться к нулю. Однако этот не происходит. Видимо, существует какой-то механизм, поддерживающий разность концентраций. С помощью такого механизма ионы калия должны закачиваться внутрь клетки (где их концентрация и так больше), а ионы натрия – откачиваться наружу, где их концентрация также больше, чем внутри. Что же это за механизм? Выше уже шла речь о том, что в клеточную мембрану встроены различные белковые молекулы. Оказывается, что некоторые из них играют роль своеобразных насосов, закачивающих ионы калия внутрь, а ионы натрия – наружу (пример активного ионного транспорта). Известно также, за счет энергии какого источника происходит работа насосов. В случае калий – натриевого насоса опыты с радиоактивными изотопами показали, что для закачивания внутрь клетки 2 ионов калия и выкачивания наружу 3 ионов натрия (один цикл работы насоса) достаточно энергии распада одной молекулы АТФ (рис.9). Это обнаружил еще в 1957г. С.Скоу. Оказалось, что работа ионных насосов управляется концентрацией ионов внутри и вне клетки. Работа насоса ускоряется избытком ионов калия снаружи клетки и избытком ионов натрия внутри. Важнейшую роль в осуществлении различных клеточных функций играет ион кальция. Так, для мышечного сокращения необходимо много ионов кальция и его необходимо доставлять к каждой из белковых фибрилл, пронизывающих тело клетки, а затем также быстро убирать от фибрилл, чтобы мышца могла расслабиться. Если бы каждый ион кальция поступал и удалялся через наружную мембрану клетки, то его быстрое перемещение было бы невозможным. Внутри мышечных клеток имеется разветвленная система полостей и трубочек, образованных специальной внутренней мембранной, в которых хранится кальций, туда же он убирается после расслабления мышцы. Вся эта мембрана «покрыта» кальциевыми насосами. Источником активного транспорта кальция является также гидролиз АТФ (рис. XII.10). Рассмотрим распространение потенциала действия по нервному волокну. Если в каком – нибудь участке возбудимой мембраны сформировался потенциал действия, мембрана деполяризована, возбуждение распространяется на другие участки мембраны. Рассмотрим распространения на приеме передачи нервного импульса по аксону. В аксоплазме и в окружающем растворе возникают локальные токи между участками поверхности мембраны с большим потенциалом (положительно заряженными) и участками с меньшим потенциалом (отрицательно заряженными). Локальные токи образуются и внутри сксона, и на наружной его поверхности. Локальные электрические токи приводят к повышению потенциала внутренней поверхности невозбужденного участка мембраны
Большую скорость распространения нервного импульса по аксону кальмара обеспечивает его гигантский по сравнению с аксоном позвоночных диаметр. У позвоночных большая скорость передачи возбуждения в нервных волокнах обеспечивается другими способами. Аксоны позвоночных снабжены миелиновой оболочкой, которая увеличивает сопротивление мембраны. Возбуждение по миелинизированному волокну распространяется сальтаторно (скачкообразно) от одного перехвата Рантье (участка, свободного от миелиновой оболочки) до другого. Нервные импульсы проводятся по аксонам в какой – то степени аналогично тому, как передаются электрические сигналы по кабельно – релейной линии. Электрический импульс передается без затухания из-за его усиления на промежуточных релейных станциях, роль которых в аксонах выполняют участки возбудимой мембраны, где генерируются потенциалы действия. Свойства жидкостей Вещество в жидком состоянии сохраняет свой объем, но принимает форму сосуда. Если сила тяжести капли уравновешивается силой Архимеда, на каплю действуют только молекулярные силы, то она принимает форму шара. В состоянии невесомости жидкость принимает шарообразную форму и вне сосуда, что было проверено космонавтами. Сохранение объема у жидкости доказывает, что между ее молекулами действуют силы притяжения. Следовательно, расстояния между молекулами жидкости должны быть меньше радиуса молекулярного действия. Если вокруг какой-либо молекулы жидкости описать сферу молекулярного действия, то внутри этой сферы окажутся центры многих других молекул, которые будут взаимодействовать с этой молекулой. Эти силы взаимодействия удерживают молекулу жидкости около ее временного положения равновесия примерно в течение 10-12 – 10-10 сек., после чего она перескакивает в новое временное положение равновесия приблизительно на расстояние своего диаметра. Молекулы жидкости между переходами совершают колебательное движение около временного положения равновесия. Время между переходами молекулы из одного положения в другое называется временем оседлой жизни. Это время зависит от вида жидкости и от температуры. При нагревании жидкости среднее время оседлой жизни молекул уменьшается. Жидкость обладает текучестью, вызванной тем, что время действия внешней силы обычно во много раз больше времени релаксации, поэтому жидкость течет и принимает форму сосуда, в котором она находится. В небольшом объеме жидкости наблюдается упорядоченное расположение ее молекул, а в большом объеме оно оказывается хаотическим. В этом смысле говорят, что в жидкости существует ближний порядок в расположении молекул и отсутствует дальний порядок. Такое строение жидкости называют квазикристаллическим (кристаллоподобным). В некоторых жидкостях с удлиненной формой молекул возможна единообразная ориентация их по всему объему. Такие жидкости называются жидкими кристаллами, а свойства их отличаются от обычных жидкостей. При достаточно сильном нагревании время оседлой жизни становится очень маленьким и ближний порядок в жидкости практически исчезает. Жидкость может обнаруживать механические свойства, присущие твердому телу. Если время действия силы на жидкость мало, то жидкость проявляет упругие свойства. Например, при резком ударе палкой о поверхность воды палка может вылететь из руки или сломаться; камень можно бросить так, что он при ударе о поверхность воды отскакивает от нее, и лишь совершив несколько скачков, тонет в воде. Если же время воздействия на жидкость велико, то вместо упругости проявляется текучесть жидкости. Например, рука легко проникает внутрь воды. При кратковременном действии силы на струю жидкости последняя обнаруживает хрупкость. Сжимаемость жидкости больше, чем у этих же веществ в твердом состоянии. Например, при увеличении давления на 1 атм объем воды уменьшается на 50 миллионных долей. Разрывы внутри жидкости, в которой нет посторонних веществ, например воздуха, могут получаться только при интенсивном воздействии на жидкость, например при распространении в жидкости ультразвуковых волн. Такого рода пустоты внутри жидкости долго существовать не могут и резко захлопываются, т.е. исчезают. Это явление называют кавитацией (от греческого «кавитас» -полость).
|
|||||||||
|
Последнее изменение этой страницы: 2017-02-17; просмотров: 736; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.221.85.33 (0.037 с.) |
 , получим, что разность хода лучей
, получим, что разность хода лучей  .
. .
. наблюдается, например,
наблюдается, например, .
. ÷
÷ 
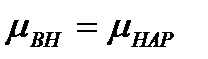
 . Используя для нахождения электрохимического потенциала формулу (XI.4), получим:
. Используя для нахождения электрохимического потенциала формулу (XI.4), получим: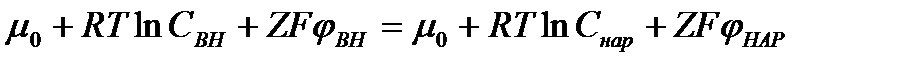

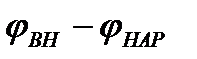 и есть обсуждаемый нами потенциал покоя:
и есть обсуждаемый нами потенциал покоя:
 ÷
÷  . Если концентрация калия внутри и снаружи волокна была одинаковой, то потенциал покоя в полном соответствии с формулой Нернста не возникал. Если внутрь волокна накачивали морскую воду, а в наружную среду – раствор с высокой концентрацией калия, знак потенциала покоя менялся, а его величина соответствовала формуле Нернста. Это стало важным подтверждением теории Бернштейна.
. Если концентрация калия внутри и снаружи волокна была одинаковой, то потенциал покоя в полном соответствии с формулой Нернста не возникал. Если внутрь волокна накачивали морскую воду, а в наружную среду – раствор с высокой концентрацией калия, знак потенциала покоя менялся, а его величина соответствовала формуле Нернста. Это стало важным подтверждением теории Бернштейна.

 . Такой импульс (рис..3) называют потенциалом действия. Ходжкин и Хаксли построили также электрическую модель процесса возбуждения, согласно этой модели мембрана представляется следующей схемой (рис. XII.4).
. Такой импульс (рис..3) называют потенциалом действия. Ходжкин и Хаксли построили также электрическую модель процесса возбуждения, согласно этой модели мембрана представляется следующей схемой (рис. XII.4). , 3 источника ЭДС, имитирующих равновесные, рассчитанные по формуле Нернста разности потенциалов для ионов калия, натрия и хлора, а также еще одно сопротивление (суммарное сопротивление мембраны для ионов хлора и ряда других) – соответствующая проводимость обозначена на схеме.
, 3 источника ЭДС, имитирующих равновесные, рассчитанные по формуле Нернста разности потенциалов для ионов калия, натрия и хлора, а также еще одно сопротивление (суммарное сопротивление мембраны для ионов хлора и ряда других) – соответствующая проводимость обозначена на схеме.
 - емкостный ток (ток перезарядки мембраны), протекающий по той ветви цепи, куда включен конденсатор.
- емкостный ток (ток перезарядки мембраны), протекающий по той ветви цепи, куда включен конденсатор. ) равен нернстовскому потенциалу, который иначе называют потенциалом равновесия для калия
) равен нернстовскому потенциалу, который иначе называют потенциалом равновесия для калия  , то сохраняется динамическое равновесие, т.е. калиевый ток
, то сохраняется динамическое равновесие, т.е. калиевый ток 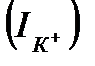 равен нулю. Если мембранный потенциал отклоняется от равновесного, то возникает калиевый ток, величину которого можно определить по закону Ома:
равен нулю. Если мембранный потенциал отклоняется от равновесного, то возникает калиевый ток, величину которого можно определить по закону Ома: 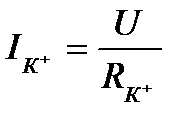 . Заменив
. Заменив 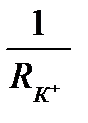 на калиевую проводимость
на калиевую проводимость  - на величину отклонения мембранного потенциала от равновесного, т.е.
- на величину отклонения мембранного потенциала от равновесного, т.е. 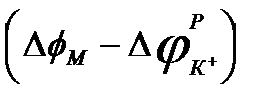 , получаем:
, получаем: 
 ,
, - равновесный натриевый потенциал, т.е. нернстовский потенциал для натрия, который равен примерно +40 мВ (он примерно равен овершуту – превышению нуля значением
- равновесный натриевый потенциал, т.е. нернстовский потенциал для натрия, который равен примерно +40 мВ (он примерно равен овершуту – превышению нуля значением  в точке максимума; Как видно, силы токов зависят от мембранного потенциала довольно сложным образом:
в точке максимума; Как видно, силы токов зависят от мембранного потенциала довольно сложным образом: 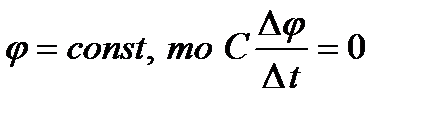 . Чтобы отдельно зарегистрировать токи ионов калия и натрия, использовали блокаторы. При введении тетраэтиламмония (блокатор калия) фиксировали зависимость тока ионов натрия от времени, при введении тетродотоксина – зависимость тока ионов калия от времени. Зависимость
. Чтобы отдельно зарегистрировать токи ионов калия и натрия, использовали блокаторы. При введении тетраэтиламмония (блокатор калия) фиксировали зависимость тока ионов натрия от времени, при введении тетродотоксина – зависимость тока ионов калия от времени. Зависимость  графически выражалась так, как показано на рис. 5. Графики1, 2 и 3 соответствовали различным значениям фиксированного потенциала. Для конкретности положим
графически выражалась так, как показано на рис. 5. Графики1, 2 и 3 соответствовали различным значениям фиксированного потенциала. Для конкретности положим  .
. менялся во времени, а это возможно лишь при условии, что проводимость
менялся во времени, а это возможно лишь при условии, что проводимость  являлась функцией времени:
являлась функцией времени:  .
. наибольшая (+ 70 мВ) и по абсолютной величине сила тока в этом случае будет также наибольшей. Это вполне согласуется с моделью Ходжкина – Хаксли.
наибольшая (+ 70 мВ) и по абсолютной величине сила тока в этом случае будет также наибольшей. Это вполне согласуется с моделью Ходжкина – Хаксли. и к понижению наружного потенциала невозбужденного участка мембраны
и к понижению наружного потенциала невозбужденного участка мембраны  , оказавшегося по соседству с возбужденной зоной. Таким образом, отрицательный потенциал покоя
, оказавшегося по соседству с возбужденной зоной. Таким образом, отрицательный потенциал покоя 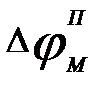 уменьшается по абсолютной величине, т.е. повышается выше порогового значения. Поэтому под действием изменения мембранного потенциала открываются натриевые каналы и дальнейшее повышение происходит уже в результате потока ионов через мембрану. Происходит деполяризация мембраны, развивается потенциал действия. Затем возбуждение передается дальше на первоначально невозбужденные участки мембраны (рис.11).
уменьшается по абсолютной величине, т.е. повышается выше порогового значения. Поэтому под действием изменения мембранного потенциала открываются натриевые каналы и дальнейшее повышение происходит уже в результате потока ионов через мембрану. Происходит деполяризация мембраны, развивается потенциал действия. Затем возбуждение передается дальше на первоначально невозбужденные участки мембраны (рис.11).


