
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Организм как открытая система
Начальное развитие термодинамики стимулировалось потребностями промышленного производства. На этом этапе (XIX в.) ее основные достижения заключались в формулировке законов, разработке теории циклов и термодинамических потенциалов применительно к идеализированным процессам: равновесным и обратимым. Термодинамика биологических систем в этот период не развивалась. Одним ярким исключением из этого была работа Майера, который по цвету венозной крови матросов, работающих в условиях тропического климата, сформулировал, по существу, приложимость закона сохранения энергии в термодинамике (первого начала термодинамики) к живым системам. Первый закон термодинамики как закон сохранения энергии настолько очевиден, что его применения к биологическим системам здесь не рассматриваются, тем более что в курсе нормальной физиологии изучаются такие темы, как «Обмен веществ и энергии. Питание. Терморегуляция», а в § 22.5 анализируется теплообмен человека с окружающей средой посредством теплового излучения. Более существенно рассмотреть некоторые вопросы, связанные со вторым началом термодинамики и энтропией применительно к биологическим системам. Биологические объекты являются открытыми термодинамическими системами. Они обмениваются с окружающей средой энергией и веществом. Вообще говоря, живой организм — развивающаяся система, которая не находится в стационарном состоянии. Однако обычно в каком-либо не слишком большом интервале времени принимают состояние биологической системы за стационарное. Рассмотрим в этом предположении некоторые вопросы. Для организма — стационарной системы — можно записать dS = 0, S = const, dSi > 0, dSe < 0. Это означает, что большая энтропия, должна быть в продуктах выделения, а не в продуктах питания. Энтропия системы организм — окружающая среда возрастает как у изолированной системы, однако энтропия организма при этом сохраняется постоянной. Энтропия есть мера неупорядоченности системы (см. § 10.2), поэтому можно заключить, что упорядоченность организма сохраняется ценой уменьшения упорядоченности окружающей среды. При некоторых патологических состояниях энтропия биологической системы может возрастать (dS > 0), это связано с отсутствием стационарности, увеличением неупорядоченности; так, например, при раковых заболеваниях происходит хаотическое, неупорядоченное разрастание клеток.
Формулу (10.21) можно преобразовать к виду
или для стационарного состояния (S = const, dS/dt = 0)
Из (10.22) видно, что при обычном состоянии организма скорость изменения энтропии за счет внутренних процессов равна скорости изменения отрицательной энтропии за счет обмена веществом и энергией с окружающей средой. Поскольку, согласно принципу Пригожина, производная " dSi/dt > 0, причем минимальна. Отсюда можно сделать вывод, что скорость изменения энтропии окружающей среды при сохранении стационарного состояния организма также минимальна. Основа функционирования живых систем (клетки, органы, организм) — это поддержание стационарного состояния при условии протекания диффузионных процессов, биохимических реакций, осмотических явлений и т. п. При изменении внешних условий процессы в организме развиваются так, что его состояние не будет прежним стационарным состоянием. Можно указать некоторый термодинамический критерий приспособления организмов и биологических структур к изменениям внешних условий (адаптации). Если внешние условия изменяются (возрастает или уменьшается температура, изменяется влажность, состав окружающего воздуха и т. д.), но при этом организм (клетки) способен поддерживать стационарное состояние, то организм - адаптируется (приспосабливается) к этим изменениям и существует. Если организм при изменении внешних условий не способен сохранить стационарное состояние, выходит из этого состояния, то это приводит к его гибели. Организм в этом случае не смог адаптироваться, т. е. не смог сравнительно быстро оказаться в стационарном состоянии, соответствующем изменившимся условиям
Термометрия и калориметрия Точные измерения температур являются неотъемлемой частью научно-исследовательских и технических работ, а также медицинской диагностики и биологии. Диапазон известных температур очень широк. Самая низкая температура, полученная к настоящему времени, около 2 • 10-5 К. Верхний предел достижимых температур ничем не ограничен. Наибольшая температура достигнута в земных условиях при взрыве водородной бомбы и составляет примерно 108 К. В недрах звезд, по спектроскопическим данным, температура может достигать 109 К и более.
Температурный интервал окружающей среды, в которой могут длительно или кратковременно находиться биологические системы, сохраняя способность к функционированию, значительно уже. И совсем невелик (приблизительно от 0 до 90 °С) диапазон температур самих живых организмов в состоянии их активной жизнедеятельности. Методы получения и измерения температур в широком диапазоне весьма различны. Отдел прикладной физики, в которой изучаются методы измерения температуры и связанные с этим вопросы, называют термометрией. Как известно, температура не может быть измерена непосредственно. Для ее определения нужно установить температурную шкалу: выбрать термометрическое вещество и физическое свойство, зависящее от температуры (термометрическое свойство), условиться о начальной точке отсчета и единице температуры. Для этого обычно выбирают две основные температуры (реперные точки), соответствующие температурам фазовых переходов, например плавлению льда и кипению воды при определенных внешних условиях. Участок шкалы между этими точками называют основным интервалом. За начало отсчета принимают одну из реперных точек (например, 0 °С — температура плавления, или таяния льда), за единицу температуры — долю основного интервала. Так, 1 °С составляет 0,01 долю основного интервала. Температурные шкалы различаются по термометрическому свойству или веществу. Можно построить огромное количество шкал, значительно отличающихся одна от другой, так как ни одно из свойств не зависит от температуры строго линейно и, кроме того, определяется природой вещества. Принципиальным недостатком всех эмпирических шкал является их зависимость от свойств термометрического вещества. Независимая от свойств и вещества шкала построена на основе второго начала термодинамики и названа термодинамической шкалой температур. За реперную точку ее принята температура тройной точки воды 273,16 К. Определяется эта шкала с помощью цикла Карно. Измерив количества теплоты Qo и Qs в изотермических процессах этого цикла соответственно при температуре Т0 таяния льда и Тs кипения воды, можно найти
. Аналогично, для произвольной температуры Т
где Q — количество теплоты, сообщенное системе в изотермическом процессе при температуре Т. Установленную таким образом температуру называют термодинамической. Единицей термодинамической температуры является Кельвин (К) — 1/273,16 термодинамической температуры тройной точки воды. Кельвин как единица температурного интервала равен 1/273,16 интервала термодинамической температуры между 0К и тройной точкой воды. Любая эмпирическая шкала приводится к термодинамической посредством введения поправок, учитывающих зависимость термометрического свойства данного вещества от температуры. Так как температура определяется по значению какой-либо характеристики термометрического вещества, то ее определение состоит в измерении таких физических параметров и характеристик, как объем, давление, электрические, механические, оптические, магнитные свойства и т. п. Разнообразие методов измерения температуры связано с большим количеством термометрических веществ и их свойств, используемых при этом.
Термометры — устройства для измерения температуры — состоят из чувствительного элемента, в котором реализуется термометрическое свойство, и измерительного прибора (дилатометр, манометр, гальванометр, потенциометр и т. д.). Необходимое условие измерения температуры — тепловое равновесие чувствительного элемента и тела, температура которого определяется. В зависимости от измеряемых интервалов температур наиболее распространены жидкостный, газовый термометры, термометр сопротивления, термопара как термометр и пирометры. В жидкостном термометре термометрической характеристикой является объем, чувствительным элементом — резервуар с жидкостью (обычно ртуть или спирт). В пирометрах в качестве термометрической характеристики используется интенсивность излу-
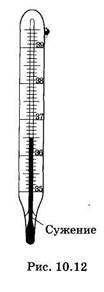
Используемый в медицине ртутный термометр указывает максимальную температуру и называется максимальным термометром. Эта особенность обусловлена его устройством: резервуар с ртутью отделен от градуированного капилляра волосяным сужением, которое не позволяет ртути при охлаждении термометра возвратиться в резервуар (рис. 10.12). Существуют и минимальные термометры, показывающие наименьшую температуру, наблюдаемую за длительный промежуток времени. Многие процессы в физике, химии и биологии существенно зависят от температуры, поэтому получение и поддержание определенной температуры является важной задачей. Для этой цели служат термостаты — приборы, в которых температура поддерживается постоянной, что осуществляют либо автоматическими регуляторами, либо используют для этого свойство фазовых переходов протекать при неизменной температуре. Для измерения количества теплоты, выделяющегося или поглощаемого в различных физических, химических и биологических процессах, применяют ряд методов, совокупность которых составляет калориметрию1. Калориметрическими методами измеряют теплоемкость тел, теплоты фазовых переходов, растворения, смачивания, адсорбции, теплоты, сопровождающие химические реакции, энергию излучения, радиоактивного распада и т. п. Подобные измерения производят с помощью калориметров. Эти приборы можно разделить на два основных типа: калориметры, в которых количество теплоты определяют по изменению их температуры, и калориметры, у которых температура постоянна и количество теплоты определяют по количеству вещества, перешедшего в • другое фазовое состояние (например, плавящееся твердое тело). Группу методов измерения тепловых эффектов, сопровождающих процессы жизнедеятельности, называют также биокалориметрией, а соответствующие приборы — биокалориметрами.
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-17; просмотров: 567; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.189.180.76 (0.008 с.) |




 чения (см. гл. 22). Принципиальное отличие пирометров от других термометров состоит в том, что их чувствительные элементы не находятся в непосредственном контакте с телом. Пирометры применяют для измерения сколь угодно высоких температур.
чения (см. гл. 22). Принципиальное отличие пирометров от других термометров состоит в том, что их чувствительные элементы не находятся в непосредственном контакте с телом. Пирометры применяют для измерения сколь угодно высоких температур.


