Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Обратный транспорт ХС из клетки с участием лпвпСтр 1 из 5Следующая ⇒
Обратный транспорт ХС из клетки с участием ЛПВП Функцию акцепции и удаления ХС из клетки выполняют ЛПВП. ЛПВП выполняют также и функцию донатора ХС по отношению к гепатоцитам, энте-роцитам, а также - к клеткам стероидогенных тканей - коркового вещества надпочечников и половых желез, снабжая эти клетки ХС для синтеза гормонов. ЛПВП-частицы содержат апопротеины A-1 и А-2, они богаты белком и ФЛ, содержат относительно мало ХС и ЭХС (3 и 15%, соответственно). ЛПВП осуществляют транспорт ХС из мембраны с помощью следующих механизмов: 1. через водную фазу по градиенту концентрации (так называемая ЛХАТ- 2. путем взаимодействия со специфическими ЛПВП-рецепторами клеточной мембраны. ЛХАТ - ловушка Реакция, катализируемая лецитин-холестерин-ацилтрансферазой (ЛХАТ), заключается в переносе остатка жирной кислоты из 2-го положения лецитина на гидроксильную группу ХС, в результате чего образуются лизолецитин и ЭХС. Исходные субстраты реакции находятся на поверхности ЛПВП-частицы, а образовавшиеся продукты удаляются с ее поверхности: ЭХС вследствие своей гидрофобности перемещается в ядро ЛПВП, а лизолецитин сорбируется на альбумине. Таким образом, в результате ЛХАТ-реакции на поверхности ЛПВП- частицы уменьшается содержание свободного ХС, в то время как в клеточной мембране или на поверхности ЛП других классов содержание свободного ХС значительно большее. Возникает градиент концентрации свободного ХС между мембраной и поверхностью ЛПВП: [ХСмембраны] > [ХСЛПВП ]. Следовательно, в результате контакта ЛПВП-частицы с мембраной клетки ХС из мембраны переходит на поверхность ЛПВП. Далее, с помощью ЛХАТ, эта молекула ХС вновь подвергнется эстерификации и переместится в ядро частицы, освобождая тем самым место для новых молекул ХС. Таким образом, ЛПВП и ЛХАТ работают как своеобразная «помпа» по откачке ХС из клеточных мембран или ЛП других классов. Рис. 5. Баланс ХС в макрофагах (по B.C. Репину, В.Н. Смирнову, 1989). ЛПНП - рецептор Скэвенджср-рсиептор для модифицированных ЛПНП Рецептор для бета-ЛПОНП Рецептор для комплексов ЛПНП-lg 5. рецептор для других атсрогснных ЛП, включая ЛП(а) Эндосома с ЛПНП-частицей
Пул ХС и его эфиров в лизосомах Пул ХС в цитоплазме (липидные капли) 9. мультимеллярные везикулы с ЭХС Рецептор для Л ПВП-3 11. ретроэндоцитоз ЛПВП2-частиц, обогащенных ЭХС АХАТ - ацил-КоА-холестерин-ацилтрансфераза ГЭХ — гидролаза эфиров ХС. ЛПВП-частицы, обогащенные ХС и апо-Е, направляются в печень, где взаимодействуют с апо-В, Е-рецепторами, интернализуются и разрушаются. Таким образом, апо-Е выступает в роли вектора, направляющего частицы ЛПВП в печень для окисления содержащегося в них ХС. Доказано, что ХС ЛПВП - предпочтительный субстрат для образования в гепатоцитах желчных кислот. Взаимодействие ЛПВП с гепатоцитами, по существу, завершает процесс «обратного» транспорта ХС в организме. Таким образом, ЛПВП активно забирают ХС из ГМК, фибробластов, макрофагов, эндотелиальных клеток и направляют его в печень для окисления и удаления из организма. Подводя итоги, можно констатировать, что существующие в норме механизмы регуляции доставки и удаления ХС достаточно эффективно поддерживают ХС гомеостаз отдельной клетки и целостного организма (рис. 6). Рис. 6. Транспорт ХС липопротеинамн различных классов из печени В периферическую клетку и обратно. В, С, Е - соответствующие Патологические ЛП 1. Бета-ЛПОНП. При некоторых нарушениях ЛП обмена в крови у человека и некоторых животных обнаруживаются бета-ЛПОНП или флотирующие бета-ЛП. В частности, бета-ЛПОНП появляются у экспериментальных кроликов, содержащихся на высокохолестериновой диете, а также у человека при III-м типе ДЛП.
Это - самостоятельная фракция ЛП, близкая по свойствам к ЛП промежуточной плотности, но отличающаяся от последних большей насыщенностью ХС, апо-Е-1 и путями катаболизма. Эти ЛП не превращаются в ЛПНП под действием печеночной липазы, как нормальные ЛП промежуточной плотности. Предполагается, что в результате структурных изменений они утрачивают сродство к этому ферменту и поэтому длительно циркулируют в крови. На макрофагах имеются специфические рецепторы к бета-ЛПОНП, в результате взаимодействия с которыми происходит их проникновение в клетку, однако этот процесс не регулируется по механизму обратной связи, поэтому макрофаги трансформируются в пенистые клетки, характерные для атеросклеротического процесса.
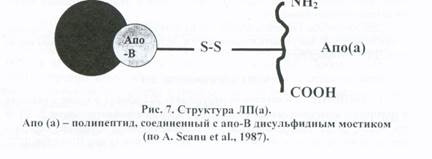
2. ЛПВПхс. Эта фракция ЛПВП появляется у экспериментальных кроликов, находящихся на ХС диете, а также у людей, потребляющих пищу, богатую 3. Разновидность ЛП, обозначаемая как ЛП-Х. Эти ЛП появляются в крови при заболеваниях печени, сопровождающихся застоем желчи и желтухой. 4. Липопротеин(а), ЛП(а), в англоязычной литературе - Lp(a). ЛП(а) - На долю апо(а) приходится 20% массы белка, на долю апо-В - около 65% и на долю необычного для ЛП белка - альбумина - около 15%. Обнаружено близкое структурное сходство апо(а) с плазминогеном - одним из факторов свертывания крови. В настоящее время точно не установлены места синтеза и катаболизма ЛП(а). Частичная деградация этих ЛП происходит путем их связывания с апо-В, Е-рецепторами. Один из наиболее важных аспектов изучения этих ЛП - их роль в развитии атеросклероза. На основании эпидемиологических исследований удалось установить четкую связь между повышенной концентрацией ЛП(а) в крови и развитием коронарного атеросклероза с инфарктом миокарда. Повышенный уровень ЛП(а) определяется более чем у половины пациентов, перенесших инфаркт миокарда. Особенно высок уровень этого ЛП у больных, перенесших инсульт. Считается, что 20-30 мг/дл - предельная концентрация ЛП(а) для здорового человека, превышение этого уровня рассматривается как патология. Важно то, что повышенный уровень ЛП(а) в крови практически не снижается при применении известных в настоящее время гиполипидемических препаратов. ЛП(а) обнаружены в местах поражения сосудов, причем отложения апо(а) располагаются, главным образом, внеклеточно и в участках скопления фибриногена, что подтверждает связь ЛП(а) со свертывающей системой крови. Атерогенность ЛП(а) может быть обусловлена следующими факторами: • Апо(а), соединенный с апо-В, задерживает деградацию и удаление • Апо(а), конкурируя с плазминогеном за места связывания на фибрине,
• ЛП(а) или очищенный апо(а) стимулирует рост ГМК аорты человека в Популяционные исследования, проведенные в различных регионах мира показали, что повышение уровня ЛП(а) в крови представляет собой самостоятельный и независимый фактор риска ИБС - наиболее частого и тяжелого клинического проявления атеросклероза. Таблица 2 ФАКТОРЫ РИСКА АТЕРОСКЛЕРОЗА Атеросклероз - мультифакторное заболевание, возникновение которого связано с многими факторами риска. Большинство кардиологов разделяют все факторы риска атеросклероза на управляемые и неуправляемые. Данный подход позволяет не просто констатировать наличие тех или иных факторов риска в целой популяции, но и осуществлять, по возможности, коррекцию конкретных факторов риска у конкретного индивидуума. К неуправляемым факторам риска относят: • Возраст • Пол • Наследственность К управляемым факторам риска относят: • Нерациональное питание с высоким содержанием животных жиров • Артериальная гипертензия • Ожирение • Курение • Интоксикация • Множественные психо-эмоциональные стрессы • Гиподинамия • Гипофункция щитовидной железы, сахарный диабет, нарушение толерантности к глюкозе и т.д. Несмотря на наличие множества факторов риска, все они в той или иной степени вызывают главное нарушение, являющееся ведущей причиной развития атеросклероза - атерогенную дислипопротеинемию (ДЛП). Таким образом, ДЛП - не фактор риска атеросклероза, а фактор, непосредственно обусловливающим развитие этого заболевания. Дислипопротеинемии Под термином «дислипопротеинемии» (ДЛП) понимают изменения в содержании ЛП в плазме крови, характеризующиеся их повышением, снижением или практически полным отсутствием. Сюда же относят случаи появления в крови необычных или патологических ЛП. Таким образом, понятие ДЛП охватывает все разновидности изменения уровня ЛП в крови. Более узкий термин -гиперлипопротеинемия, отражающая увеличение содержания какого-либо класса ЛП в крови. Первую классификацию ДЛП в 1967 г. предложил Д. Фредриксон, а в 1970г. ее одобрила ВОЗ. Классификация ДЛП по ВОЗ и характеристика клинических проявлений различных ДЛП представлены в таблицах.
Таблица 3 Диетическая коррекция ДЛП Европейская ассоциация экспертов сформулировала семь «золотых» правил питания, которые помогают значительно снизить заболеваемость атеросклерозом и сердечно-сосудистыми заболеваниями: 1. Уменьшить на 10% общее потребление жиров. 2. Резко уменьшить в рационе насыщенные жиры (животные жиры, масло, 3. Увеличить потребление продуктов, богатых полиненасыщенными жирными кислотами (растительные масла, рыба и морепродукты). 4. Увеличить в рационе долю клетчатки и сложных углеводов (овощи, 5. Заменить в домашнем приготовлении пищи сливочное масло и маргарин на растительное масло. 6. Резко уменьшить потребление продуктов, богатых холестерином. 7. Значительно снизить количество поваренной соли в рационе питания.
Лекарственная коррекция ДЛП Литература Основная: 1. Патологическая физиология / Под ред. Н.Н. Зайко. Элиста: АОЗГ Эсен, 1994. - С. 392- 2. Патологическая физиология / Под ред. А.Д. Адо. В.В. Новицкого. Томск: Изд. Томского 3. Патологическая физиология / Под ред. Н.Н. Зайко. Ю.В. Быць. Киев: Логос, 1996. - С. Дополнительная 1. Дзизинский А.Л. Атеросклероз. - М: Медицина. 1997. - 386 с. 2. Зайчик А.Ш., Чурилов Л.П. Основы общей патологии. Часть 2. Основы патохимии. 3. Климов А.Н.. Никульчева Н.Г. Липиды, липопротеины и атеросклероз. - Спб.: Питер 4. Литвинов А.В. Норма в медицинской практике. - М.: Медицина. 1999. - 144 с. 5. Митьковская Н.П.. Курченкова В.И., Вельская Е.С., Болотина Н.Г. Клинические аспекты 6. Нагорнев В.А. Кинетика клеточных элементов сосудистой стенки при атеросклерозе // 7. Оганов Р.Г. Факторы риска атеросклероза и ишемической болезни сердца. Вопросы профилактики. В кн.: Болезни сердца и сосудов / Под ред. Е.И. Чазова. М.: Медицина, 1992.
8. Репин B.C. Атеросклероз. В кн.: Болезни сердца и сосудов / Под ред. Е.И. Чазова. М.: 9. Репин B.C. Современные молекулярно-клеточные доказательства липопротеидной теории 10. Репин B.C., Смирнов В.Н. Фундаментальные науки против атеросклероза. Обзорная ин 11. Таганович А.Д. Основы структуры и метаболизм липопротеинов плазмы крови. Учебное 12. Холестериноз / Лопухин Ю.М., Арчаков А.И., Владимиров Ю.А., Коган Э.М. - М.: Медицина, 1983. -352 с. 13. Community prevention and control of cardiovascular diseases // Report of a WHO expert 14. Goldstein J.L., Brown M.S. Progress in understanding the LDL receptor and HMG-CoA- 15. Kodama Т., Freeman M., Rohrer L. et al. Type I macrophage scavenger receptor contains a-
16. Mahley R.W., Weisgraber K.H., Melchior G.W., Innerarity T.L. Inhibition of receptor-mediated 17. Scanu A.M., Pfaffmger D., Fless G.M. The lipid-free apo B-lOO-apolipoprotein(a) complex de
Учебное пособие
Касап Валентина Александровна Зиновкина Вера Юрьевна Висмонт Франтишек Иванович
АТЕРОСКЛЕРОЗ (патофизиологические аспекты) Методические рекомендации
Ответственная за выпуск доцент В.А. Касап Редактор Л.И. Жук Корректор А.В. Миронова Компьютерная верстка Н.М.Федорцовой
Подписано в печать 30.11.2000.Формат 60х84/16. Бумага писчая Усл. Печ. Л.2,32. Уч.-изд. л. 2,87. Тираж 150 экз. Заказ 574. Издательство и полиграфическое исполнение – Минский государственный медицинский институт ЛВ № 410 от 08.11.99; ЛП № 51 от 17.11.97. 220050, г. Минск, ул. Ленинградская, 6. Обратный транспорт ХС из клетки с участием ЛПВП Функцию акцепции и удаления ХС из клетки выполняют ЛПВП. ЛПВП выполняют также и функцию донатора ХС по отношению к гепатоцитам, энте-роцитам, а также - к клеткам стероидогенных тканей - коркового вещества надпочечников и половых желез, снабжая эти клетки ХС для синтеза гормонов. ЛПВП-частицы содержат апопротеины A-1 и А-2, они богаты белком и ФЛ, содержат относительно мало ХС и ЭХС (3 и 15%, соответственно). ЛПВП осуществляют транспорт ХС из мембраны с помощью следующих механизмов: 1. через водную фазу по градиенту концентрации (так называемая ЛХАТ- 2. путем взаимодействия со специфическими ЛПВП-рецепторами клеточной мембраны. ЛХАТ - ловушка Реакция, катализируемая лецитин-холестерин-ацилтрансферазой (ЛХАТ), заключается в переносе остатка жирной кислоты из 2-го положения лецитина на гидроксильную группу ХС, в результате чего образуются лизолецитин и ЭХС. Исходные субстраты реакции находятся на поверхности ЛПВП-частицы, а образовавшиеся продукты удаляются с ее поверхности: ЭХС вследствие своей гидрофобности перемещается в ядро ЛПВП, а лизолецитин сорбируется на альбумине. Таким образом, в результате ЛХАТ-реакции на поверхности ЛПВП- частицы уменьшается содержание свободного ХС, в то время как в клеточной мембране или на поверхности ЛП других классов содержание свободного ХС значительно большее. Возникает градиент концентрации свободного ХС между мембраной и поверхностью ЛПВП: [ХСмембраны] > [ХСЛПВП ]. Следовательно, в результате контакта ЛПВП-частицы с мембраной клетки ХС из мембраны переходит на поверхность ЛПВП. Далее, с помощью ЛХАТ, эта молекула ХС вновь подвергнется эстерификации и переместится в ядро частицы, освобождая тем самым место для новых молекул ХС. Таким образом, ЛПВП и ЛХАТ работают как своеобразная «помпа» по откачке ХС из клеточных мембран или ЛП других классов.
|
|||||||||||
|
Последнее изменение этой страницы: 2017-02-17; просмотров: 170; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.212.145 (0.048 с.) |