
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Сущность процесса кристаллизации
Сущность процесса кристаллизации стали заключается в переходе ее из жидкого состояния в твердое. При понижении температуры увеличивается вероятность существования образований (кристаллов или роев) с упорядоченным строением, а их структура приближается к структуре твердого кристалла. При определенной температуре, называемой температурой кристаллизации, термодинамически одинаково вероятно наличие в системе как жидкой, так и твердой фаз. При этой температуре свободная энергия чистого металла в жидком и твердом состояниях одинакова. Из схемы (рисунок 51) следует, что выше температуры кристаллизации Т2 > Те устойчивым является жидкое состояние Gж < Gтв и наоборот.
Сталь в изложницах кристаллизуется или затвердевает в виде кристаллов древовидной формы — дендритов. Процесс кристаллизации складывается из двух стадий — зарождения кристаллов и последующего их роста. Различают гомогенное и гетерогенное зарождение кристаллов. Под гомогенным подразумевают образование зародышей кристалла в объеме жидкой фазы, под гетерогенным — на имеющейся межфазной поверхности (на поверхности находящихся в расплаве твердых частиц — например, неметаллических включений, стенок изложниц и кристаллизаторов). Гомогенное зарождение - происходит следующим образом: в жидком металле вблизи точки кристаллизации вследствие флуктуации энергии, состава и плотности непрерывно образуются группировки атомов с упорядоченной структурой — комплексы или зародыши твердой фазы. Одновременно и непрерывно происходит разрушение большей части их них. С тем, чтобы зародыш стал термодинамически устойчивым, т. е. способным к дальнейшему росту необходимы определенные условия.
Условия гомогенного зарождения. Из термодинамики известно, что переход жидкости в твердое состояние и наоборот возможны, если свободная энергия системы при этом уменьшается. Затвердевание или расплавление в процессе изменения температуры объясняются тем, что при температурах, превышающих точку кристаллизации, меньшей удельной свободной энергией обладает жидкая фаза, а при более низких температурах — твердая. В процессе образования зародыша свободная энергия системы с одной стороны возрастает в результате затраты энергии на образование поверхности раздела «расплав — зародыш»
и с другой стороны уменьшается в результате перехода части жидкости в твердую фазу, у которой уровень свободной энергии ниже
где σ – межфазное натяжение на границе раздела фаз (удельная поверхностная энергия). При температуре кристаллизации свободная энергия жидкой и твердой фаз равны и образование зародыша невозможно, так как нет источника для компенсации затрат энергии на образование поверхности раздела фаз. Поэтому для образования зародыша необходимо некоторое переохлаждение расплава.
Величину критического радиуса зародыша определяют из соотношения:

где σ – межфазное натяжение на границе раздела жидкой и твердой фаз; Ткр — температура начала кристаллизации; ΔТ — величина переохлаждения; QKp — скрытая теплота кристаллизации. Таким образом, на процесс кристаллизации решающее влияние оказывают степень переохлаждения и удельная поверхностная энергия на границе кристалл—жидкость. При увеличении степени переохлаждения критический радиус зародыша уменьшается, т. е. термодинамически устойчивыми становятся более мелкие зародыши. Аналогичное влияние оказывает уменьшение величины поверхностной энергии σ.
Приближенные расчеты показывают, что гомогенное зарождение кристалла ряда металлов возможно при переохлаждении, равном 0,2•Ткр, т. е. около 350 °С для железа. Уменьшение переохлаждения до 200 °С снижает вероятность образования равновесного зародыша при гомогенной кристаллизации почти в 105 раз. Однако величина переохлаждения в стальном слитке обычно не превышает 10 °С. Следовательно, кристаллизация по гомогенному механизму на практике не реализуется. В реальных условиях механизм затвердевания имеет гетерогенный характер, когда образование и рост зародыша происходят на уже имеющейся поверхности раздела – центрах кристаллизации. Процесс зарождения и роста кристаллов в этом случае существенно облегчается - в реальных условиях сталь начинает кристаллизоваться при переохлаждении в несколько градусов. В формировании структуры слитка не меньшую роль играет последующий рост кристаллов, который обусловливается прежде всего интенсивностью и направленностью отвода тепла. Рост кристаллов. Зарождающийся кристалл имеет правильную форму, определяемую типом кристаллической решетки твердого металла. Однако вскоре после зарождения правильный рост возникшего кристалла прекращается и начинается преимущественный рост его вершин, т, е. ветвей дендрита. Объясняется это следующим: количество тепла и примесей сплава, выделяющихся при кристаллизации, будет минимальным у вершин и максимальным у центра граней кристалла, что препятствует дальнейшей кристаллизации у граней. От вершин кристалла вырастают оси первого порядка (стволы дендрита), на них перпендикулярно направленные оси второго порядка (ветви), на которых аналогичным образом развиваются оси третьего порядка и т. д. Появление все новых осей и их постепенное утолщение приводят к формированию сплошного кристалла (дендрита). При отсутствии направленного теплоотвода оси во всех направлениях развиваются примерно одинаково и кристалл получается равноосным. При направленном теплоотводе кристаллы имеют вытянутую форму. Вид структуры слитка определяется условиями охлаждения. Качественная связь между скоростью образования зародышей V0.3, линейной скоростью кристаллизации Vл. к и величиной переохлаждения представлена на рисунке 53.
 При высокой степени переохлаждения (при первоначальном контакте жидкого металла с холодной стенкой изложницы или кристаллизатора) число образовавшихся зародышей велико, а скорость роста зерна ограничена. В этом случае формируется мелкозернистая структура. По мере уменьшения переохлаждения скорость образования зародышей снижается быстрее, чем скорость их линейного роста. Кристаллы будут развиваться до больших размеров. При степени переохлаждения, равной ΔТ2, когда образуется мало зародышей, а скорость роста зерна еще велика – структура будет крупнозернистой. При высокой степени переохлаждения (при первоначальном контакте жидкого металла с холодной стенкой изложницы или кристаллизатора) число образовавшихся зародышей велико, а скорость роста зерна ограничена. В этом случае формируется мелкозернистая структура. По мере уменьшения переохлаждения скорость образования зародышей снижается быстрее, чем скорость их линейного роста. Кристаллы будут развиваться до больших размеров. При степени переохлаждения, равной ΔТ2, когда образуется мало зародышей, а скорость роста зерна еще велика – структура будет крупнозернистой.
Скорость роста кристаллов определяется в первую очередь интенсивностью теплоотвода; чем больше скорость теплоотвода и чем больше переохлаждение жидкого металла, тем больше будет скорость роста. Рост кристаллов протекает одинаково как в случае гомогенного, так и в случае гетерогенного их зарождения.
Интервал кристаллизации. Сталь как многокомпонентный раствор кристаллизуется в определенном интервале температур путем так называемой «избирательной кристаллизации». При температуре, соответствующей началу интервала кристаллизации образуются и начинают расти оси кристаллов, обедненные углеродом и другими составляющими стали, а в остающемся жидком металле их содержание возрастает. Поэтому понижается температура затвердевания жидкой фазы и последующие оси кристалла формируются при все более низкой температуре, а содержанке примесей в них возрастает. Величина интервала кристаллизации определяется составом стали и условиями затвердевания слитка. Она возрастает при увеличении содержания в стали углерода и легирующих элементов. При увеличении интервала кристаллизации возрастает степень химической неоднородности слитка. Скорость затвердевания слитка. При затвердевании стали в изложнице тепло отводится через ее стенки, поэтому зарождение и рост кристаллов начинаются у стенок изложницы, а толщина затвердевшего слоя непрерывно возрастает в направлении к центру слитка.
Разливка стали в изложницы
|
|||||||||||||
|
Последнее изменение этой страницы: 2017-02-17; просмотров: 708; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.136.97.64 (0.01 с.) |
 Таким образом, при температуре Те возможно возникновение кристаллика, который при определенных условиях может расти.
Таким образом, при температуре Те возможно возникновение кристаллика, который при определенных условиях может расти.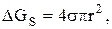
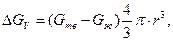
 При данной величине переохлаждения термодинамически устойчивыми, т. е. способными к дальнейшему росту, оказываются те зародыши, размер которых превысит так называемый «критический». Критический размер это такой, начиная с которого дальнейший рост сопровождается снижением суммарной свободной энергии образования зародыша (рисунок 52).
При данной величине переохлаждения термодинамически устойчивыми, т. е. способными к дальнейшему росту, оказываются те зародыши, размер которых превысит так называемый «критический». Критический размер это такой, начиная с которого дальнейший рост сопровождается снижением суммарной свободной энергии образования зародыша (рисунок 52).


