
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Раздел 5. Кислородсодержащие соединения алифатического ряда
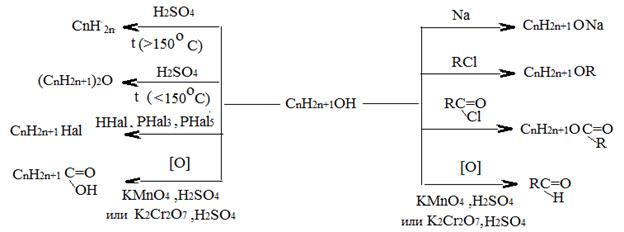
Спирты. Производные углеводородов в которых один или несколько атомов водорода замещены гидроксильной группой (-ОН) называют спиртами. В зависимости от числа гидроксильных групп различают одноатомные (например, метанол СН3ОН), двухатомные (например, 1,2-этандиол, или этиленгликоль HO-CН2- CН2-OH), трехатомные (например, 1,2,3-пропантриол, или глицерин CН2(OH)CH(OH)CН2OH и др.). Гомологические ряды предельных одноатомных спиртов, простых эфиров и эпоксидов имеют одну и ту же эмпирическую формулу CnН2n+2О. Однако их различие четко проявляется в реакциях со щелочными металлами, йодистым водородом, водой, аммиаком и т.д. Химические свойства спиртов определяются присутствием гидроксильной группы и подразделяются на реакции гидроксильного водрода (образование алголятов, простых и сложных эфиров), реакции самой гидроксилъной группы (дегидратация, замещение) и окисления:
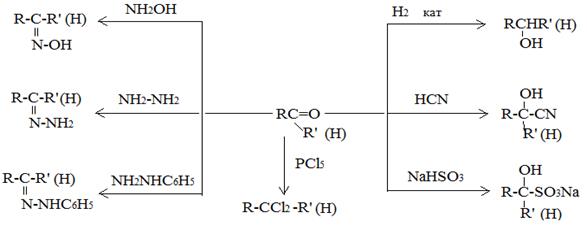
Сравните условия проведения промышленно важных реакций дегидрирования и окисления спиртов. Изучите реакции винилирования спиртов при действии ацетилена. Промышленные методы получения спиртов включают в себя каталитическую и кислотную гидратации олефинов, восстановление карбонильных соединений и биохимические методы. Получение, химические свойства и применение многоатомных спиртов следует рассмотреть на примерах этиленгликоля и глицерина. Альдегиды и кетоны. Альдегиды и кетоны характеризуются присутствием в их молекулах полярной карбонильной группы, которая и обуславливает их высокую реакционную способность. Реакционная способность карбонильного атома кислорода в альдегидах и кетонах позволяет осуществлять реакции присоединения к ним ряда веществ: NaHSO3, NH2OH, НCN, кислорода, водорода и др.
В зависимости от строения углеводородного радикала различают альдегиды и кетоны алифатического и ароматического рядов. Альдегиды и кетоны алифатического ряда. Это соединения, в которых карбонильная группа связана с алифатическим атомом углерода. Расположение атомов углерода в радикалах относительно карбонильной группы иногда указывают с буквами греческого алфавита α, β, γ, δ и т.д. или порядковым номером:
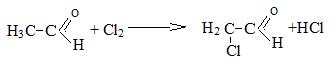
CH3 -.... CH2 - CH2 - CH2 – C – H 4 3 2 1 Водород, находящийся в α -положении к карбонильной группе, обладает повышенной реакционной способностью. Он может замещаться на хлор:
Альдольная конденсация альдегидов протекает по α- углеродному атому одной из двух реагирующих молекул:
Следует иметь в виду, что альдегиды обладают большей реакционной способностью, чем кетоны. Взаимодействие с аммиаком, спиртом, окисление в условиях реакции "серебряного зеркала", полимеризация, альдольная и кротоновая конденсация характерны только для альдегидов.
Из промышленных способов получения карбонильных соединений следует рассмотреть: I) оксосинтез (условия); 2) гидратацию алкинов (реакцию М.Г. Кучерова); 3) получение из дигалогенпроизводных углеводородов. В наибольших масштабах промышленность органического синтеза среди других представителей этого класса производит муравьиный альдегид (формальдегид), уксусный альдегид (ацетальдегид) и ацетон. Нужно изучить основные способы их получения. Карбоновые кислоты и их производные. Органические кислоты характеризуются наличием карбоксильной группы –СООН. По числу карбоксильных групп кислоты могут быть одноосновными (CH3COОH), двухосновными (HOOC(СН2)СООН) и т.д. В зависимости от строения углеводородного радикала кислоты могут быть предельными, непредельными и ароматическими. Важнейшим свойством органических кислот является подвижность атома водорода карбоксильной группы, с чем связано понятие кислотности:
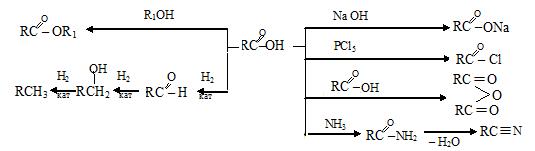
Самой сильной кислотой является муравьиная кислота НСООН. С ростом углеводородного радикала сила кислоты уменьшается. Важными химическими свойствами кислот являются: образования солей, ангидридов, галогенангидридов, сложных эфиров, амидов и нитрилов кислот.
Общими способами получения кислот являются окисление соответствующих углеводородов, спиртов, альдегидов, гидролиз нитрилов, магнийорганический синтез. Обратите внимание на промышленные синтезы муравьиной и уксусной кислот. Сложные эфиры глицерина и высших жирных кислот, например С17Н35COOH, являются жирами. Соли высших жирных кислот, например стеарат натрия С17Н35COONa, являются мылами. Это широко применяемые моющие средства.
Большой промышленный интерес представляют непредельные одноосновные кислоты, например акриловая кислота СН2=СН-СООН,
CH3 Полимеризацией последних и их эфиров СН2=СН-СООR получают синтетические волокна и органические стекла. Дикарбоновые кислоты (например, адипиновую HOOC(CН2)4СООН) используют для получения полиамидных и полиэфирных смол (найлона, лавсана и др.).
|
||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 443; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.14.6.194 (0.022 с.) |





 метакриловая кислота CH2 = C – COOH.
метакриловая кислота CH2 = C – COOH.


