
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Понятие и история естествознанияСтр 1 из 26Следующая ⇒
Е.П. Прохорова О.И. Тесленок ОСНОВЫ СОВРЕМЕННОГО ЕСТЕСТВОЗНАНИЯ
Пособие
Минск 2011
Введение
У любого человека уже в самом раннем возрасте возникает любопытство – естественное стремление познать окружающий мир. С возрастом это неосознанное стремление постепенно перерастает в осознанную форму любопытства – желание познать законы, которые управляют природой, способы их применения, позволяющие человеку предвидеть возможные последствия своих действий. Эти навыки важны для человека любой профессии. Для чего же будущим юристам или экономистам изучать естествознание? Во-первых, во избежание узости специального образования. По словам Д.И. Менделеева, «тот, кто знает только химию, тот и химию плохо знает». Действительно, современный специалист с высшим образованием должен быть широко образованным человеком, обладающим не только профессиональными знаниями, но и имеющим ясное представление об устройстве окружающего мира. Ведь первую оценку того или иного предложения настоящий руководитель любого ранга обычно производит самостоятельно, до того, как примет окончательное решение о необходимости прибегнуть к услугам других специалистов. Вероятность того, что оценка будет объективной, а решение – единственно верным, тем выше, чем шире профессиональный кругозор руководителя. Таким образом, первая задача, стоящая перед курсом «Основы современного естествознания», — это формирование в сознании студентов современной естественнонаучной картины мира.
Во-вторых, методы естественных наук оказались чрезвычайно плодотворными для решения экономических проблем. Это стало особенно очевидным в конце XX в. в связи с развитием синергетики — науки о самоорганизации сложных неравновесных систем. Вряд ли кто станет отрицать, что предполагаемые экономические решения, особенно если речь идет о крупных проектах, лучше вначале «обыграть» на математических и компьютерных моделях, прежде чем пускаться в рискованные эксперименты с реальными финансовыми потоками. Поэтому для подготовки высококвалифицированных специалистов экономического и юридического профиля важно знать и уметь применять естественнонаучные подходы в практической деятельности предприятия, отрасли, экономики в целом. Естествознание как наука Термин «естествознание» заимствован из старославянского языка и образован из слова естьство (представляющего собой прочтение греческого ousia — сущность, бытие) и слова знание, откуда получается буквальное толкование исследуемого слова — знание о бытии, знание о сущности. Следовательно, прямой перевод термина «естествознание» — учение о бытии. Естествознание — система наук об общих свойствах и закономерностях природы. Цели естествознания как науки: · выявлять сущность явлений природы, их законы и на этой основе предвидеть или создавать новые явления; · раскрывать возможности использования на практике познанных законов природы. Целью естествознания как учебной дисциплины является формирование в мировоззрении студентов естественнонаучной картины мира как части общей личностной картины мира. Предметом исследования современного естествознания является весь мир в его внутренней сложности, многообразии и единстве, а именно: · различные формы движения материи в природе; · уровни организации материи и их взаимосвязи; · основные формы всякого бытия — пространство и время; · закономерная связь явлений природы, как общего, так и специфического характера. К особенностям современного естествознания можно отнести: 1. возникновение ряда новых наук на стыках традиционных (например, физическая химия, химическая физика, геохимия и ряд других); 2. учет эволюционных процессов в природе (принцип глобального эволюционизма гласит, что Вселенная в целом и во всех ее элементах не может существовать без непрерывного развития); 3. переход от идеи покорения природы к эволюции вместе с ней (коэволюции); 4. объединение гуманитарной и естественнонаучной культур; 5. системный подход, в рамках которого объект исследования любого масштаба рассматривается как система некоторого уровня. Выводы 1. Естествознание - система наук о природных явлениях и процессах - ставит своей целью познание законов природы для предвидения или создания новых явлений, способных использоваться в практической деятельности современного человека. 2. Целью учебной дисциплины «Основы современного естествознания» является формирование современной естественнонаучной картины мира – целостной системы представлений об общих свойствах и закономерностях природы. Являясь частью общей личностной картины мира, естественнонаучная составляющая позволит расширить мировоззренческий потенциал студентов экономических и юридических специальностей.
3. Наука— особый рациональный способ познания мира, основанный на эмпирической проверке или математическом доказательстве. Выделяют фундаментальные и прикладные науки; естественные, общественные и технические. 4. Одним из основных внутренних факторов развития любой науки является динамика развития науки Т.Куна: старая парадигма – нормальная стадия развития науки – революция в науке – новая парадигма. Истинность научного знания устанавливается с помощью принципов верификации (эмпирической проверки) и фальсификации (попыток опровергнуть научное утверждение). 5. Научное познание осуществляется на двух уровнях – эмпирическом (чувственного познания) и более высоком теоретическом (преимущественно рационального познания, то есть построенного с учетом логики). 6. В истории естествознания выделяют следующие периоды: до 1900 гг. – классическое, 1900-1960 гг. – неклассическое (квантовое), начиная с 1960-70-х гг. – постнеклассическое. Другой подход разбивает историю естествознания на этапы натурфилософии, аналитического, синтетического и интегрального естествознания. 7. Глобальные научные революции осуществляли радикальную смену научных картин мира благодаря трудам целого ряда ученых, наиболее значимыми из которых признаются Аристотель, И.Ньютон, А.Эйнштейн. Четвертая научная революция – научно-техническая – носит особый статус ввиду превращения науки в ведущий фактор развития современного общества.
Структурные уровни материи В настоящее время считается, что признаком структуры материи являются размер объекта и его масса. На основе этих критериев выделяют следующие уровни организации ( структурные уровни) материи: микромир, макромир, мегамир. - микромир – область предельно малых, непосредственно ненаблюдаемых материальных объектов, размер которых определяется в диапазоне от 10-8 до 10-16 см, а время жизни – от бесконечности до 10-24 с. Это мир атомов и элементарных частиц, которые обладают как волновыми, так и корпускулярными свойствами. - макромир – мир материальных объектов, соизмеримых по своим масштабам с человеком. На этом уровне пространственные величины измеряются в диапазоне от миллиметров до километров, а время в диапазоне от секунд до лет. Макромир представлен макромолекулами (полимеры), веществами в различных агрегатных состояниях (газ, жидкость, твердое), живыми организмами, человеком и продуктами его деятельности.
- мегамир – сфера огромных космических масштабов и скоростей, расстояние в котором измеряется астрономическими единицами, световыми годами и парсеками (см 4.1), а время существования космических объектов – миллионами и миллиардами лет. К этому уровню относятся наиболее крупные материальные объекты и их системы: звезды, галактики и их скопления (метагалактики). Основы классической физики. Эволюция классической физики представляет собой формирование механистической, термодинамической и электромагнитной картин мира. Основы классической физики были заложены в XVI в Г.Галиллеем, а затем развиты в XVII в в механике И.Ньютона. Законы сохранения. Важными законами в классической физике являются законы сохранения. Закон сохранения электрического заряда: в электрически замкнутой системе сумма зарядов есть величина постоянная. Т.е. электрические заряды могут возникать и исчезать, но при этом обязательно появляется и исчезает равное количество элементарных зарядов противоположных знаков. Закон сохранения массы вещества. Массы веществ, вступивших во взаимодействие (реакцию), всегда будут равны массам веществ, образовавшихся в результате взаимодействия. Закон сохранения энергии. Энергия никогда не образуется и не уничтожается, она только переходит из одного вида в другой. Э нергия – универсальная мера различных форм движения и взаимодействия материи. Закон сохранения энергии и в настоящее время является важнейшим научным принципом. Новая форма действия этого закона основана на учете взаимосвязи массы и энергии: Е = mс2, где E — энергия тела, m — его масса, c — скорость света в вакууме, равная 300 000 км/с. Таким образом, в современной физике закон сохранения массы применяется совместно с законом сохранения энергии. Закон сохранения импульса: импульс замкнутой системы, на которую не действуют внешние силы (или действие этих сил скомпенсировано), сохраняется, т. е. не изменяется с течением времени. Импульс (количество движения) – векторная физическая величина, характеризующая меру механического движения тела. В классической механике импульс тела p равен произведению массы этого тела m на его скорость v, направление импульса совпадает с направлением вектора скорости: p = mv Следствием законов сохранения являются законы движения. Классическая физика опирается на законы движения Ньютона. Первый закон (закон инерции): тело сохраняет состояние покоя или равномерного и прямолинейного движения, пока на него не оказывают воздействие другие тела. Способность тела сопротивляться воздействию на него сил называется инертностью. Второй закон: ускорение, приобретаемое телом в результате воздействия на него силы, прямо пропорционально действующей силе и обратно пропорционально массе тела. Если ускорение равно а, сила равна F, масса равна m, то
a = F/m. Третий закон: силы, с которыми тела действуют друг на друга, равны по величине (модулю) и противоположны по направлению. Силы действуют вдоль прямой, соединяющей эти тела, т.е. каждому действию всегда соответствует равное и противоположно направленное противодействие. Из второго и третьего законов движения вытекает закон сохранения импульса. Система законов движения была дополнена законом всемирного тяготения. Закон всемирного тяготения: тела притягиваются друг к другу с силой, которая прямо пропорциональна произведению их масс, и обратно пропорциональна квадрату расстояния между ними. Законы Ньютона послужили основой классического естествознания, но по своей сути МКМ являлась метафизичной (т.е. абстрактной, не учитывающей внутренние связи), т.к. все многообразие законов материального мира сводилось к механике. Механистическая картина мира фактически отвергала качественные изменения, сводя все к изменениям чисто количественным. Выводы 1. Физика – наука о природе, изучающая простейшие и вместе с тем наиболее общие свойства материального мира. Различают следующие виды материи: вещество, физическое поле и физический вакуум. Формы и свойства материи описывают с точки зрения корпускулярной и континуальной теории. Выделяют следующие уровни организации (структурные уровни) материи: микромир, макромир, мегамир. 2. В истории развития физики как науки выделяют период становления классической физики (17 век – начало 20 века) и период современной физики (с 1905 г). Эволюция классической физики представляет собой формирование механистической, термодинамической и электромагнитной картин мира. 3. Механистическая картина мира опирается на атомно-молекулярное учение о строении вещества. Важнейшими принципами МКМ являются: принцип относительности, принцип дальнодействия, принцип причинности. Важными законами в классической физике являются законы сохранения: (Закон сохранения электрического заряда, Закон сохранения массы, Закон сохранения энергии), законы движения (первый, второй, третий законы движения Ньютона, закон сохранения импульса, закон всемирного тяготения) 4. Термодинамическая картина мира опирается на первое и втрое начало термодинамики. Первое начало термодинамики: количество теплоты ΔQ, сообщенное телу, идет на увеличение его внутренней энергии ΔU и на совершение телом работы А. Второе начало термодинамики: нельзя осуществить работу за счет энергии тел, находящихся в состоянии термодинамического равновесия. Второе начало термодинамики называют также законом возрастания энтропии: для всех происходящих в замкнутой системе тепловых процессов энтропия системы возрастает; максимально возможное значение энтропии замкнутой системы достигается в тепловом равновесии: Таким образом, замкнутая система, находящаяся в состоянии равновесия, обладает максимальной неупорядоченностью и минимальной энергией. 5. Основой электромагнитной картины мира является теория электромагнитного поля. Сущность теории электромагнитного поля заключается в следующем: - источниками электромагнитного поля могут быть электрические заряды или изменяющиеся во времени магнитные поля. Магнитные поля могут возбуждаться движущимися электрическими зарядами или переменными электрическими полями. 6. Современная физика формируется на основе релятивистской квантовой механики. Она отказывается от наглядности, признает различие микро-, макро- и мегамира, опирается на принципы дополнительности и неопределенности, и для описания процессов использует статистические закономерности, которые носят вероятностный характер. 7. Современной физики опирается на положения теории относительности (специальной и общей). Специальная теория относительности распространила принципы относительности для механических систем на электромагнитные взаимодействия. Она показала, что пространство и время связаны между собой и зависят от скорости движения системы отсчета, в которой проводятся измерения. Общая теория относительности (гравитационная теория) позволяет рассматривать не только инерциальные системы отсчета, но и любые системы координат, которые движутся по криволинейным траекториям и с любыми ускорениями. Она установила, что законы геометрии меняются около тяжелых тел. 8. В современной физике вещество изучается на субатомном и субъядерном уровнях. Атом – электронейтральная система, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. Ядро состоит из положительно заряженных протонов и нейтральных нейтронов (нуклонами). 9. Элементарные частицы – структурные элементы микромира. Фундаментальными частицами микромира являются кварки. По свойствам и характеру взаимодействия элементарные частицы принято делить на фермионы (частицы, составляющие вещество) и бозоны (частицы, которые переносят взаимодействие). Характеристиками элементарных частиц являются: масса покоя, электрический заряд, спин, время жизни. Микрочастицы обладают корпускулярно-волновым дуализмом, т.е. могут вести себя одновременно и как волна, и как частица. 10. Взаимодействие – важнейшее свойство материи. За счет взаимодействия объекты объединяются в системы. Различают следующие виды фундаментальных взаимодействий: гравитационное, электромагнитное, сильное и слабое. Гравитационное взаимодействие. Источником гравитационного взаимодействия является масса тела, оно проявляется через взаимное притяжение тел согласно закону всемирного тяготения. Электромагнитные взаимодействия возникают между заряженными частицами. Слабое взаимодействие проявляется в некоторых видах ядерных процессов и объясняет процессы радиоактивности (распад ядер атомов). 11. Сильное взаимодействие обеспечивает связь протонов и нейтронов (нуклонов) в ядре, и отвечает за образование ядер атомов. Таким образом, сильное взаимодействие не дает протонам разлетаться за счет электромагнитных сил отталкивания. Учение о составе вещества В основе классической химии лежит концепция атомизма, которая была сформулирована еще в античной философии Левкипом, Демокритом и Эпикуром. На основе атомизма в середине 19 века были сформулированы основные положения атомно-молекулярного учения. 1. Вещества состоят из молекул. Молекула - наименьшая частица вещества, обладающая его химическими свойствами. Молекулы отличаются между собой составом, размерами, физическими и химическими свойствами. 2. Молекулы находятся в непрерывном движении; между ними существует взаимное притяжение и отталкивание. Скорость движения молекул зависит от агрегатного состояния веществ. 3. При физических явлениях состав молекул остается неизменным, при химических реакциях из одних молекул образуются другие. 4. Молекулы состоят из атомов. Свойства атомов одного элемента отличаются от свойств атомов других элементов. Атомы характеризуются определенными размерами и массой. Масса атома, выраженная в атомных единицах массы (а.е.м.) называется относительной атомной массой. 1 а.е.м. = 1,667 10-27кг. Атомно-молекулярное учение позволило объяснить основные понятия и законы химии. Понятие «химический элемент» предложил Р.Бойль, обозначение химических элементов символами предложил в 1814 г. Й. Берцелиус. Х имический элемент – определенный вид атомов с одинаковым зарядом ядра. Заряд ядра численно равен порядковому номеру элемента в периодической системе. В настоящее время известно 118 химических элементов, из них 94 обнаружены в природе, остальные 24 получены искусственно в результате ядерных реакций. Атом - наименьшая частица химического элемента, сохраняющая все его химические свойства. Химические свойства элемента определяются строением его атома. Отсюда следует определение атома, соответствующее современным представлениям: Атом - это электронейтральная частица, состоящая из положительно заряженного атомного ядра и отрицательно заряженных электронов. Изотопы – атомы одного и того же химического элемента, имеющие разную массу и, соответственно, различное количество нейтронов в ядре. Изотопы могут быть стабильными, т.е. их ядра не подверженными самопроизвольному распаду, и радиоактивными, которые способны превращаться в атомы других элементов до тех пор, пока не образуется стабильный изотоп (Уран-238 Аллотропия – способность элементов существовать в виде различных простых веществ, отличающихся физическими и химическими свойствами. Аллотропия может быть результатом образования молекул с различным числом атомов (например, атомарный кислород O, молекулярный кислород O2 и озон O3) или образования различных кристаллических форм (например, графит и алмаз). В результате аллотропии из 118 элементов образуется около 400 простых веществ. Молекула - это наименьшая частица данного вещества, обладающая его химическими свойствами. Понятие молекула ввел итальянский ученый А.Авогадро. В 1811 году он предложил молекулярную теорию строения вещества. Химические свойства молекулы определяются ее составом и химическим строением. Размеры молекул определяются их массой и структурой и у больших молекул могут достигать 10-5 см. В настоящее время известно свыше 18 млн. видов молекул разных веществ. Химическая формула - это условная запись состава вещества с помощью химических знаков и индексов. Химическая формула показывает, атомы каких элементов и в каком отношении соединены между собой в молекуле. Основные химические законы. Закон сохранения массы (М.В.Ломоносов, А.Л.Лавуазье): масса веществ, вступивших в реакцию, равна массе веществ, образующихся в результате реакции. С точки зрения атомно-молекулярного учения в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка (химическое превращение). Поскольку число атомов до и после реакции остается неизменным, то их общая масса также изменяться не должна. Исходя из закона сохранения массы, можно составлять уравнения химических реакций и по ним производить расчеты. Этот закон является основой количественного химического анализа. В начале 20 века формулировка закона сохранения массы подверглась пересмотру в связи с появлением теории относительности (см. п.2.4.1), согласно которой масса тела зависит от его скорости и, следовательно, характеризует не только количество материи, но и ее движение. Полученная телом энергия Закон постоянства состава вещества: Согласно закону постоянства состава, всякое химически чистое вещество имеет постоянный качественный и количественный состав независимо от способа его получения. Качественный и количественный состав вещества показывает химическая формула. Например, независимо от того, каким способом получено вещество вода (Н2О), оно имеет постоянный состав: два атома водорода и один атом кислорода. Из закона постоянства состава следует, что при образовании сложного вещества элементы соединяются друг с другом в определенных массовых соотношениях. В настоящее время установлено, что этот закон всегда выполним для соединений с молекулярной структурой. Состав же соединений с немолекулярной структурой (с атомной, ионной и металлической кристаллической решеткой) не является постоянным и зависит от условий получения. Закон кратных отношений (Дж. Дальтон) - если два элемента образуют друг с другом несколько химических соединений, то массы элементов соотносятся между собой как небольшие целые числа. Например: в оксидах азота N2O, N2O3, NO2 (N2O4), N2O5 число атомов кислорода, приходящихся на два атома азота, относятся между собой как 1: 3: 4: 5. Закон объемных отношений (Гей-Люссак)- объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа. Следовательно, стехиометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получаются газообразные вещества. Например: 2CO + O2 При окислении двух объемов оксида углерода (II) одним объемом кислорода образуется 2 объема углекислого газа, т.е. объем исходной реакционной смеси уменьшается на 1 объем. Закон Авогадро - в равных объемах любых газов, взятых при одной и той же температуре и при одинаковом давлении, содержится одно и то же число молекул. Согласно этому закону: · одно и то же число молекул различных газов при одинаковых условиях занимает одинаковые объемы; · 1моль любого идеального газа при нормальных условиях (0°C = 273°К, 1 атм = 101,3 кПа) занимает одинаковый объем 22,4 л. Французский химик А.Л. Лавуазье впервые попытался систематизировать химические элементы в соответствии с их массой. Английский химик Дж.Дальтон ввел понятие атомная масса и явился создателем теории атомного строения. В 1804 году он предложил таблицу относительных атомных масс водорода, азота, углерода, серы и фосфора, приняв за единицу атомную массу водорода. В настоящее время атомная масса измеряется относительно 1/12 массы атома изотопа углерода. Работу по изучению свойств атомов продолжил Д.И. Менделеев и в 1869 г. сформулировал периодический закон и разработал Периодическую систему химических элементов. Периодический закон был сформулирован в следующем виде: «Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов». В качестве системообразующего фактора Д.И.Менделеев использовал массу химического элемента. В Периодической системе Д.И. Менделеева насчитывалось 62 элемента. Квантовая механика уточнила, что свойства химических элементов и их соединений определяются зарядом атомного ядра. Современная формулировка периодического закона химических элементов: свойства простых веществ, а также формы и свойства соединений элементов находятся в периодической зависимости от величины заряда ядра атомаи определяются периодически повторяющимися однотипными электронными конфигурациями их атомов. Реакционная способность атома химического элемента определяется количеством электронов на внешней оболочке атома. Валентность – свойства атомов одного элемента образовывать определенное число связей с атомами других элементов. Осуществляют химические связи между атомами электроны, расположенные на внешней оболочке и связанные с ядром наименее прочно. Их назвали валентными электронами. Определить валентность (число валентных электронов) можно по таблице Д.И.Менделеева, зная номер группы, в которой находится химический элемент. Электроотрицательность – свойство атома в соединении притягивать к себе валентные электроны. Чем сильнее атом оттягивает к себе электроны, тем больше его электроотрицательность. Степень окисления - условный заряд, который образуется на атоме, если учесть, что электрон при образовании связи переходит полностью к более электроотрицательному атому. Максимальная степень окисления элемента определяется номером группы в таблице Менделеева. Атомы в молекулах связаны между собой химическими связями, которые образуются за счет перераспределения валентных электронов между атомами. При образовании химической связи атомы стремятся приобрести устойчивую (завершенную) внешнюю электронную оболочку. Химическая связь – вид фундаментального электромагнитного взаимодействия. Образование химической связи происходит за счет притяжения положительных и отрицательных зарядов, которые образуются на атоме при потере или смещении его электрона со стационарной орбиты. В зависимости от характера взаимодействия атомов различают ковалентную, ионную, металлическую и водородную химические связи. Ковалентная связь осуществляется за счет образования общих электронных пар между двумя атомами. Она может быть полярной и неполярной. Ионная связь представляет собой электростатическое притяжение между ионами, которые образуются за счет полного смещения электронной пары к одному из атомов. Металлическая связь — это связь между положительными ионами металлов посредством общего электронного облака («электронного газа»). Кроме внутримолекулярных связей образуются и межмолекулярные связи. Межмолекулярные взаимодействия - взаимодействия молекул между собой, не приводящие к разрыву или образованию внутримолекулярных химических связей. От межмолекулярных взаимодействий зависят агрегатное состояние вещества, структурные, термодинамические, теплофизические и другие свойства веществ. Примером межмолекулярной связи является водородная связь. Водородная связь - межмолекулярная связь, образованная за счет притяжения более электроотрицательного атома (F, O, N), и атома водорода с частичным положительным зарядом. Например, водородная связь реализуется между молекулами воды, спирта, органических кислот. Она оказывает влияние на температуру кипения вещества. Водородная связь может образоваться и внутри молекул. Например, внутримолекулярные водородные связи существуют в молекулах нуклеиновых кислот, белков, полипептидов и др. и определяют структуру этих макромолекул Учение о строении вещества Химическая связь образуется в определенном направлении в пространстве и задает пространственную ориентацию (структуру) молекулы. Теория химического строения вещества была разработана в середине 19 века благодаря трудам шотландского химика А.Купера, немецкого химика А.Кекуле и русского химика А. М. Бутлерова. Эта теория объясняла огромное разнообразие органических веществ, которые образованы весьма небольшим числом химических элементов. Выводы 1. Химия – наука о веществах и их превращениях, которые сопровождаются изменением состава и строения вещества. 2. В истории развития химии как науки выделяют четыре этапа, в течение каждого формируется определенная концептуальная система знаний:учение о составе вещества, учение о структуре вещества, учение о химических процессах, эволюционная химия. 3. Основой химии являются атомно-молекулярное учение о составе вещества и основные химические законы: закон сохранения массы, закон постоянства состава вещества, закон кратных отношений, закон объемных отношений, закон Авогадро, периодический закон Д.И.Менделеева. 4. Вещество состоит из молекул. Молекула - это наименьшая частица данного вещества, обладающая его химическими свойствами. Молекулы состоят из атомов. Х имический элемент – определенный вид атомов с одинаковым зарядом ядра. Атомы способны образовывать химические связями согласно валентности. Различают ковалентную, ионную, металлическую и водородную химические связи. 5. Химическая связь образуется в определенном направлении в пространстве и задает пространственную ориентацию (структуру) молекулы. Теория химического строения вещества определяет зависимость свойств вещества от структуры молекулы. Изомеры – вещества, имеющие одинаковый состав, но разное строение молекулы. Изомерия может быть структурной и пространственной. 6. Учение о химическом процессе изучает возможности и условиях протекания химических реакций и способы управления ими. Химическая реакция – процесс превращения исходных веществ в отличающиеся по химическому составу и строению другие вещества. Учение о химическом процессе рассматривает энергетику химических реакций, химическое равновесие и условия его смещения, кинетику (скорость) и механизмы реакций. Особое значение имеют каталитические реакции, так как основой процессов в живом организме является биокатализ, который протекает под действием ферментов. 7. Эволюционная химия изучает процессы самопроизвольного синтеза новых химических соединений, являющихся более сложными и высокоорганизованными по сравнению с исходными веществами. Существует два разных подхода к проблеме самоорганизации предбиологических систем - субстратный и функциональный.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 550; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.250.114 (0.067 с.) |
 Свинец-206).
Свинец-206).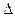 E связана с увеличением его массы
E связана с увеличением его массы 


