

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Варіанти домашніх індивідуальних завдань
Таблиця 2
| №
варіанту
| ДІЗ №1 до модулю 1
| ДІЗ №2 до модулю 2
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
ЗАВДАННЯ ДЛЯ ІНДИВІДУАЛЬНОЇ РОБОТИ
1-30. Молярний коефіцієнт світлопоглинання сполуки металу в розчиннику при λ дорівнює ε. Яку масову частку металу можливо визначити, якщо із наважки зразка сплаву масою m одержують розчин об’ємом V і вимірюють мінімальну оптичну густину D у кюветі товщиною ℓ см.
| №
| метал
| λ,нм
| ε
| m,г
| V, мл
| Dmin
| ℓ,см
| |
| Мідь
|
| 4,52·104
| 1,00
|
| 0,020
|
| |
| Залізо
|
| 6,00·103
| 2,20
|
| 0,029
|
| |
| Олово
|
| 3,00·103
| 1,55
|
| 0,053
|
| |
| Хром
|
| 1,12·103
| 3,45
|
| 0,034
|
| |
| Свинець
|
| 2,00·102
| 2,50
|
| 0,061
|
| |
| Марганець
|
| 6,20·104
| 3,20
|
| 0,055
|
| |
| Ванадій
|
| 4,30·103
| 1,80
|
| 0,033
|
| |
| Кобальт
|
| 1,50·104
| 2,60
|
| 0,039
|
| |
| Титан
|
| 1,10·104
| 1,40
|
| 0,026
|
| |
| Молібден
|
| 1,30·104
| 4,00
|
| 0,048
|
| |
| Нікель
|
| 1,30·103
| 3,30
|
| 0,036
|
| |
| Цинк
|
| 9,20·104
| 2,25
|
| 0,029
|
| |
| Алюміній
|
| 7,30·103
| 1,60
|
| 0,027
|
| |
| Вісмут
|
| 4,84·104
| 1,22
|
| 0,024
|
| |
| Срібло
|
| 4,00·104
| 1.00
|
| 0,012
|
| |
| Скандій
|
| 3,20·103
| 0,80
|
| 0,032
|
| |
| Вольфрам
|
| 8,80·102
| 1,10
|
| 0,062
|
| |
| Кадмій
|
| 5,15·104
| 1,90
|
| 0,043
|
| |
| Стронцій
|
| 3,30·103
| 2,15
|
| 0,039
|
| |
| Рубідій
|
| 5,10·104
| 3,60
|
| 0,028
|
| |
| Тантал
|
| 4,90·104
| 4,00
|
| 0,037
|
| |
| Талій
|
| 3,75·103
| 3,10
|
| 0,057
|
| |
| Паладій
|
| 8,98·104
| 2,40
|
| 0,036
|
| |
| Рутеній
|
| 1,27·103
| 0,60
|
| 0,026
|
| |
| Цирконій
|
| 3,50·104
| 2,70
|
| 0,084
|
| |
| Ніобій
|
| 1,10·104
| 0,80
|
| 0,032
|
| | №
| метал
| λ,нм
| ε
| m,г
| V, мл
| Dmin
| ℓ,см
| |
| Індій
|
| 2,35·104
| 1,45
|
| 0,054
|
| |
| Лантан
|
| 7,70·103
| 1,80
|
| 0,067
|
| |
| Празеодим
|
| 5,52·102
| 1,10
|
| 0,032
|
| |
| Неодим
|
| 1,02·102
| 2,30
|
| 0,045
|
|
31-60. Визначте молярну концентрацію йонів металу, якщо оптична густина досліджуваного розчину дорівнює Dд, а стандартного розчину, який містить m мг йонів металу у певному об’ємі V мл, Dcт.
| №
| метал
| Dд
| Dcт
| m,мг
| V, мл
| |
| Залізо
| 0,250
| 0,820
| 0,0576
| 25,00
| |
| Свинець
| 0,295
| 0,730
| 0,0342
| 10,00
| |
| Рубідій
| 0,530
| 0,850
| 0,0225
| 50,00
| |
| Стронцій
| 0,342
| 0,634
| 0,0432
| 25,00
| |
| Мідь
| 0,461
| 0,555
| 0,0754
| 25,00
| |
| Кобальт
| 0,155
| 0,315
| 0,0534
| 50,00
| |
| Хром
| 0,332
| 0,753
| 0,0289
| 25,00
| |
| Марганець
| 0,398
| 0,649
| 0,0477
| 50,00
| |
| Нікель
| 0,296
| 0,426
| 0,0387
| 25,00
| |
| Ванадій
| 0,485
| 0,734
| 0,0430
| 50,00
| |
| Титан
| 0,166
| 0,372
| 0,0260
| 25,00
| |
| Вісмут
| 0,292
| 0,720
| 0,0470
| 50,00
| |
| Молібден
| 0,127
| 0,364
| 0,0854
| 25,00
| |
| Цинк
| 0,224
| 0,496
| 0,0389
| 25,00
| |
| Вольфрам
| 0,124
| 0,347
| 0,0542
| 50,00
| |
| Алюміній
| 0,321
| 0,854
| 0,0478
| 25,00
| |
| Срібло
| 0,326
| 0,549
| 0,0687
| 25,00
| |
| Скандій
| 0,430
| 0,544
| 0,0332
| 50,00
| |
| Кадмій
| 0,239
| 0,684
| 0,0776
| 25,00
| |
| Олово
| 0,128
| 0,456
| 0,0634
| 50,00
| |
| Ніобій
| 0,237
| 0,580
| 0,0523
| 25,00
| |
| Осмій
| 0,257
| 0,435
| 0,0279
| 50,00
| |
| Реній
| 0,236
| 0,406
| 0,0483
| 50,00
| | №
| метал
| Dд
| Dcт
| m,мг
| V, мл
| |
| Лантан
| 0,326
| 0,527
| 0,0821
| 25,00
| |
| Індій
| 0,184
| 0,468
| 0,0240
| 25,00
| |
| Тантал
| 0,132
| 0,320
| 0,0350
| 50,00
| |
| Цирконій
| 0,254
| 0,545
| 0,0629
| 25,00
| |
| Рутеній
| 0,367
| 0,670
| 0,0580
| 50,00
| |
| Паладій
| 0,432
| 0,785
| 0,0274
| 50,00
| |
| Талій
| 0,345
| 0,655
| 0,0227
| 25,00
|
61-90. При визначенні NaCl у розчині натрій гідроксиду приготували стандартний розчин. Для цього V мл розчину NaCl (Т = 0,100 мг/мл) перенесли у мірну колбу місткістю 25,0 мл, додали реактиви, які необхідні для одержання суспензії AgCl, виміряли удавану оптичну густину за допомогою нефелометра Dст. Наважку розчину, що аналізується, масою m г нейтралізували нітратною кислотою, перенесли у мірну колбу і приготували V1 мл розчину, V2 мл якого використали для приготування 25,0 мл суспензії AgCl. Визначте масову частку NaCl, якщо удавана оптична густина приготовленої суспензії AgCl має значення Dд.
| №
| m,г
| V,мл
| Dст
| V1,мл
| V2, мл
| Dд
| |
| 19,35
| 1,50
| 1,050
| 50,0
| 1,0
| 0,563
| |
| 25,41
| 2,00
| 0,950
| 50,0
| 2,0
| 0,332
| |
| 22,44
| 1,00
| 0,870
| 25,0
| 3,0
| 0,462
| |
| 17,33
| 0,30
| 1,100
| 100,0
| 1,0
| 0,743
| |
| 19,99
| 0,50
| 1,225
| 25,0
| 2,0
| 0,839
| |
| 18,45
| 0,70
| 1,290
| 100,0
| 4,0
| 0,928
| |
| 13,73
| 0,40
| 1,150
| 50,0
| 1,5
| 0,337
| |
| 15,86
| 0,80
| 1,200
| 25,0
| 2,7
| 0,857
| |
| 17,93
| 1,20
| 0,970
| 50,0
| 3,5
| 0,636
| |
| 28,84
| 1,50
| 0,845
| 100,0
| 4,0
| 0,526
| |
| 22,66
| 1,30
| 0,615
| 50,0
| 1,5
| 0,384
| |
| 21,15
| 0,60
| 0,990
| 25,0
| 2,0
| 0,532
| | №
| m,г
| V,мл
| Dст
| V1,мл
| V2, мл
| Dд
| |
| 27,05
| 1,80
| 0,680
| 50,0
| 3,5
| 0,432
| |
| 25,75
| 0,90
| 0,730
| 100,0
| 5,5
| 0,362
| |
| 15,25
| 1,10
| 0,855
| 50,0
| 4,0
| 0,468
| |
| 14,76
| 1,00
| 0,550
| 25,0
| 2,0
| 0,325
| |
| 17,82
| 2,10
| 1,140
| 50,0
| 1,0
| 0,545
| |
| 11,96
| 1,90
| 0,880
| 50,0
| 1,5
| 0,670
| |
| 18,05
| 1,40
| 1,225
| 25,0
| 2,5
| 0,787
| |
| 12,36
| 1,60
| 0,940
| 50,0
| 3,8
| 0,469
| |
| 28,00
| 2,40
| 0,715
| 100,0
| 2,0
| 0,488
| |
| 26,70
| 2,20
| 0,580
| 50,0
| 1,8
| 0,368
| |
| 30,12
| 1,70
| 0,980
| 100,0
| 3,3
| 0,582
| |
| 16,27
| 0,60
| 1,145
| 50,0
| 1,9
| 0,659
| |
| 20,82
| 1,90
| 1,250
| 25,0
| 2,0
| 0,935
| |
| 21,62
| 0,40
| 0,995
| 50,0
| 1,0
| 0,748
| |
| 27,85
| 1,80
| 0,750
| 100,0
| 5,0
| 0,358
| |
| 23,75
| 1,10
| 0,825
| 50,0
| 4,5
| 0,577
| |
| 32,73
| 0,80
| 0,944
| 100,0
| 3,0
| 0,672
| |
| 13,35
| 0,50
| 1,280
| 50,0
| 2,5
| 0,780
|
91-120. Визначте вміст Х-йонів у розчині, якщо при фотометрируванні його розчинів на полум'яному фотометрі отримано такі дані:
| №
| Х-йон
| С,мкг/мл
| І,мкА
| №
| Х-йон
| С,мкг/мл
| І,мкА
| |
| Na+
| 10,5
| 30,5
|
| Li+
| 22,9
| 42,5
| | x
| 45,0
| x
| 53,8
| | 20,2
| 50,5
| 37,0
| 64,6
| |
| Ca2+
| 15,3
| 41,8
|
| Rb+
| 29,5
| 51,0
| | x
| 47,6
| x
| 58,1
| | 28,8
| 55,3
| 52,7
| 69,9
| |
| K+
| 27,2
| 29,2
|
| Cs+
| 12,0
| 44,5
| | x
| 36,5
| x
| 56,2
| | 31,4
| 38,9
| 27,3
| 72,6
| | №
| Х-йон
| С,мкг/мл
| І,мкА
| №
| Х-йон
| С,мкг/мл
| І,мкА
| |
| Ba2+
| 17,6
| 28,3
|
| Cs+
| 27,5
| 72,6
| | x
| 33,1
| x
| 76,1
| | 22,3
| 35,9
| 37,8
| 82,5
| |
| Sr2+
| 20,9
| 31,0
|
| Na+
| 17,3
| 44,5
| | x
| 39,3
| x
| 49,3
| | 38,0
| 53,8
| 25,5
| 57,7
| |
| K+
| 6,1
| 10,3
|
| Li+
| 12,3
| 22,5
| | x
| 15,4
| x
| 31,1
| | 19,6
| 23,5
| 17,6
| 35,6
| |
| Na+
| 25,0
| 57,7
|
| K+
| 35,4
| 47,3
| | x
| 69,3
| x
| 53,0
| | 34,5
| 71,3
| 42,9
| 64,5
| |
| Li+
| 37,8
| 64,6
|
| Na+
| 19,0
| 48,5
| | x
| 72,7
| x
| 55,0
| | 48,3
| 74,9
| 25,3
| 57,7
| |
| Ba2+
| 28,0
| 43,8
|
| Li+
| 22,2
| 42,5
| | x
| 51,4
| x
| 48,2
| | 39,4
| 57,4
| 46,9
| 70,4
| |
| Cs+
| 27,4
| 72,6
|
| Cs+
| 37,0
| 82,5
| | x
| 87,7
| x
| 84,8
| | 44,5
| 93,6
| 44,5
| 93,6
| |
| Ca2+
| 15,6
| 41,8
|
| Ba2+
| 22,1
| 35,9
| | x
| 53,5
| x
| 39,5
| | 30,6
| 58,9
| 28,6
| 43,8
| |
| Na+
| 44,5
| 88,0
|
| Rb+
| 15,5
| 32,7
| | x
| 90,3
| x
| 48,1
| | 51,5
| 94,6
| 52,0
| 69,9
| |
| K+
| 11,4
| 19,4
|
| Na+
| 34,5
| 71,3
| | x
| 21,6
| x
| 75,9
| | 18,3
| 25,0
| 44,5
| 88,0
| |
| Sr2+
| 8,1
| 15,7
|
| K+
| 10,3
| 17,3
| | x
| 18,9
| x
| 14,6
| | 20,0
| 31,0
| 18,3
| 25,0
| | №
| Х-йон
| С,мкг/мл
| І,мкА
| №
| Х-йон
| С,мкг/мл
| І,мкА
| |
| Li+
| 48,6
| 74,9
|
| Ca2+
| 10,7
| 33,7
| | x
| 79,7
| x
| 36,9
| | 55,5
| 84,5
| 28,3
| 55,3
|
121-150. Для люмінесцентного визначення вітаміну В2 у харчовому продукті методом добавок m г продукту розчинили і після обробки інтенсивність люмінесценції отриманого розчину виявилася I x. Після додавання стандартного розчину, що містить m 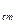 мкг вітаміну В2, інтенсивність люмінесценції збільшилася до мкг вітаміну В2, інтенсивність люмінесценції збільшилася до 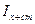 . Визначте масову частку вітаміну В2 у продукті, якщо інтенсивність люмінесценції холостого розчину склала I 0. . Визначте масову частку вітаміну В2 у продукті, якщо інтенсивність люмінесценції холостого розчину склала I 0.
| №
| m,г
| I x
| m 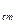 ,мкг ,мкг
| 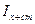
| I 0
| |
| 0,2002
| 23,5
| 15,0
| 45,7
| 5,5
| |
| 0,2342
| 25,3
| 16,3
| 52,6
| 4,0
| |
| 0,2743
| 35,2
| 27,9
| 66,2
| 8,2
| |
| 0,2062
| 24,8
| 36,4
| 48,3
| 2,7
| |
| 0,2212
| 27,5
| 28,7
| 56,7
| 7,3
| |
| 0,1902
| 15,0
| 36,0
| 34,0
| 5,8
| |
| 0,2129
| 25,3
| 23,0
| 55,8
| 3,3
| |
| 0,2251
| 26,7
| 27,3
| 63,9
| 8,1
| |
| 0,2843
| 37,9
| 44,4
| 74,3
| 2,0
| |
| 0,2745
| 35,4
| 36,7
| 83,0
| 7,8
| |
| 0,2694
| 33,3
| 25,8
| 74,3
| 9,4
| |
| 0,2072
| 24,8
| 25,0
| 57,5
| 3,0
| |
| 0,2322
| 25,8
| 30,9
| 68,6
| 10,1
| |
| 0,3102
| 42,8
| 37,5
| 83,9
| 4,6
| |
| 0,3632
| 52,0
| 40,5
| 94,0
| 6,3
| |
| 0,2902
| 36,7
| 40,7
| 78,9
| 2,9
| |
| 0,1725
| 20,3
| 26,0
| 53,2
| 8,3
| |
| 0,3642
| 53,7
| 24,5
| 83,1
| 5,8
| | №
| m,г
| I x
| m 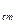 ,мкг ,мкг
| 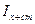
| I 0
| |
| 0,2478
| 28,9
| 39,4
| 67,5
| 6,3
| |
| 0,3831
| 54,6
| 37,4
| 88,4
| 8,5
| |
| 0,2235
| 26,2
| 36,9
| 68,5
| 9,6
| |
| 0,1628
| 18,9
| 17,0
| 36,2
| 10,8
| |
| 0,3689
| 55,4
| 27,5
| 92,4
| 6,4
| |
| 0,2844
| 32,9
| 38,0
| 71,5
| 5,3
| |
| 0,1721
| 21,5
| 42,5
| 76,8
| 3,8
| |
| 0,3378
| 38,4
| 36,2
| 81,0
| 7,0
| |
| 0,2156
| 24,7
| 27,4
| 45,6
| 6,2
| |
| 0,3200
| 47,0
| 22,0
| 75,2
| 8,5
| |
| 0,1604
| 24,1
| 15,6
| 42,8
| 4,4
| |
| 0,3645
| 48,5
| 25,4
| 89,3
| 3,0
|
До задач 151-180 потрібно побудувати графік.
151-165. Для визначення вмісту цукру в розчині приготували 3 наважки цукру масою m1, m2 і m3, перенесли в мірні колби місткістю 100 мл, довели до мітки дистильованою водою і ретельно перемішали. За допомогою рефрактометра визначили показник заломлення кожного розчину – n1, n2 і n3. Визначте масову частку цукру в досліджуваному розчині, якщо його коефіцієнт заломлення nх.
| №
| m1,г
| m2,г
| m3,г
| n1
| n2
| n3
| nх
| |
| 1,00
| 4,00
| 8,00
| 1,3331
| 1,3379
| 1,3445
| 1,3385
| |
| 1,00
| 5,00
| 10,00
| 1,3331
| 1,3396
| 1,3478
| 1,3368
| |
| 1,00
| 5,00
| 15,00
| 1,3331
| 1,3396
| 1,3552
| 1,3454
| |
| 2,00
| 4,00
| 8,00
| 1,3344
| 1,3379
| 1,3445
| 1,3559
| |
| 2,00
| 5,00
| 10,00
| 1,3344
| 1,3396
| 1,3478
| 1,3406
| |
| 2,00
| 5,00
| 15,00
| 1,3344
| 1,3396
| 1,3552
| 1,3516
| |
| 3,00
| 6,00
| 10,00
| 1,3364
| 1,3412
| 1,3478
| 1,3437
| |
| 3,00
| 6,00
| 12,00
| 1,3364
| 1,3412
| 1,3522
| 1,3492
| |
| 3,00
| 8,00
| 15,00
| 1,3364
| 1,3445
| 1,3552
| 1,3505
| |
| 4,00
| 8,00
| 15,00
| 1,3379
| 1,3445
| 1,3552
| 1,3415
| | №
| m1,г
| m2,г
| m3,г
| n1
| n2
| n3
| nх
| |
| 4,00
| 10,00
| 15,00
| 1,3379
| 1,3478
| 1,3552
| 1,3488
| |
| 4,00
| 10,00
| 20,00
| 1,3379
| 1,3478
| 1,3638
| 1,3606
| |
| 5,00
| 10,00
| 15,00
| 1,3396
| 1,3478
| 1,3552
| 1,3518
| |
| 5,00
| 10,00
| 20,00
| 1,3396
| 1,3478
| 1,3638
| 1,3578
| |
| 5,00
| 15,00
| 25,00
| 1,3396
| 1,3552
| 1,3736
| 1,3652
|
166-180. Для визначення вмісту глюкози в розчині приготували 3 наважки глюкози масою m1, m2 і m3, перенесли в мірні колби місткістю 100 мл, довели до мітки дистильованою водою і ретельно перемішали. За допомогою поляриметра визначили кут обертання кожного розчину – β1, β2 і β3. Визначте масову частку глюкози в досліджуваному розчині, якщо його кут обертання βх (за тих же умов).
| №
| m1,г
| m2,г
| m3,г
| β1,град
| β2,град
| β3,град
| βх,град
| |
| 1,00
| 4,00
| 8,00
| 0,53
| 2,10
| 4,20
| 1,56
| |
| 1,00
| 5,00
| 10,00
| 0,53
| 2,65
| 5,30
| 2,18
| |
| 1,00
| 5,00
| 15,00
| 0,53
| 2,65
| 7,95
| 3,15
| |
| 2,00
| 4,00
| 8,00
| 1,06
| 2,10
| 4,20
| 3,25
| |
| 2,00
| 5,00
| 10,00
| 1,06
| 2,65
| 5,30
| 2,34
| |
| 2,00
| 5,00
| 15,00
| 1,06
| 2,65
| 7,95
| 4,58
| |
| 3,00
| 6,00
| 10,00
| 1,54
| 3,18
| 5,30
| 4,86
| |
| 3,00
| 6,00
| 12,00
| 1,54
| 3,18
| 6,36
| 5,15
| |
| 3,00
| 8,00
| 15,00
| 1,54
| 4,20
| 7,95
| 5,45
| |
| 4,00
| 8,00
| 15,00
| 2,10
| 4,20
| 7,95
| 5,63
| |
| 4,00
| 10,00
| 15,00
| 2,10
| 5,30
| 7,95
| 5,86
| |
| 4,00
| 10,00
| 20,00
| 2,10
| 5,30
| 10,60
| 6,18
| |
| 5,00
| 10,00
| 15,00
| 2,65
| 5,30
| 7,95
| 6,43
| |
| 5,00
| 10,00
| 20,00
| 2,65
| 5,30
| 10,60
| 7,18
| |
| 5,00
| 15,00
| 25,00
| 2,65
| 7,95
| 13,25
| 9,58
|
181-210. Наважку сплаву m г розчинили в кислоті і після відповідної обробки довели об’єм розчину до V мл. Визначте масову частку срібла у сплаві, якщо дані потенціометричного титрування зі срібним електродом V1 мл досліджуваного розчину розчином натрій хлориду з молярною концентрацією СNaCl (моль/л) наступні *:
| №
| m,г
| V,мл
| V1, мл
| СNaCl,моль/л
| VNaCl,мл
| Е,мВ
| |
| 2,2893
| 100,0
| 25,0
| 0,1150
| 18,0
19,0
19,2
19,3
19,4
19,5
20,0
21,0
22,0
|
| |
| 1,9700
| 50,0
| 25,0
| 0,1500
| |
| 2,0130
| 100,0
| 10,0
| 0,1125
| |
| 2,5500
| 200,0
| 10,0
| 0,1225
| |
| 2,6750
| 250,0
| 25,0
| 0,1422
| |
| 1,8940
| 100,0
| 50,0
| 0,3350
| |
| 1,9552
| 200,0
| 50,0
| 0,2550
| |
| 2,0459
| 100,0
| 50,0
| 0,1450
| |
| 2,4873
| 200,0
| 100,0
| 0,2450
| 16,0
17,0
18,0
18,1
18,2
18,3
18,5
19,0
20,0
21,0
|
| |
| 2,3339
| 100,0
| 50,0
| 0,1595
| |
| 2,4312
| 100,0
| 25,0
| 0,2500
| |
| 2,2219
| 100,0
| 50,0
| 0,1998
| |
| 1,7549
| 50,0
| 10,0
| 0,1120
| |
| 1,9875
| 50,0
| 25,0
| 0,2675
| |
| 2,0045
| 100,0
| 25,0
| 0,2750
| |
| 2,4587
| 50,0
| 10,0
| 0,1154
| |
| 2,3126
| 100,0
| 50,0
| 0,3265
| |
| 1,4570
| 50,0
| 10,0
| 0,2598
| 13,0
14,0
14,1
14,2
14,3
14,5
15,0
16,0
|
| |
| 2,2035
| 100,0
| 25,0
| 0,3220
| |
| 2,2659
| 250,0
| 50,0
| 0,2375
| |
| 1,6398
| 50,0
| 10,0
| 0,2320
| |
| 2,0545
| 100,0
| 25,0
| 0,1364
| |
| 2,7387
| 200,0
| 50,0
| 0,1778
| |
| 1,5588
| 50,0
| 10,0
| 0,1840
| | №
| m,г
| V,мл
| V1, мл
| СNaCl,моль/л
| VNaCl,мл
| Е,мВ
| |
| 2,0325
| 100,0
| 50,0
| 0,2185
| 19,0
20,0
20,1
20,2
20,5
21,0
22,0
|
| |
| 2,4943
| 250,0
| 10,0
| 0,2940
| |
| 1,6843
| 200,0
| 100,0
| 0,1678
| |
| 2,0535
| 100,0
| 25,0
| 0,1222
| |
| 2,9321
| 50,0
| 50,0
| 0,2355
| |
| 1,9652
| 100,0
| 25,0
| 0,2210
|
* Для визначення еквівалентного об’єму побудуйте диференційний графік потенціометричного титрування в координатах ΔE/ΔVNaCl – VNaCl.
211-240. Кулонометричне титрування А моль натрій тіосульфату при силі струму І мА проводилось τ сек. Обчисліть відносну та абсолютну похибку цього вимірювання.
| №
| А,
10–5 моль
| І,мА
| τ,с
| №
| А,
10–5 моль
| І,мА
| τ,с
| |
| 4,40
|
|
|
| 4,10
|
|
| |
| 3,20
|
|
|
| 2,30
|
|
| |
| 5,00
|
|
|
| 1,50
|
|
| |
| 1,25
|
|
|
| 1,70
|
|
| |
| 3,90
|
|
|
| 2.40
|
|
| |
| 2,45
|
|
|
| 3,90
|
|
| |
| 5,60
|
|
|
| 5,40
|
|
| |
| 3,45
|
|
|
| 2,38
|
|
| |
| 1,65
|
|
|
| 4,10
|
|
| |
| 3,60
|
|
|
| 3,50
|
|
| |
| 2,70
|
|
|
| 2,70
|
|
| |
| 1,35
|
|
|
| 2,45
|
|
| |
| 1,00
|
|
|
| 2,70
|
|
| |
| 3,50
|
|
|
| 3,40
|
|
| |
| 4,20
|
|
|
| 4,00
|
|
|
241-270. При полярографічному аналізі деякої сполуки, що відновлюється необоротно з витратою одного електрону (z = 1), спостерігався (максимальний) дифузійний струм Іd при молярній концентрації розчину сM. Період крапання ртутного крапельного електроду t, а швидкість витікання ртуті m за 1 с. Визначте концентрацію розчину сM (моль/л), якщо коефіцієнт дифузії становить D.
| №
| Іd,мкА
| t,с
| m,
мг
| D,
10-5 см2/с
| №
| Іd,мкА
| t,с
| m,
мг
| D,
10-5 см2/с
| |
| 3,10
| 3,53
| 1,26
| 1,2
|
| 3,90
| 3,08
| 1,12
| 0,8
| |
| 3,25
| 2,14
| 1,08
| 1,1
|
| 4,05
| 2,64
| 1,16
| 1,3
| |
| 3,40
| 3,08
| 1,34
| 1,3
|
| 4,20
| 2,25
| 1,56
| 1,4
| |
| 3,55
| 2,64
| 1,56
| 1,4
|
| 3,10
| 3,36
| 1,85
| 0,9
| |
| 3,70
| 2,25
| 1,85
| 0,9
|
| 3,25
| 2,14
| 1,12
| 1,2
| |
| 3,80
| 3,36
| 1,12
| 0,8
|
| 3,40
| 3,53
| 1,16
| 1,1
| |
| 3,90
| 2,14
| 1,16
| 1,3
|
| 3,70
| 2,14
| 1,26
| 1,3
| |
| 4,05
| 3,08
| 1,56
| 1,4
|
| 3,80
| 3,08
| 1,08
| 1,4
| |
| 4,20
| 2,64
| 1,85
| 0,9
|
| 3,90
| 2,64
| 1,34
| 1,1
| |
| 4,35
| 2,25
| 1,12
| 1,2
|
| 4,05
| 3,53
| 1,26
| 1,3
| |
| 4,50
| 2,14
| 1,16
| 1,1
|
| 3,70
| 2,14
| 1,85
| 1,4
| |
| 4,65
| 3,08
| 1,56
| 1,3
|
| 4,65
| 3,08
| 1,12
| 0,9
| |
| 4,80
| 2,64
| 1,85
| 1,4
|
| 4,80
| 3,53
| 1,16
| 0,8
| |
| 4,95
| 3,53
| 1,26
| 1,2
|
| 4,95
| 2,14
| 1,56
| 1,3
| |
| 5,05
| 2,14
| 1,08
| 0,9
|
| 4,65
| 3,08
| 1,85
| 1,4
|
КОНТРОЛЬ ВИКОНАННЯ
САМОСТІЙНОЇ РОБОТИ СТУДЕНТАМИ
Засвоєння матеріалу контролюється засобом модульного контролю (табл. 3). Планується 2 модулі при вивченні дисципліни. Кожний модуль містить тест та контрольне завдання, яке обов’язково містить розрахункові задачі.
Контроль знань студентів денної форми навчання
Таблиця 3
Розподіл балів, що присвоюються студенту з дисципліни «Аналітична хімія»
| № з/п
| Вид роботи
| Змістовий модуль 1
| Змістовий модуль 2
| | 1.
| Захист
лабораторних
робіт
| лаб. роб. 1
|
| лаб. роб. 5
|
| | лаб. роб. 6
|
| | лаб. роб. 2
|
| лаб. роб. 7
|
| | лаб. роб. 8
|
| | лаб. роб. 3
|
| лаб. роб. 9
|
| | лаб. роб. 4
|
| лаб. роб. 10
|
| |
| Самостійна і індивідуальна робота
| ДІЗ №1 (літ.6)
|
| ДІЗ № 2(літ.6)
|
| |
| Виконання модульної контрольної роботи
| Тест (30х0,4)
|
| Тест(30х0,4)
|
| | Контрольне завдання (7х3)
|
| Контрольне завдання(6х3)
|
| |
| Творче завдання
| | | |
| | Разом
| |
| |
|
МОДУЛЬ № 1
|


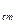 мкг вітаміну В2, інтенсивність люмінесценції збільшилася до
мкг вітаміну В2, інтенсивність люмінесценції збільшилася до 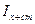 . Визначте масову частку вітаміну В2 у продукті, якщо інтенсивність люмінесценції холостого розчину склала I 0.
. Визначте масову частку вітаміну В2 у продукті, якщо інтенсивність люмінесценції холостого розчину склала I 0.


