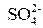Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Параметры качества природной воды и методы их контроля
Качество природной воды характеризуются следующими параметрами: 1) Содержанием грубодисперсных примесей (частиц песка, глины и др.), определяемых фильтрованием через бумагу с последующим взвешиванием. 2) Мутностью, которая зависит от присутствия в воде взвешенных и коллоидных веществ различного происхождения: взвешенного ила (сложная смесь твердых органических и минеральных веществ), органических коллоидов гидроксида железа и алюминия, микроорганизмов, фито- и зоопланктонов и т. д.Мутность определяется фотометрическим методом в зелёной части спектра, путем сравнения с образцами, замутненными стандартной взвесью каолина. Применяется также метод определения прозрачности (величины обратной мутности) которая определяется толщиной слоя воды через который просматривается стандартный шрифт. 3) Цветностью, обусловливаемой в основном растворенными в воде гуминовыми веществами, вымываемыми из торфяных болот и комплексных соединений трехвалентного железа. Цветность определяется фотометрическим методом с синим светофильтром, она измеряется в градусах цветности платинокобальтовой или хромокобальтовой шкал (от 0 до 70°). 4) Вкусом и привкусом которые зависят от присутствия в воде веществ природного происхождения или веществ, которые попадают в воду со сточными промышленными и хозяйственно-бытовыми водами. Подземные воды имеют специфический вкус, который вызван наличием железа, марганца, магния, натрия, калия, хлоридов и карбонатов; Различают 4 основных вкуса: соленый, кислый, сладкий, горький. Все другие виды вкусовых ощущений называются привкусами: хлорный, рыбный; металлический. Характер и интенсивность вкуса и привкуса определяют с помощью органолептических методов. Исследуемую воду набирают в рот малыми порциями, не проглатывают, задерживая 3–5 с, а затем сплевывают. Интенсивность вкуса и привкуса определяют при 20°C и оценивают по 5-балльной шкале. 5) Запахом, который обусловлен наличием в воде летучих пахнущих веществ естественного и искусственного происхождения. Запах воды определяют в помещении, где воздух не имеет постороннего запаха. Для исключения субъективной ошибки целесообразно анализ производить в группе из 3–5 человек. Интенсивность запаха также оценивается по 5-балльной шкале.
6) Окисляемостью, обусловленной наличием в воде легко окисляющихся органических примесей. Количественно окисляемостьхарактеризуется количеством мг кислорода, эквивалентным количеству окислителя, необходимого для окисления органических примесей, содержащихся в 1 дм3 воды. Окисляемость определяется титрованием воды растворами перманганата или бихромата калия. Соответственно различают перманганатную и хроматную окисляемость. Для питьевой воды, чистых подпочвенных, родниковых и поверхностных источников, окисляемость не превышает 5–10мг/дм3. 7) Показателем pH, который у большинства природных вод равен 6,6–8,6. Величина pH обусловлена наличием в воде карбонатов, гидроксидов, солей, подверженных гидролизу, гуминовых веществ и т. д. При выпадении pH воды определяется потенциометрическим методом с использованием в качестве индикаторного стеклянного электрода. 8) Щелочностью, которая определяется как сумма эквивалентных концентраций анионов слабых кислот ( 9) Жесткостью. Совокупное определение содержания ионов Ca2+ и Mg2+ производится комплексонометрическим титрованием трилоном Б. 10) Сухим остатком – характеризующим общее содержание растворенных в воде минеральных и частично органических веществ, температура кипения которых превышает 110°C, нелетучих и неразлагающихся при указанной температуре. Величина сухого остатка выражается в мг/дм3. 11) Общим солесодержанием – суммарной концентрацией растворенных в воде минеральных солей, рассчитанной по данным отдельных определений. 12) Содержанием ионов 13) Содержанием железа. Ионы железа Fe3+ гидролизуясь, образуют коллоидную гидроокись железа Fe(OH)3, коагулирующуюся в виде хлопьевидной суспензии. В присутствии гуминовых веществ могут образоваться стойкие гуминовокислые соединения железа. Определение общего содержания железа производится колориметрическим методом с роданидом аммония. 14) Количеством растворенных газов: O2, N2, CO2, и H2S, поглощаемых водой при ее выпадении в виде атмосферных осадков, а также при проникновении их в почву. Одним из источников поступления O2 в воду является фотосинтез, а CO2 – окисление органических примесей в поверхностных водах.
15) Содержанием токсических неорганических веществ в частности ионов меди, свинца, мышьяка, ртути и др. Определение содержания каждого из этих ионов производится по отдельным методикам с использованием методов химического и физикохимического анализа. 16) Количеством микроорганизмов (бактерии, грибы, водоросли), а также патогенных микробов и вирусов. Определение производится микробиологическими методами. 17) Содержанием токсических органических веществ искусственного происхождения – пестицидов, ароматических, гетероциклических соединений и др. 18) Уровнем радиоактивности. Обычно производится измерение общей радиоактивности в a-, b- и g-диапазонах. При необходимости может быть произведено отдельное определение содержания радиоактивных изотопов цезия-137, стронция-90, иттрия-90 и др.
Качество питьевой воды. Водоподготовка Вода, применяемая в пищевых целях – непосредственно для питья, для приготовления пищи, для мытья продуктов питания – должна строго соответствовать требованиям соответствующих ГОСТов (ГОСТ 2761–57 и 2874–54). Питьевая вода должна быть безопасна по бактериальному составу, безвредна и не должна обладать неприятными органолептическими свойствами. Требования, предъявляемые к питьевой воде приведены в таблицах 4.1.– 4.3. Таблица 4.1. Общие свойства питьевой воды
Таблица 4.2. Предельно допустимые нормы содержания некоторых ионов в питьевой воде, мг/дм3
Таблица 4.3. Бактериальная характеристика питьевой воды
Если качество воды в источнике не удовлетворяет санитарно-гигиеническим требованиям, предъявляемым к питьевой воде, то недостатки устраняют обработкой воды на очистных сооружениях перед подачей потребителям. Процесс водоподготовки питьевой воды включает следующие стадии: 1) Осветление и обесцвечивание забираемой из водоема воды производится пропусканием ее через решетки и сита для задержания листьев, водорослей и прочих механических примесей. Затем добавляют коагулянты (A12(SO4)3, Fe2(SO4)3, FeCl3 и др.) для осаждения содержащейся в природной воде взвеси и коллоидных веществ. Образовавшийся осадок задерживается в отстойниках или осветлителях. Из отстойников или осветлителей вода для окончательного освобождения от взвеси направляется на фильтры, где фильтруется через слой песка или антрацита и песка. Осветленная вода направляется в резервуар чистой воды.
2) Обеззараживание воды достигается ее хлорированием (обработка хлорной известью или молекулярным хлором). Кроме того, применяется озонирование и облучение бактерицидными лучами. Для предотвращения образования хлорфенольных привкусов (при наличии в исходной воде примеси фенолов) и удлинения срока действия хлора в воду вводится аммиак, образующий с хлором хлорамины. Избыток хлора в обработанной воде может быть удален сернистым газом. Хлорированная вода обязательно подвергается анализу на активный хлор. Анализ производится иодометрическим методом. Содержание активного хлора в воде, подаваемой потребителю должно быть не менее 0,3 мг/дм3, но не более 0,5 мг/дм3,хлорфенольные запахи должны отсутствовать. К обеззараживанию питьевой воды приводит также её кипячение непосредственно перед применением. 3) Обезжелезивание воды осуществляется путем аэрации (окисление двухвалентного железа в трехвалентное), хлорирования (окисление или разрушение органических коллоидов), коагуляции (удаление коллоидов и взвеси) и известкования (повышение pH) с последующим осветлением воды. 4) Дегазация воды (удаление H2S, CO2) достигается, как правило, путём интенсивной аэрации. 5) Дезодорация воды (удаление привкусов и запахов) проводится введением аммиака перед хлорированием, хлорированием повышенными дозами, обработкой порошком активного угля. 6) Фторирование. При недостатке в вода фтора его добавляют в виде раствора фтористых солей (например, Na2SiF6). Избыток фтора может быть удален пропусканием воды через взвешенный слой Mg(OH)2, образующий с фтором малорастворимое соединение, или фильтрацией через слой активной гидроокиси алюминия или синтетического гидроаппатита. 7) Опреснения воды можно достигнуть методами ионного обмена, термическим, электрохимическим и др. 8) Умягчение питьевой воды достигается путём её обработки кальцинированной содой или гашеной известью. Для снабжения питьевой водой могут использоваться лишь источники, которые имеют зону санитарной охраны или могут быть ею обеспечены. Методика проведения работы
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-25; просмотров: 253; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.217.228.35 (0.012 с.) |
 гуматов).
гуматов).
 . Определение содержания каждого из этих ионов производится по индивидуальным методикам.
. Определение содержания каждого из этих ионов производится по индивидуальным методикам.