
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Аденилосукцинат Ксантинмонофосфат
АМФ+Фн глутамат
АДФ
АДФ
АТФ ГТФ
Синтез пуриновых нуклеотидов регулируется ключевыми ферментами, активность которых зависит от концентрации конечных и некоторых промежуточных продуктов, т.е. при контроле синтеза реализуется один из механизмов - регуляция по принципу отрицательной обратной связи: 1) АТФ, ГМФ ингибируют образование ФРПФ (угнетают активность 5–фосфорибозил–1–пирофосфатсинтазы); 2) ИМФ, АМФ, ГМФ – ингибируют образование фосфорибозиламина - это наиболее важный пункт контроля (угнетают активность глутамин–ФРПФ–амидотрансферазы);3) АМФ ингибирует образование аденилосукцината, который является промежуточным продуктом его синтеза, а ГМФ- ксантинмонофосфата;4) АМФ ингибирует образование ксантинмонофосфата при синтезе ГМФ, а ГМФ, в свою очередь, угнетает образование аденилосукцината, который является промежуточным продуктом синтеза АМФ. Т.о. изменения концентрации АМФ влияют на синтез ГМФ и наоборот;5) АТФ может активировать процессы синтеза ГМФ также на этапе образования ксантинмонофосфата, а ГТФ - активировать образование аденилосукцината. 16. Біосинтез піримідинових нуклеотидів: схема реакцій; регуляція синтезу. Синтез пиримидиновых нуклеотидов начинается со сборки кольца азотистого основания, которое затем присоединяется к рибозо-5-фосфату. Донором является ФРПФ. Предшественниками пиримидинового кольца служат карбамоилфосфат и аспартат. Синтез начинается с образования карбамоилфосфата, который синтезируется в цитозоле. Донором азота при синтезе карбомаилфосфата является глутамин.. Реакцию катализирует карбомаилфосфатсинтаза ІІ: Глутамин + 2 АТФ + СО2 ® карбамоилфосфат + 2 АДФ + Фн+ глутамат. Следующий этап – образование N–карбамоиласпартата.(фермент – аспартат–карбамоилтрансфераза – АТКаза)
COOH COOH Аспартат N–карбамоиласпартата
В следующей последовательности реакций образуется предшественник всех пиримидиновых нуклеотидов - УМФ:
дигидрооротаза
НАД оротат– НАДН++ Н дегидроге–
наза Оротат
фосфо– ФФн рибозил– транс– фераза ОМФ
Н+ декарбокси– СО2 лаза
УМФ С участием молекул АТФ под действием специфических киназ (УМФ–киназа, нуклеозид–фосфаткиназа) УМФ превращается в УТФ. УТФ служит предшественником ЦТФ:
глутамин + глутамат + АТФ + Н2О АДФ + Фн+ 2Н+
Регуляция синтеза пуриновых нуклеотидов. Ключевыми ферментами процесса являются карбамоилфосфатсинтаза II (1) и АТКаза (2), схема регуляции которых изображена ниже: (1)
УМФ, УТФ (2) ЦТФ
ЦТФ
В регуляции 2 реакция – решающий этап. ЦТФ значительно снижает сродство фермента АТКазы к субстрату (степень ингибирования до 90%). Активация этого фермента происходит под действием АТФ, что позволяет координировать скорости образования пуринов и пиримидинов.
17. Біосинтез дезоксирибонуклеотидів. Утворення тимідилових нуклеотидів; інгібітори біосинтезу дТМФ як протипухлинні засоби. Дезоксирибонуклеотиды образуются из рибонук–леотиддифосфатов путем их восстановления во 2'–положении. Фермент, который катализирует эту реакцию, – рибонуклеозидредуктаза (рибонуклеотиддифосфатредук–таза). Общая реакция: Рибонуклеозиддифосфат + НАДФН+Н+ ® дезоксири–бонуклеозиддифосфат + НАДФ+ + Н2О Электроны при восстановлении переносятся на субстрат через ряд сульфгидрильных групп, для этого в реакции участвует тиоредоксин (белок с близко расположенными SH-группами). При переносе электронов происходит окисление тиоредоксина. После реакции образования дезоксирибонуклеозиддифосфата он восстанавливается с участием НАДФН под действием тиоредоксинредуктазы
S SH Образование тимидиновых нуклеотидов (ТМФ) происходит из УМФ: УДФ
тимидилатсинтаза
Далее происходит восстановление дигидрофолевой кислоты (ДГФК) до тетрагидрофолевой кислоты (ТГФК) под действием дигидрофолатредуктазы:
НАДФН НАДФ
После образования дТМФ с участием АТФ происходит последующий синтез всех остальных тиминовых нуклеотидов:
АТФ АДФ АТФ АДФ Основной механизм контроля синтеза - аллостерическая регуляция. Ключевой фермент – рибонуклеозидредуктаза. При синтезе дАТФ ингибитор этого фермента – дАТФ (конечный продукт), активатор – АТФ.Если синтезируется дТТФ, то в регуляции процесса также реализуется принцип отрицательной обратной связи. Т.е. рибонуклеотидредуктаза имеет несколько конформацион–ных состояний, что обеспечивает синтез достаточного количества всех четырех дезоксирибонуклеотидов. 18. Катаболізм пуринових нуклеотидів; спадкові порушення обміну сечової кислоти. Схема катаболізму піримідинових нуклеотидів. В организме человека нет ферментов, необходимых для разрыва пуринового кольца. Потому избыток пуринов выводится из организма человека неразрушенным, в виде мочевой кислоты. В печени свободные пуриновые основания (экзогенного и эндогенного происхождения) подвергаются дезаминированию с образованием ксантина и гипоксантина.
рибозо-ф
ксантин
Мочевая кислота за сутки образуется до 1,5 г мочевой кислоты, которая выводится в основном с мочой. 60% этого количества образуется при катаболизме эндо–генных пуринов, остальная – пуринов пищи. В сыворотке крови концентрация мочевой кислоты, которая находится в виде солей - уратов (на 98% с Na), – 0,18–0,42 ммоль/л. Ураты выводятся на 2/3 почками и на 1/3 через тонкий кишечник. Соли мочевой кислоты в крови не кристаллизуются. В тканях и моче ураты кристаллизуются при меньших концентрациях. Наибольшее сродство к уратам имеют хрящевая ткань и почки.Главный клинический синдром нарушения пуринового обмена – подагра. Для лечения - аллопуринол - структурный аналог гипоксантина, который ингибирует ксантиноксидазу. Для повышения экскреции уратов назначают также пробенецид. синдром Леша–Нихана. наследственное заболевание- дефект одного из ферментов реутилизации пуриновых азотистых оснований - гипоксантин-гуанинфосфорибозилтрансферазы. У больных детей наблюдаются симптомы подагры, церебральные параличи, нарушения интеллекта, попытки наносить себе увечья (укусы губ, пальцев). Катаболизм пиримидиновых нуклеотидов.. Сначала происходит расщепление нуклеотидов до азотистых оснований с последующей их деградацией до b-аланина, b-аминоизобутирата, СО2 и NH3: дТМФ ® Тимидин ® Тимин
СО2, NH3 b–аминоизобутират
Цитозин® Урацил
b-аланин метилмалонил-КоА
Таким образом, конечными продуктами расщепления пиримидиновых нуклеотидов являются: b-аланин, b-аминоизобутират, СО2 и NH3. СО2 и NH3 идут на синтез мочевины, а b-аминоизобутират может метаболизировать аналогично аминокислотам с разветвленной цепью.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 130; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.205.186 (0.037 с.) |
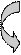



 АТФ глутамин -
АТФ глутамин -
 Фумарат
Фумарат

 АМФ ГМФ
АМФ ГМФ
 АТФ АТФ
АТФ АТФ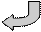
 2 АДФ ГДФ
2 АДФ ГДФ
 АТФ
АТФ
 H2N-CО-O-PO3H2 + H2N-CH-COOH H2N-CО-NH-CH- СООН
H2N-CО-O-PO3H2 + H2N-CH-COOH H2N-CО-NH-CH- СООН к арбамоилфосфат - Фн
к арбамоилфосфат - Фн
 CH2 CH2
CH2 CH2 Н2О
Н2О
 N–карбамоиласпартат Дигидрооротат
N–карбамоиласпартат Дигидрооротат дигидро–
дигидро–
 ФРПФ оротат–
ФРПФ оротат– оротидилат–
оротидилат–
 УТФ ЦТФ
УТФ ЦТФ

 СО2 + глутамин + 2АТФ карбамоилфосфат
СО2 + глутамин + 2АТФ карбамоилфосфат аспартат
аспартат карбамоиласпартат
карбамоиласпартат
 УМФ
УМФ УТФ
УТФ S SH
S SH

 Тиоредоксин + НАДФН+Н+ ® тиоредоксин + НАДФ
Тиоредоксин + НАДФН+Н+ ® тиоредоксин + НАДФ Фн ТГФК ДГФК
Фн ТГФК ДГФК

 дУДФ дУМФ дТМФ
дУДФ дУМФ дТМФ
 ДГФК ТГФК
ДГФК ТГФК

 дТМФ дТДФ дТТФ
дТМФ дТДФ дТТФ


 Гуанин ИМФ
Гуанин ИМФ рибозо-ф
рибозо-ф гипоксантин
гипоксантин


 метилмалонат
метилмалонат


 ЦЛК сукцинил-КоА
ЦЛК сукцинил-КоА


