Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение и номенклатура основных пуриновых и пиримидиновых нуклеотидов. Роль свободных нуклеотидов.Стр 1 из 6Следующая ⇒
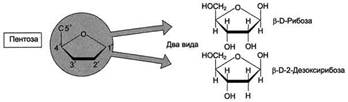
Строение и номенклатура основных пуриновых и пиримидиновых нуклеотидов. Роль свободных нуклеотидов. Каждый нуклеотид содержит 3 химически различных компонента: гетероциклическое азотистое основание, моносахарид (пентозу) и остаток фосфорной кислоты. В зависимости от числа имеющихся в молекуле остатков фосфорной кислоты различают нуклеозидмонофосфаты (НМФ), нуклеозиддифосфаты (НДФ), нуклео-зидтрифосфаты (НТФ). В состав нуклеиновых кислот входят азотистые основания двух типов: пуриновые - аденин (А), гуанин (G) и пиримидиновые - цитозин (С), тимин (Т) и урацил (U). Нумерация атомов в основаниях записывается внутри цикла. Пентозы в нуклеотидах представлены либо рибозой (в составе РНК), либо дезоксирибозой (в составе ДНК). Пентозу соединяет с основанием N-гликозидная связь, образованная С1-атомом пентозы (рибозы или дезоксирибозы) и N1 -атомом пиримидина или N9-aтомом пурина (рис. 4-4). Нуклеотиды, в которых пентоза представлена рибозой, называют рибонуклеотидами, а нуклеиновые кислоты, построенные из рибонуклеотидов, - рибонуклеиновыми кислотами, или РНК. Нуклеиновые кислоты, в мономеры которых входит дезоксирибоза, называют дезоксири-бонуклеиновыми кислотами, или ДНК. Нуклеиновые кислоты по своему строению относят к классу линейных полимеров. Остов нуклеиновой кислоты имеет одинаковое строение по всей длине молекулы и состоит из чередующихся групп - пентоза-фосфат-пентоза- (рис. 4-5). Вариабельными группами в полинуклеотидных цепях служат азотистые основания - пурины и пиримидины. В молекулы РНК входят аденин (А), урацил (U), гуанин (G) и цитозин (С), в ДНК - аденин (А), тимин (Т), гуанин (G) и цитозин (С). Уникальность структуры и функциональная индивидуальность молекул ДНК и РНК определяются их первичной структурой -последовательностью азотистых оснований в полинуклеотидной цепи.
Рис. 4-4. Пуриновый и пиримидиновый нуклеотиды. Свободные нуклеотиды, в частности АТФ, цАМФ, АДФ, играют важную роль в энергетических и информационных внутриклеточных процессах, а также являются составляющими частями нуклеиновых кислот и многих коферментов.
Основные типы РНК В цитоплазме клеток присутствуют 3 типа рибонуклеиновых кислот - транспортные РНК (тРНК), матричные РНК (мРНК) и рибосомальные РНК (рРНК). Они различаются по первичной структуре, молекулярной массе, конфор-мации, продолжительности жизни и, самое главное, по функциональной активности.
Рис. 10-9. Катаболизм пуриновых нуклеотидов до мочевой кислоты.
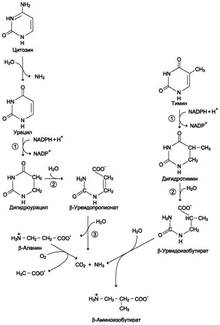
Рис. 10-16. Катаболизм пиримидиновых оснований. Рис. 10-11. Строение аллопуринола и гипоксантина. Аллопуринол оказывает двоякое действие на обмен пуриновых нуклеотидов: · ингибирует ксантиноксидазу и останавливает катаболизм пуринов на стадии образования гипоксантина, растворимость которого почти в 10 раз выше, чем мочевой кислоты. Действие препарата на фермент объясняется тем, что сначала он, подобно гипоксанти-ну, окисляется в гидроксипуринол, но при этом остаётся прочно связанным с активным центром фермента, вызывая его инактивацию; · с другой стороны, будучи псевдосубстратом, аллопуринол может превращаться в нуклеотид по "запасному" пути и ингибировать ФРДФ синтетазу и амидофосфорибозилтрансферазу, вызывая торможение синтеза пуринов de novo. При лечении аллопуринолом детей с синдромом Лёша-Нихена удаётся предотвратить развитие патологических изменений в суставах и почках, вызванных гиперпродукцией мочевой кислоты, но препарат не излечивает аномалии в поведении, неврологические и психические расстройства. 8. Ферменты синтеза рибо- и дезоксирибонуклеотидов как мишени действия противовирусных и противоопухолевых препаратов. Синтезировано очень много аналогов дНТФ, которые включаются ДНК полимеразами в ДНК и ингибируют репликацию. К числу мощных противоопухолевых препаратов принадлежит 5-фторурацил (5-FU) - аналог урацила. В организме по "запасным" путям 5-FU превращается в 5-Р-УМФ либо в реакции, катализируемой оротатфосфорибозилтрансферазой, либо через промежуточное образование нуклеозида и последующее фосфорилирование. Превращаясь в нуклеозиддифосфат, 5-FU может участвовать в реакции, катализируемой РНР, и восстанавливаться в соответствующее дезоксипроизводное. Под действием фосфатазы 5-Р-дУДФ снова теряет фосфат, и образующийся 5-Р-дУМФ связывается с тимидилатсинтазой и N5, N10-метилен-Н4-фолатом, образуя комплекс, напоминающий промежуточное соединение в реакции превращения дУМФ в дТМФ. Тимидилатсинтаза оказывается полностью блокированной, и синтез дТМФ прекращается: Цитозинарабинозид (или цитарабин) представляет собой соединение, в котором остаток ри-бозы замещён на стериоизомер - арабинозу. Оно используется в химиотерапии рака, в частности, при острой миелоцитарной лейкемии. В организме препарат может превращаться в дНТФ, ингибировать ДНК полимеразы и снижать скорость репликации. Аналоги фолиевой кислоты. В обмене нуклеотидов производные Н4-фолата как доноры од-ноуглеродных групп участвуют в формировании пуринового гетероциклического кольца и в ключевой реакции синтеза дТМФ из дУМФ, катализируемой тимидилатсинтазой. В последнем случае N5,N10-метилен-Н4-фолат служит донором метальной группы и в ходе реакции превращается в Н2-фолат. Для активного синтеза тимидиловых нуклеотидов Н2-фолат должен повторно использоваться, проходя стадию восстановления в Н4-фолат (см. формулу ниже). Метотрексат и аминоптерин - структурные аналоги фолиевой кислоты - ингибируют дигидрофолатредуктазу и таким образом нарушают синтез пуриновых нуклеотидов и превращение дУМФ в дТМФ, снижая внутриклеточную концентрацию субстратов синтеза ДНК и РНК. Препараты широко используют в химиотерапии опухолей. Б. Антивирусные и антибактериальные препараты. Азидотимидин (AZT, или зидовидин) представляет собой мощный противовирусный препарат, применяющийся в лечении инфекций, которые сопровождают приобретённые формы иммунодефицита. Будучи структурным аналогом тимиди-на, препарат имеет в З'-положении дезоксирибозы азидогруппу AZT может фосфорилироваться и с помощью ДНК-полимераз включаться в растущую молекулу ДНК. Однако присутствие в 3'-положении дезоксирибозы азидогруппы делает синтезирующиеся молекулы ДНК не способными к последующему удлинению. В результате образование новых молекул ДНК прекращается. Важно, что фосфорилированные производные AZT утилизируются более эффективно вирусной ДНК-полимеразой или так называемой обратной транскриптазой, чем ДНК-полимеразами эукариотов, поэтому препарат наиболее эффективно влияет на размножение вирусов и, в частности, ретровируса, вызывающего ВИЧ-инфекцию. 5-йоддезоксиуридин используют в терапии кератитов и поражений роговицы глаза вирусом герпеса. Азатиоприн в организме превращается в 6-меркаптопурин, который оказывает мощное иммуносупрессорное действие. Препарат широко используют в трансплантологии для предотвращения развития иммунологических реакций, вызывающих отторжение трансплантата.
9. Структурная организация нуклеиновых кислот. Структура ДНК и РНК.Строение нуклеотидов Каждый нуклеотид содержит 3 химически различных компонента: гетероциклическое азотистое основание, моносахарид (пентозу) и остаток фосфорной кислоты. В зависимости от числа имеющихся в молекуле остатков фосфорной кислоты различают нуклеозидмонофосфаты (НМФ), нуклеозиддифосфаты (НДФ), нуклео-зидтрифосфаты (НТФ) В состав нуклеиновых кислот входят азотистые основания двух типов: пуриновые - аденин (А), гуанин (G) и пиримидиновые - цитозин (С), тимин (Т) и урацил (U). Нумерация атомов в основаниях записывается внутри цикла (рис. 4-2). Номенклатура нуклеотидов приведена в табл. 4-1. Пентозы в нуклеотидах представлены либо рибозой (в составе РНК), либо дезоксирибозой (в составе ДНК). Первичная структура ДНК -порядок чередования дезоксирибонуклеозидмонофосфатов (дНМФ) в полинукпеотидной цепи. Каждая фосфатная группа в полинукпеотидной цепи, за исключением фосфорного остатка на 5'-конце молекулы, участвует в образовании двух эфирных связей с участием 3'- и 5'-углеродных атомов двух соседних дезоксирибоз, поэтому связь между мономерами обозначают 3', 5'-фосфодиэфирной. Концевые нуклеотиды ДНК различают по структуре: на 5'-конце находится фосфатная группа, а на 3'-конце цепи - свободная ОН-группа. Эти концы называют 5'- и 3'-концами.. В каждом мономере нуклеиновой кислоты присутствует остаток фосфорной кислоты.Азотистые основания почти нерастворимы в воде, но некоторые атомы пуринового и пиримидинового циклов способны образовывать водородные связи. Вторичная структура ДНК. В 1953 г. Дж. Уотсоном и Ф. Криком была предложена модель пространственной структуры ДНК. Согласно этой модели, молекула ДНК имеет форму спирали, образованную двумя полинуклеотидными цепями, закрученными относительно друг друга и вокруг общей оси. Двойная спираль правозакрученная, полинуклеотидньхе цепи в ней антипараллельны (рис. 4-6), т.е. если одна из них ориентирована в направлении 3'→5', то вторая - в направлении 5'→3'. Поэтому на каждом из концов молекулы ДНК расположены 5'-конец одной цепи и 3'-конец другой цепи. Комплементарые основания уложены в стопку в сердцевине спирали. Между основаниями двухцепочечной молекулы в стопке возникают гидрофобные взаимодействия, стабилизирующие двойную спираль. Такая структура исключает контакт азотистых остатков с водой. Третичная структура ДНК (суперспирализация ДНК) Каждая молекула ДНК упакована в отдельную хромосому. В диплоидных клетках человека содержится 46 хромосом. Общая длина ДНК всех хромосом клетки составляет 1,74 м, но она упакована в ядре, диаметр которого в миллионы раз меньше. Чтобы расположить ДНК в ядре клетки, должна быть сформирована очень компактная структура. Компактизация и суперспирализация ДНК осуществляются с помощью разнообразных белков, взаимодействующих с определёнными последовательностями в структуре ДНК. Все связывающиеся с ДНК эукариотов белки можно разделить на 2 группы: гисгоновые и негистоновые белки. Комплекс белков с ядерной ДНК клеток называют хроматином. Первичная структура РНК -порядок чередования рибонуклеозидмонофосфатов (НМФ) в полинуклеотидной. цепи. В РНК, как и в ДНК, нук-леотиды связаны между собой 3',5'-фосфодиэфирными связями. Концы полинуклеотидных цепей РНК неодинаковы. На одном конце находится фосфорилированная ОН-группа 5'-углеродного атома, на другом конце - ОН-группа 3'-углеродного атома рибозы, поэтому концы называют 5'- и 3'-концами цепи РНК. Гидроксильная группа у 2'-углеродного атома рибозы делает молекулу РНК нестабильной. Так, в слабощелочной среде молекулы РНК гидролизуются даже при нормальной температуре, тогда как структура цепи ДНК не изменяется. Вторичная структура РНК Молекула рибонуклеиновой кислоты построена из одной полинуклеотидной цепи. Отдельные участки цепи РНК образуют спирализованные петли - "шпильки", за счёт водородных связей между комплементарными азотистыми основаниями A-U и G-C. Участки цепи РНК в таких спиральных структурах антипараллельны, но не всегда полностью комплементарны, в них встречаются неспаренные нуклеотидные остатки или даже одноцепочечные петли, не вписьюающиеся в двойную спираль. Наличие спирализованных участков характерно для всех типов РНК. Третичная структура РНК Одноцепочечные РНК характеризуются компактной и упорядоченной третичной структурой, возникающей путём взаимодействия спирализованных элементов вторичной структуры. Так, возможно образование дополнительных водородных связей между нуклеотидными остатками, достаточно удалёнными друг от друга, или связей между ОН-группами остатков рибо-зы и основаниями. Третичная структура РНК стабилизирована ионами двухвалентных металлов, например ионами Mg2+, связывающимися не только с фосфатными группами, но и с основаниями. Основные типы РНК В цитоплазме клеток присутствуют 3 типа рибонуклеиновых кислот - транспортные РНК (тРНК), матричные РНК (мРНК) и рибосомальные РНК (рРНК). Они различаются по первичной структуре, молекулярной массе, конфор-мации, продолжительности жизни и, самое главное, по функциональной активности. Транспортные РНК (тРНК) Пространственную структуру любых тРНК, независимо от различий в последовательности нук-леотидов, описывают универсальной моделью "клеверного листа. В каждой молекуле тРНК есть участки цепи, не участвующие в образовании водородных связей между нуклеотидными остатками. К ним, в частности, относят участок, ответственный за связывание с аминокислотой на 3'-конце молекулы и антикодон - специфический триплет нуклеотидов, взаимодействующий комплементарно с кодоном мРНК. В состав нуклеотидов тРНК входят минорные основания (в среднем 10-12 оснований на молекулу). Они представлены метилированными основаниями, изомерами и аналогами пиримидинов (рис. 4-11). Минорные основания выполняют 2 функции: они делают тРНК устойчивыми к действию нук-леаз цитоплазмы и поддерживают определённую третичную структуру молекулы, так как не могут участвовать в образовании комплементарных
10. Репликация, этапы репликации, ферменты. Реплика́ция ДНК — ключевое событие в ходе деления клетки. Репликация проходит в три этапа: 1. инициация репликации 2. элонгация 3. терминация репликации. Регуляция репликации осуществляется в основном на этапе инициации. Это достаточно легко осуществимо, потому что репликация может начинаться не с любого участка ДНК, а со строго определённого, называемого сайтом инициации репликации. В геноме таких сайтов может быть как всего один, так и много. С понятием сайта инициации репликации тесно связано понятие репликон. Репликон — это участок ДНК, который содержит сайт инициации репликации и реплицируется после начала синтеза ДНК с этого сайта. Геномы бактерий, как правило, представляют собой один репликон, это значит, что репликация всего генома является следствием всего одного акта инициации репликации. Геномы эукариот (а также их отдельные хромосомы) состоят из большого числа самостоятельных репликонов, это значительно сокращает суммарное время репликации отдельной хромосомы. Молекулярные механизмы, которые контролируют количество актов инициации репликации в каждом сайте за один цикл деления клетки, называются контролем копийности. В бактериальных клетках помимо хромосомной ДНК часто содержатся плазмиды, которые представляют собой отдельные репликоны. У плазмид существуют свои механизмы контроля копийности: они могут обеспечивать синтез как всего одной копии плазмиды за клеточный цикл, так и тысяч копий[1].Репликация начинается в сайте инициации репликации с расплетания двойной спирали ДНК, при этом формируется репликационная вилка — место непосредственной репликации ДНК. В каждом сайте может формироваться одна или две репликационные вилки в зависимости от того, является ли репликация одно- или двунаправленной. Более распространена двунаправленная репликация.В репликационной вилке ДНК копирует крупный белковый комплекс (реплисома), ключевым ферментом которого является ДНК-полимераза. Репликационная вилка движется со скоростью порядка \ нуклеотидов в минуту у \ 500—5000 — у эукариот[3]. Молекулярный механизм репликации. Ферменты (хеликаза, топоизомераза) и ДНК-связывающие белки расплетают ДНК, удерживают матрицу в разведённом состоянии и вращают молекулу ДНК. Правильность репликации обеспечивается точным соответствием комплементарных пар оснований и активностью ДНК-полимеразы, способной распознать и исправить ошибку. Репликация у эукариот осуществляется несколькими разными ДНК-полимеразами. Далее происходит закручивание синтезированных молекул по принципу суперспирализации и дальнейшей компактизации ДНК. Синтез энергозатратный.Цепи молекулы ДНК расходятся, образуют репликационную вилку, и каждая из них становится матрицей, на которой синтезируется новая комплементарная цепь. В результате образуются две новые двуспиральные молекулы ДНК, идентичные родительской молекуле.Характеристики процесса репликации · матричный — последовательность синтезируемой цепи ДНК однозначно определяется последовательностью материнской цепи в соответствии с принципом комплементарности; · полуконсервативный — одна цепь молекулы ДНК, образовавшейся в результате репликации, является вновь синтезированной, а вторая — материнской; · идёт в направлении от 5’-конца новой молекулы к 3’-концу; · полунепрерывный — одна из цепей ДНК синтезируется непрерывно, а вторая — в виде набора отдельных коротких фрагментов (фрагментов Оказаки); · начинается с определённых участков ДНК, которые называются сайтами инициации репликации. 11. Клеточный цикл и его регуляция. Процессы роста и деления клеток лежат в основе жизни любого организма. Но прежде чем совершить деление, клетка должна с высокой точностью копировать свой геном, синтезировать множество высоко- и низкомолекулярных соединений. Совокупность событий, обеспечивающих деление эукариотических клеток, называют "клеточный цикл". Продолжительность клеточного цикла зависит от типа делящихся клеток, у взрослого человека она может варьировать примерно от 8 ч и более, а для некоторых типов клеток до года и больше Все фазы клеточного цикла G1, S, G2, M могут различаться по длительности, но в особенности это касается фазы G1, длительность которой может быть равна практически нулю или быть столь продолжительной, что может казаться, будто клетки вообще прекратили деление. В этом случае говорят, что клетки находятся в состоянии покоя (фаза G0). Так, нейроны взрослого человека не делятся вообще. Клетки эпителия кишечника делятся на протяжении всей жизни человека, но даже у этих быстропролиферирующих клеток подготовка к делению занимает 24 ч. Клетки лёгких, почек, печени во взрослом организме начинают делиться только лишь в ответ на повреждение органов. Внешние сигналы могут стимулировать или ингибировать прохождение клетки через цикл. Пролиферативные сигналы очень разнообразны, они зависят от типа клетки, стадии развития и других факторов. Такими сигналами могут быть факторы роста, интерлейкины, гормоны, способные поддерживать или индуцировать пролиферацию определённых типов клеток. Сигнальные молекулы связываются специфическими мембранными рецепторами, активируют внутриклеточные пути передачи сигналов от рецептора к ядру и таким образом индуцируют транскрипцию определённых генов. Одними из первых активируются гены, кодирующие белки циклины. Белки были названы циклинами, потому что их концентрация в клетке периодически меняется по мере прохождения клеткой разных фаз клеточного цикла. Все циклины делят на 2 подсемейства: G1-циклины (D, Е) и митотические циклины (А и В). Любой из циклинов представлен группой полиморфных белков, например циклин D представлен формами Dl, D2, D3. У каждого типа циклинов есть гомологичный участок из 100 аминокислотных остатков - "циклиновый бокс", отвечающий за связывание с циклинзависимой киназой (от англ. CDK - cyclin-dependent kinases). В клетках эукариотов существует примерно восемь различных CD К (CDK1-8), активирующихся различными циклинами Циклинзависимые киназы, связывая циклин, переходят в активную форму и могут фосфорилировать специфические белки, например факторы транскрипции, белки-ингибиторы факторов транскрипции, которые регулируют синтез ферментов, обеспечивающих репликацию. Синтез каждого циклина начинается при подготовке к соответствующей фазе клеточного цикла, его концентрация в клетке повышается, а после окончания фазы резко падает до нуля. Завершившие свою работу комплексы циклинов и CDK связываются специфическими белками, ингибирующими их активность, и затем подвергаются разрушению. 12. РЕПАРАЦИЯ (от латинского reparatio — восстановление), свойственный клеткам всех организмов процесс восстановления природной (нативной) структуры ДНК, повреждённой при нормальном биосинтезе ДНК в клетке, а также физическими или химическими агентами. Осуществляется специальными ферментными системами клетки. Наиболее изучена репарация ДНК бактерий, повреждённой ультрафиолетовыми или ионизирующими излучениями. Обычно рассматривают 3 основных механизма репарации: фоторепарацию (фотореактивацию), эксцизионную репарацию и пострепликативную репарацию. Фоторепарация заключается в расщеплении ферментом дезоксирибопиримидинфотолиазой, активируемой видимым светом, циклобутановых димеров, возникающих в ДНК под действием ультрафиолетового излучения. Эксцизионная репарация заключается в узнавании повреждения ДНК, вырезании (эксцизии) повреждённого участка, ресинтезе ДНК по матрице интактной цепочки и восстановлении непрерывности цепи ДНК. Пострепликативная репарация включается в тех случаях, когда эксцизионная репарация не справляется с устранением всех повреждений, возникших в ДНК до её репликации. В этом случае воспроизведение повреждённых молекул приводит к появлению молекул с однонитевыми пробелами, а нативная структура восстанавливается с использованием, этапа рекомбинации. Ферменты репарации принимают участие в редупликации и рекомбинации, а также в мутационном процессе. В последнем случае в клетке работает особый тип индуцибельной репарации, склонной к ошибкам. В результате происходит восстановление нативной структуры ДНК, однако, с искажением заключённой в ней генетической информации. Мутации, блокирующие процессы репарации, часто приводят к повышению или понижению частоты мутационного процесса. Ряд наследственных заболеваний (например, пигментная ксеродерма, атаксия-телеангиэктазия, прогерия) связан с дефектами систем репарации. Штаммы бактерий и дрожжей, дефектные по репарации и обладающие повышенной чувствительностью к повреждающим агентам, используются в качестве индикаторов в генетической токсикологии. В радиобиологии под репарацией понимают восстановление биологических объектов от повреждений ионизирующим или ультрафиолетовым излучением. У многоклеточных организмов репарация проявляется в форме регенерации повреждённых облучением органов и тканей. Вопрос №33 Таблица 9-4. Наследственные нарушения орнитинового цикла и основные их проявления
Все симптомы гипераммониемии - проявление действия аммиака на ЦНС (см. выше подраздел IV, Б). Для диагностики различных типов гипераммониемии производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, акгивности фермента в биоптатах печени. Основной диагностический признак -повышение концентрации аммиака в крови. Содержание аммиака в крови может достигать 6000 мкмоль/л (в норме - 60 мкмоль/л). Однако в большинстве хронических случаев уровень аммиака может повышаться только после белковой нагрузки или в течение острых осложнённых заболеваний. Лечение больных с различными дефектами орнитинового цикла в основном направлено на снижение концентрации аммиака в крови за счёт малобелковой диеты, введения кетоаналогов аминокислот в рацион и стимуляцию выведения аммиака в обход нарушенных реакций: · путём связывания и выведения NH3 в составе фенилацетилглутамина и гишгуровой кислоты; · повышением концентрации промежуточных метаболитов цикла (аргинина, цитруллина, глутамата), образующихся вне блокируемых реакций. Вводимый больным с дефектом карбамоил-фосфатсинтетазы I в качестве пищевой добавки фенилацетат в результате его конъюгации с глутамином образует фенилацетилглутамин, который экскретируется почками. Состояние больных при этом улучшается, так как происходит активация синтеза глутамина и снижение концентрации аммиака в крови. Аналогичное действие оказывает введение бензоата, который связывает молекулу глицина. Образующаяся пшпуровая кислота выводится с мочой. В составе гиппурата происходит выделение азота из организма. Недостаток глицина компенсируется либо путём синтеза его из серина, либо за счёт образования из NH3 и СО2 в реакции, катализируемой глицинсинтетазой. При этом образование глицина сопровождается связыванием одной молекулы аммиака. При гипераммониемии II типа (дефект орнитинкарбамоилтрансферазы) введение больших доз цитруллина стимулирует синтез мочевины из аспартата (рис. 9-19, В), что также приводит к вьшедению азота из организма. Введение больших доз аргинина при аргининосукцинатурии (дефект аргининосукцинатлиазы) стимулирует регенерацию орнитина и выведение азота в составе цитруллина и аргининосукцината. Вопрос №35 Гиповитаминозы Нехватка витаминов ведет к развитию патологических процессов в виде специфическихгиповитаминозов или авитаминозов. Широко распространенные скрытые формы витаминной недостаточности не имеют ярко выраженных внешних проявлений и симптомов, но оказывают отрицательное влияние на работоспособность, общий тонус организма и его устойчивость к разным неблагоприятным факторам. Гипервитаминозы Жирорастворимые витамины при увеличении дозы накапливаются и могут вызывать гипервитаминозы с рядом общих симптомов (потеря аппетита, расстройство ЖКТ, сильные головные боли, повышенная возбудимость нервной системы, выпадение волос, шелушение кожи) и со специфическими признаками. Яркая картина гипервитаминозов отмечается только для витаминов А и D. Гиповитаминозы Причины нехватки витаминов могут быть экзогенными (внешние факторы) и эндогенными (состояние организма): Экзогенные гиповитаминозы: гельминтозы, лямблиозы, дизентерия, дисбактериоз кишечника, нерациональное питание, т.е. недостаточное потребление с пищей. Эндогенные гиповитаминозы: нарушение всасывания (энтероколиты, гастроэнтериты различного происхождения). Например, пернициозная анемия Аддисон-Бирнера при В12-зависимой макроцитарной анемии, заболевания печени, дискинезия желчного пузыря (для жирорастворимых витаминов), повышенная потребность (беременность, лактация, физические нагрузки), генетические дефекты кофермент-образующих ферментов. Провитамины Некоторые витамины поступают в организм в виде провитаминов. В организме провитамины превращаются в активные формы, например: каротиноиды превращаются в витамин А, пищевой эргостерол или 7-дегидрохолестерол под действием ультрафиолетовых лучей превращаются соответственно в эргокальциферол (D2) и холекальциферол (витамин D3). Авитамино́з — заболевание, являющееся следствием длительного неполноценного питания, в котором отсутствуют какие-либо витамины. Признаки авитаминоза § шелушение кожного покрова. § ломкость ногтей. § выпадение волос. § нежелание работать. Впоследствии авитаминоз может привести к гораздо более плохим последствиям: проблемам с желудочно-кишечным трактом, ухудшению зрения. Вопрос №37 Антивитамины Вещества, которые замещают витаминные коферменты в биохимических реакциях, или препятствуют синтезу кофермента или еще каким-либо образом препятствуют действию витамина, получили название антивитамины, например: дикумарол (антивитамин К) – препятствует образованию активной формы витамина К, что блокирует синтез факторов свертывания крови, изониазид (антивитамин РР) – образует "неправильные" коферменты, аналогичные НАД и НАДФ, что блокирует протекание окислительно-восстановительных реакций, птеридины (антифолаты) – вытесняют витамин В9 из реакций и препятствуют синтезу пуриновых и пиримидиновых оснований и, как следствие, нуклеиновых кислот, авидин (антивитамин Н) – связывается с витамином в кишечнике и не допускает его всасывания в кровь. Вопрос №40 Классификация минеральных веществ по В.И. Вернандскому: 1. Макроэлементы. Это элементы, содержание которых в организме выше 10-2 %. К ним относятся кислород, углерод, водород, азот, кальций, фосфор, калий, натрий, магний, сера и хлор. 2. Микроэлементы. Это элементы, содержание которых в организме находится в пределах от 10-3 до 10-5 %. К ним относятся железо, марганец, йод, цинк, кремний, медь, селен, бор, молибден, фтор, хром, кобальт, ванадий, германий. 3. Ультрамикроэлементы. Это элементы, содержание которых в организме ниже 10-5 %. К ним относятся алюминий, никель, олово, литий, свинец, бром, ртуть, мышьяк, кадмий, серебро, золото. В настоящее время ультрамикроэлементы объединяют с микроэлементами в одну группу. В табл. 3.2 приведены уточнённые данные по содержанию химических элементов в организме человека. Однако эта классификация отражает только содержание элементов в живых организмах, но не указывает на биологическую роль и физиологическое значение того или иного элемента. Макроэлементы сконцентрированы, как правило, в одном типе тканей живого организма (соединительные ткани, мышцы, кости, кровь). Они составляют пластический материал основных несущих тканей, обеспечивают свойства всей среды организма в целом: поддерживают определённые значения pH, осмотического давления, сохраняют в нужных пределах кислотно-основное равновесие, обеспечивают устойчивость коллоидных систем в организме. Микроэлементы неравномерно распределены между тканями и часто обладают сродством к определённому типу тканей и органов. Так цинк аккумулируется в поджелудочной железе; молибден – в почках; барий – в сетчатке глаза; стронций – в костях; йод – в щитовидной железе и др. Содержание макроэлементов в организме достаточно постоянно, но даже сравнительно большие отклонения от нормы совместимы с жизнедеятельностью организма. Напротив, уже незначительные отклонения содержания микроэлементов от нормы вызывают тяжёлые заболевания. Анализ на содержание отдельных микроэлементов в органах и тканях – чувствительный диагностический тест, позволяющий обнаруживать и лечить различные заболевания. Так, снижение содержания цинка в плазме крови – обязательное следствие инфаркта миокарда. Уменьшение содержание лития в крови – показатель гипертонического заболевания. Ещё одно различие в характере макро- и микроэлементов проявляется в том, что макроэлементы, как правило, входят в организме в состав органических соединений, тогда как микроэлементы либо образуют сравнительно простые неорганические соединения, либо входят в состав комплексных (координационных) соединений в качестве активных центров. Академик К. Б. Яцимирский назвал комплексообразующие микроэлементы «организаторами жизни». Строение и номенклатура основных пуриновых и пиримидиновых нуклеотидов. Роль свободных нуклеотидов. Каждый нуклеотид содержит 3 химически различных компонента: гетероциклическое азотистое основание, моносахарид (пентозу) и остаток фосфорной кислоты. В зависимости от числа имеющихся в молекуле остатков фосфорной кислоты различают нуклеозидмонофосфаты (НМФ), нуклеозиддифосфаты (НДФ), нуклео-зидтрифосфаты (НТФ). В состав нуклеиновых кислот входят азотистые основания двух типов: пуриновые - аденин (А), гуанин (G) и пиримидиновые - цитозин (С), тимин (Т) и урацил (U). Нумерация атомов в основаниях записывается внутри цикла. Пентозы в нуклеотидах представлены либо рибозой (в составе РНК), либо дезоксирибозой (в составе ДНК). Пентозу соединяет с основанием N-гликозидная связь, образованная С1-атомом пентозы (рибозы или дезоксирибозы) и N1 -атомом пиримидина или N9-aтомом пурина (рис. 4-4). Нуклеотиды, в которых пентоза представлена рибозой, называют рибонуклеотидами, а нуклеиновые кислоты, построенные из рибонуклеотидов, - рибонуклеиновыми кислотами, или РНК. Нуклеиновые кислоты, в мономеры которых входит дезоксирибоза, называют дезоксири-бонуклеиновыми кислотами, или ДНК. Нуклеиновые кислоты по своему строению относят к классу линейных полимеров. Остов нуклеиновой кислоты имеет одинаковое строение по всей длине молекулы и состоит из чередующихся групп - пентоза-фосфат-пентоза- (рис. 4-5). Вариабельными группами в полинуклеотидных цепях служат азотистые основания - пурины и пиримидины. В молекулы РНК входят аденин (А), урацил (U), гуанин (G) и цитозин (С), в ДНК - аденин (А), тимин (Т), гуанин (G) и цитозин (С). Уникальность структуры и функциональная индивидуальность молекул ДНК и РНК определяются их первичной структурой -последовательностью азотистых оснований в полинуклеотидной цепи.
Рис. 4-4. Пуриновый и пиримидиновый нуклеотиды. Свободные нуклеотиды, в частности АТФ, цАМФ, АДФ, играют важную роль в энергетических и информационных внутриклеточных процессах, а также являются составляющими частями нуклеиновых кислот и многих коферментов.
|
||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 1723; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.175.180 (0.088 с.) |