
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Активированные метаболиты: АТФ и другие нуклеозидтрифосфатные коферменты, активированный метионин, ацетил-КоА и др. ⇐ ПредыдущаяСтр 4 из 4
Аденозин-5′-трифосфат (АТФ) и другие нуклеозидтрифосфаты – гуанозин-5′-трифосфат (ГТФ), уридин-5′-трифосфат (УТФ), тимидин-5′-трифосфат (ТТФ) и цитидин-5′-трифосфат (ЦТФ) – являются коферментами и переносят фосфатные и нуклеозидные группы на субстраты. Например, в мышцах в значительном количестве присутствует фосфокреатин, образующийся из креатина и АТФ.
Вследствие того, что эта реакция обратима, при интенсивной мышечной работе фосфокреатин быстро пополняет расходуемые запасы АТФ, передавая остаток фосфорной кислоты на накапливающийся аденозин-5′-дифосфат (АДФ). Поскольку при использовании АТФ в ряде реакций образуется аденозин-5′-монофосфат (АМФ), а для регенерации АТФ необходим АДФ, то в местах интенсивного расходования АТФ обычно присутствует фермент аденилаткиназа, катализирующий реакцию образования АДФ из АМФ.
Кроме того, нуклеозидтрифосфаты, обладая макроэргическими связями (связи при гидролизе которых выделяется большое количество энергии), участвуют в реакциях активации различных метаболитов, а также являются исходными соединениями вбиосинтезе нуклеиновых кислот. Метаболиты становятся реакционноспособными («активированными») при присоединении фосфатных или аденозильных остатков. Примером переноса нуклеозидного остатка может служить реакция переноса 5′-аденозильной группы на метионин, в результате которой образуется S-аденозилметионин («активированный метионин»).
Лигазы катализируют сшивание соединений за счет энергии нуклеозидтрифосфатов, например, в реакции образования аспарагина из аспарагиновой кислоты и иона аммония участвует АТФ.
Кофермент А является водорастворимым коферментом ацилтрансфераз – ферментов, катализирующих реакции переноса ацильных групп. Сокращенно его обозначают как КоА (СоА) или, если требуется записать химическими символами связанный с ним ацильный остаток, его записывают как КоА-SH. В организме КоА образуется из пантотеновой кислоты (витамин В3), цистеамина и АТФ. С химической точки зрения КоА представляет собой эфир пантетеина по γ-гидроксильной группе пантоевой кислоты и 3′-фосфоаденозин-5′-дифосфата по 5′-дифосфатной группе (рис.1.1.).
Строение кофермента А – КоА.
Пантетеин состоит из трех компонентов, связанных амидными связями: пантоевой кислоты, β-аланина и цистеамина.Пантотеновая кислота,образованная из пантоевой кислоты и β-аланина, в организме человека играет роль витамина В3. Кофермент А является акцептором ацильных групп в реакциях окислительного декарбоксилирования α-кетокислот, в ходе которых образуются 6-S-ацилдигидролипоамиды.
Тиоэфиры, какими являются ацил-КоА, представляют собой активированные формы карбоновых кислот. Ацильный остаток ацил-КоА легко переносится на другие молекулы.
Тетрагидрофолат (ТГФ) является коферментом, который может переносить С1-остатки в различных степенях окисления. ТГФ образуется из витамина фолиевой кислоты в результате двойного гидрирования птеринового кольца. С1-фрагменты присоединяются к атомам N5, N10 или к обоим атомам азота в виде мостика. Наиболее важными производными тетрагидрофолата, переносящими С1 фрагменты, являются: 10N-формил-ТГФ, 5N,10N-метилен-ТГФ и 5N-метил-ТГФ. Формильное производное ТГФ используется в качестве донора формильных групп, в первую очередь в биосинтезе пуриновых нуклеотидов. Метиленовое производное ТГФ является исходным для образования формильного и метильного производных ТГФ. Метильное производное используется для метилирования главным образом по сульфгидрильным группам метоболитов.
Главным процессом, в результате которого ТГФ «заряжается» одноуглеродным фрагментом, является его реакция с серином с образованием 5N,10N-метилен-ТГФ, катализируемая ферментом гидроксиметилтрансферазой.
5N,10N-Метилен-ТГФ далее может окисляться, образуя 10N-формил-ТГФ или восстанавливаться, образуя 5N-метил-ТГФ.
Тиаминпирофосфат (ТПФ) активирует альдегиды и кетоны и переносит их в виде гидроксиалкильных групп на другую молекулу. Этот способ переноса важен, например, в транскетолазной реакции. Гидроксиалкильные остатки участвуют также в декарбоксилировании кетокислот. Они либо высвобождаются в виде альдегидов, либо переносятся на липоамидные остатки, как в случае дегидрогеназ 2-кетокислот. Ниже приведена схема реакций 2-кетокислот с участием ТПФ в качестве кофермента (рис.1.2.).
Взаимодействие ТПФ с 2-кетокислотами и перенос ацильной группы на липоамид.
Молекула ТПФ имеет подвижный атом водорода в положении 2 тиазольного кольца, благодаря чему легко присоединяется к карбонильным соединениям, образуя «заряженные» формы ТПФ. Пиридоксальфосфат - наиболее важный кофермент в метаболизме аминокислот. Его роль при трансаминировании была подробно рассмотрена нами ранее (Аминокислоты и полипептиды: учеб. пособ. Ч. I./ В.А. Смирнов, Ю.Н. Климочкин. – Самара. Самар. гос. техн. ун-т., 2007, стр. 31-33). Пиридоксальфосфат принимает участие и в других реакциях аминокислот, таких, как декарбоксилирование и дегидратирование. Представленная здесь альдегидная форма в свободном виде не встречается. В отсутствие субстрата альдегидная группа связана с аминогруппой лизинового остатка фермента в виде альдимина. Биотин реагирует с гидрокарбонатом (НСО3-) в присутствии АТФ с образованием биотин-N-кар6оксилата.
Эта активированная форма диоксида углеродаможет быть перенесена на другую молекулу. Примерами биотинзависимых реакций являются образование оксалоацетата из пирувата и синтез малонил-КоА из ацетил-КоА Примерами биотинзависимых реакций являются реакции карбоксилирования пирувата с образованием оксалоацетата; ацетил-КоА с образованием малонил-КоА; пропионил-КоА с образованием метилмалонил-КоА. СН3СОСОО‾ + НСО3‾ + АТФ → ‾ООССН2СОСОО‾ + АДФ + Н2РО4‾ СН3СО-КоА + НСО3‾ + АТФ → ‾ООССН2СО-КоА + АДФ + Н2РО4‾ СН3СН2СО-КоА + НСО3‾ + АТФ → ‾ООССН(СН3)СО-КоА + АДФ + Н2РО4‾ С помощью первой из рассматриваемых реакций осуществляется непрерывное пополнение щавелевоуксусной кислоты, необходимой для работы цикла Кребса. Вторая реакция важнейший этап в биосинтезе жирных кислот. Третья реакция обеспечивает утилизацию пропионовой кислоты, образующейся при β-окислении жирных кислот с разветвленным углеродным скелетом или нечетным числом атомов углерода. 5′-Дезоксиаденозилкобаламин (коферментная форма витамина В12) принимает участие в реакции изомеризации метилмалонил-КоА в сукцинил-КоА; биосинтезе метионина из гомоцистеина; восстановлении рибонуклеотидов бактериями до дезоксирибонуклеотидов.
|
||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 512; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.216.163 (0.009 с.) |
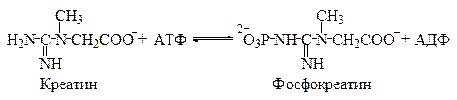




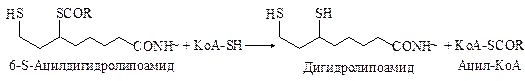
 Например, при взаимодействии ацил-КоА с 3-глицерофосфатом образуются фосфатидные кислоты.
Например, при взаимодействии ацил-КоА с 3-глицерофосфатом образуются фосфатидные кислоты. Ниже приведены структурные фрагменты С1-производных ТГФ (R – заместитель, структура которого одинакова в ТГФ и фолиевой кислоте, см. табл.1 и 3).
Ниже приведены структурные фрагменты С1-производных ТГФ (R – заместитель, структура которого одинакова в ТГФ и фолиевой кислоте, см. табл.1 и 3).


 В качестве примера переноса метильной группы рассмотрим реакцию, в которой главным образом расходуется 5N-метил-ТГФ, – синтез метионина из гомоцистеина.
В качестве примера переноса метильной группы рассмотрим реакцию, в которой главным образом расходуется 5N-метил-ТГФ, – синтез метионина из гомоцистеина.




