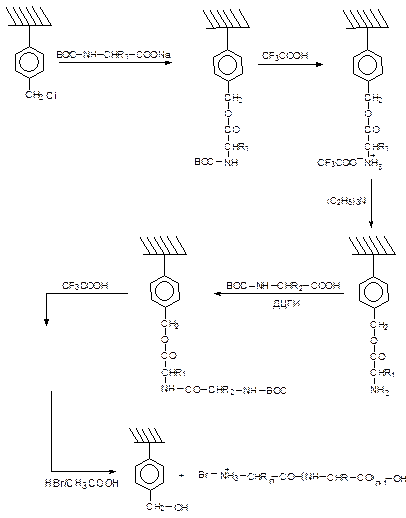Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Синтез пептидов на полимерных носителях
Пептиды, играющие большую роль в жизни организмов в качестве гормонов, регуляторов, передатчиков импульсов и др., представляют собой олигомеры (или полимеры) a-аминокислот, соединенных друг с другом амидными связями в определенной последовательности. Синтез пептидов сводится к серии циклов последовательных операций — конденсация двух аминокислот, одна из которых защищена по карбоксильной группе, другая — по аминогруппе, деблокирование (как правило, с аминоконца), депротонирование и конденсация со следующей N-защищенной аминокислотой
Z-NH-CHR1-COOH ¾¾¾® Z-NH-CHR1-COX ¾¾¾¾¾¾®
¾¾¾¾¾® Z-NH-CHR1-CO-NH-CHR2-COOY ¾¾¾¾¾¾®
¾® NH2-CHR1-CO-NH-CHR2-COOY и т.д.
где Z — защитная группа аминофункции; Rn — боковой заме-ститель при a-углеродном атоме аминокислоты; X — электроно-акцепторная активирующая группа; Y — защитная группа карбоксильной функции.
Синтез чрезвычайно трудоемок из-за необходимости очистки продуктов от избытка реагентов и побочных веществ на каждой стадии. С ростом пептидной цепи сложности значительно возрастают. В результате суммарный выход при синтезе петидов, содержащих 10 аминокислот, оказывается порядка одного процента в расчете на исходные реагенты. Суть метода, предложенного Меррифилдом, заключается в присоединении первой с С-конца синтезируемого пептида защищенной аминокислоты сложноэфирной связью к нерастворимому полимерному носителю, в качестве которого был использован хлорметилированный сополимер стирола с дивинилбензолом. Таким образом, носитель играет роль полимерной защитной группы. Затем действием кислоты производится деблокирование аминогруппы, ее депротонирование и конденсация со следующей защищенной аминокислотой с использованием, например, дициклогексилкарбодиимида (ДЦГИ) (см. схему на с. 91). При этом полимерный носитель с ковалентно присоединенной к нему растущей пептидной цепью от начала и до конца синтеза находится в одном реакционном сосуде, меняются только реакционные растворы, которые вместе с избытком реагентов и побочными продуктами реакции отделяются от носителя простым фильтрованием и промывкой. Это позволяет использовать значительные избытки активированных производных кислот и добиваться на каждой стадии практически количественных выходов. Стандартный характер производимых с носителем операций дает возможность автоматизации процесса. Меррифилд сконструировал автоматический синтезатор пептидов и провел на нем синтез белка, состоящего из 184 аминокислотных остатков — рибонуклеазы А, при этом синтезированный белок обладал полной биологической активностью. За это достижение Меррифилд был удостоен Нобелевской премии.
Схема синтеза пептидов по Меррифилду.
Впоследствии принцип синтеза на полимерных носителях был с успехом применен для получения олигонуклеотидов и олигосахаридов с заданной последовательностью нуклеотидов и моносахаридов соответственно. Вместе с тем, при всех достоинствах твердофазного метода синтеза пептидов со временем обнаружились и его недостатки. По сути такой синтез представляет собой длинную цепь полимер-аналогичных превращений, протекающих в зернах носителя гелевого или микрогетерогенного типа, со всеми вытекающими из этого достоинствами и недостатками. В первую очередь, недостатки связаны с тем, что выходы на стадии ацилирования не всегда оказываются 100%-ными. В результате накопления ошибок, особенно при синтезе длинных пептидов, целевой продукт может содержать близкие по составу и поэтому очень трудно отделимые “укороченные” пептиды, лишенные в своей структуре одного или нескольких аминокислотных остатков. Кроме того, рост пептидов может обрываться за счет взаимодействий пептидных цепей как между собой, так и с цепями самого носителя. Получающийся в результате синтеза продукт можно на определенной стадии рассматривать как привитой сополимер со всеми вытекающими из этого последствиями, главным из которых является возможность микрофазового разделения. Сегрегация пептидных цепей в виде твердых микрогетерогенных участков может иметь следствием прекращение их дальнейшего роста из-за невозможности доступа реагентов внутрь таких областей. Эти недостатки стимулировали поиск новых подходов к использованию полимеров в сложном органическом синтезе. Один из таких подходов — использование носителей, имеющих большее термодинамическое сродство с пептидами. В качестве примеров можно привести носители на основе гидрофильных полимеров — декстрана, полиакриламида и некоторых других.
Другой подход заключается в использовании в качестве носителей растворимых полимеров. Химизм процесса остается тот же, также используются значительные избытки реагентов, однако удаление этих избытков и побочных продуктов реакции производится не фильтрованием, а диализом или многократным переосаждением полимер-пептидного конъюгата после каждой стадии синтеза. Это делает процесс весьма трудоемким и в то же время не устраняет некоторые недостатки твердофазного синтеза, например, возможность взаимодействия пептидных цепей между собой, что ограничивает доступ реагентов к активным центрам даже при синтезе в растворе. Поэтому растворимые носители не нашли широкого практического применения.
|
||||||
|
Последнее изменение этой страницы: 2017-01-20; просмотров: 595; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.118.198 (0.004 с.) |