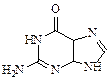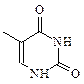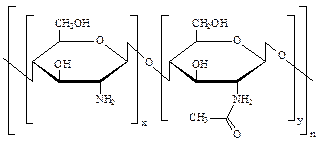Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общие сведения о биополимерах и полимерах медицинского назначения
Высокомолекулярные соединения, как отмечено выше, играют очень важную роль в существовании на Земле жизни в любых ее проявлениях. Полимеры, из которых построены клетки живых организмов и межклеточное вещество, связывающее их между собой, принято называть биополимерами. Следует подчеркнуть, что биополимеры играют определяющую роль в существовании и субклеточных форм жизни, например, вирусов. К биополимерам относятся белки, нуклеиновые кислоты, полисахариды и так называемые смешанные биополимеры, содержащие в полимерной цепи звенья различной химической природы. Например, гликопротеиды содержат звенья аминокислот и сахаридов, липопротеиды — звенья аминокислот и жирных кислот с длинной углеводородной цепью и т.д. Функциональная роль ВМС в живых организмах имеет очень широкий спектр — от структурной до информационной. Так, белки могут служить материалом для формирования тканей организмов (коллаген составляет основу соединительной ткани, актин и миозин — мышечной), катализировать биохимические реакции (ферменты), регулировать процессы в организме (гормоны), играть защитную роль, выполнять транспортную, каталитическую, хемомеханическую и множество других функций. Химическая структура цепи белковой макромолекулы может быть представлена в следующем общем виде:
Несмотря на кажущуюся простоту этой химической формулы, реальная структура белковых макромолекул очень сложна и разнообразна. Это связано с тем, что цепи белковых молекул представляют собой строго определенные последовательности, скомбинированные из, как минимум, 20 природных аминокислот L-конфигурации, различающихся природой радикала R. Число таких звеньев в цепи в сочетании с числом возможных их сочетаний огромно. Сегодня известны сотни тысяч белков, и число вновь открываемых постоянно растет. Последовательность аминокислотных звеньев в белковой макромолекуле представляет собой первичную структуру белка. Она в очень большой степени определяет его физико-химические и функциональные свойства. Первичная структура играет ключевую роль в формировании более высоких уровней структурной организации – вторичной, третичной и четвертичной. Формирование вторичной структуры белковых макромолекул или их фрагментов связано с образованием внутримакромолекулярных водородных связей. В результате могут возникать спиральные участки (α-спираль) и складчатые β-структуры. Часть последовательности цепи белковой макромолекулы может быть не структурирована и находиться в конформации статистического клубка.
Различные способы представления вторичной структуры белковых макромолекул: Третичная структура возникает при формировании внутримакромолкулярных ковалентных связей, как правило, дисульфидных, между двумя отстоящими друг от друга звеньями серосодержащей аминкислоты цистеина. Четвертичная структура формируется при ассоциации нескольких белковых макромолекул друг с другом за счет слабых нековалентных, но высокоспецифических взаимодействий. Энергетические (химические, термические и др.) воздействия на белки приводят к их денатурации – разрушению вторичной или третичной структур, сопровождающейся резким и значительным изменением их физико-химических свойств и утратой биологической активности. Как правило, процесс денатурации необратим. Основное назначение дезоксирибонуклеиновых кислот — информационное, т. е. передача генетической информации из поколения в поколение при клеточном делении. Химическая структура этих веществ достаточно сложная – основная цепь представляет собой чередующиеся звенья фосфорной кислоты и рибозы, включенной в цепь в положениях 3 и 5; в положении 1 в звене рибозы включено пуриновое или пиримидиновое основание R.
Полисахариды, как и белки, могут играть структурную роль (целлюлоза)
могут служить резервными питательными веществами (крахмал, гликоген, формула которых представлена ниже) обеспечивать специфические свойства поверхности клетки (например, антигенные полисахариды микроорганизмов), а также защищать организм в целом (камеди и слизи растений).
Химическая структура крахмала и гликогена.
В последние десятилетия значительное внимание медиков, биологов и химиков привлекают хитин – поли-β-2-ацетиламидо-1,4-гликан.
Этот натуральный полисахарид является, пожалуй, вторым после целлюлозы натуральным полимером, производимым в природе. Его основная биологическая функция – экзоскелет членистоногих. Поражают его прочностные характеристики – панцири ракообразных, крылья насекомых и другие элементы экзоскелета. Собственно хитин, как и целлюлоза, практически нерастворим. Однако путем полимераналогичных химических превращений – гидролитическим отщеплением ацетильной группы – его можно трансформировать в хитозан – полимер, несущий при гликозидном цикле свободную аминогруппу. Глубину проведения реакции гидролиза (содержание аминогрупп X) можно регулировать в широких пределах. Таким образом, хитозан не является полимером со строго определенной химической структурой, а представляет собой целое семейство полимеров с существенными различиями в свойствах внутри этого семейства. Некоторые хитозаны обладают собственной биологической активностью, но в большинстве случаев они используются как полимерные носители для лекарственных средств. Полиоксиалканоаты (алифатические полиэфиры) распространены в природе не так широко, как рассмотренные выше группы полимеров. Химические структуры наиболее распространенных полиоксиалканоатов.
Они были обнаружены у некоторых бактерий в качестве гидрофобных включений и выполняют в этих микроорганизмах роль резервных источников энергии. Эти полимеры, роль которых в природе ничтожна, привлекли внимание исследователей несколько десятилетий назад своей способностью претерпевать быструю биодеструкцию за счет гидролиза сложноэфирных связей, при этом образуются нетоксичные оксикислоты. Это свойство дало основания использовать природные полиоксиалканоаты и их синтетические аналоги в различных биомедицинских технологиях – от саморассасывающихся хирургических нитей до биодеградируемой полимерной основы искусственных тканей и органов в тканевой инженерии. Более детально биомедицинские технологии, основанные на использовании биодеградируемых полтимеров, будут рассмотрены в деталях в соответствующих разделах. Естественно, что при таком многообразии и важности функции ВМС в жизни организмов, они представляют огромный интерес не только для исследователей, но и для практиков, работающих в медицине и биологии. Самое главное, что понимание их роли и механизмов функционирования невозможно без учета их полимерной природы. В частности, уникальные свойства биополимеров, особенно белков и нуклеиновых кислот, во многом определяются существованием их макромолекул в упорядоченной конформации, которая фиксируется слабыми внутримолекулярными взаимодействиями (водородные связи, гидрофобные взаимодействия). При разрушении этой нативной конформации под действием повышенных температур или определенных химических веществ происходит так называемая денатурация, т. е. переход от упорядоченной конформации к конформации статистического клубка. Как правило, это процесс необратимый. Только в редких случаях возможна ренатурация биополимера. Поэтому биополимеры представляют собой объект исследования и моделирования для специалистов, работающих в химии высокомолекулярных соединений.
Наряду с природными полимерами огромный интерес с точки зрения их исследования и использования в медицине и биологии представляет собой и значительное число синтетических полимеров. Этот интерес определяется многообразием их свойств, как в конденсированном состоянии, так и в растворах. Многообразие свойств открывает широчайшие возможности применения полимеров во всех областях медицины, биологии, биохимии, иммунологии и других смежных с медициной дисциплинах, начиная от предметов медико-технического назначения до сложнейших систем иммунохимического анализа или активных (т. е. переносящих кислород) кровезаменителей. Основное внимание в настоящей главе уделено использованию полимеров в медицине. Особенности таких полимеров и изделий из них заключаются в том, что прямо или опосредованно они находятся в контакте с биологическими средами живого организма и могут с ними взаимодействовать. Характер и возможные последствия взаимодействия в каждом конкретном случае должны быть тщательнейшим образом изучены до того, как тот или иной полимер будет допущен к практическому использованию. По степени и характеру взаимодействия с тканями и биологическими средами организма полимеры, используемые в медицине, можно условно разделить на три большие группы. 1. Полимеры медико-технического назначения, имеющие ограниченный и опосредованный контакт с тканями организма. В эту группу входят полимеры для изготовления деталей медицинских приборов, предметов ухода за больными, упаковок лекарств и пр. 2. Полимеры, предназначенные для введения в организм и пребывания в нем в течение достаточно длительного срока (от нескольких часов до нескольких лет). Полимеры этой группы могут быть разделены на две подгруппы: полимеры, вводимые в организм оперативным (инвазивным) путем или с помощью инъекций, и полимеры, вводимые перорально, т. е. через рот. 3. Полимеры, имеющие непосредственный контакт с биологическими средами организма в качестве функциональных узлов медицинских аппаратов, таких, как искусственное легкое, искусственная почка, аппараты для гемодиализа и др. Следует учитывать условность такого разделения – группы, предложенные выше, зачастую пересекаются в своих функциях. Полимеры каждой из перечисленных групп должны отвечать определенным требованиям.
|
||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-20; просмотров: 652; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.176.66 (0.01 с.) |
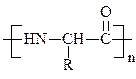

 Звено дезоксирибонуклеиновой кислоты
Звено дезоксирибонуклеиновой кислоты