
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общие представления о химическом равновесии. Константа химического равновесия
Химические реакции, в результате которых хотя бы одно из исходных веществ расходуется полностью, называются необратимыми, протекающими до конца. В уравнениях таких реакций принято ставить знак “ = “. Однако большинство реакций являются обратимыми, т.е. идущими в двух противоположных направлениях (прямом и обратном). Особенность таких реакций: они не протекают до конца, в системе всегда остается каждое из исходных веществ. Примеры: 2NO + Cl2 D 2NOCl; H2 + I2 D 2HI; N2 + 3H2 D 2NH3; СО + H2O D CO2 + H2 и т.д.
Все обратимые реакции идут до состояния равновесия. Реакция, протекающая в правую сторону (→) – прямая реакция, а в левую сторону () – обратная реакция. Кинетические кривые для прямой (1) и обратной (2) реакции представлены на рис. 7.1. Со временем скорость прямой реакции, V®, уменьшается, а скорость обратной, V, возрастает. В некоторый момент времени V® становится равной V, наступает химическое равновесие (частный случай термодинамического равновесия). Химическим равновесием называют такое состояние реагирующей системы, при котором скорость прямой реакции V® равна скорости обратной реакции V. Равенство V® = V является кинетическим условием химического равновесия. Химическое равновесие характеризуется постоянством величины энергии Гиббса системы GP,T. Равенство D GP,T = 0 является термодинамическим условием химического равновесия. Концентрации исходных веществ и продуктов реакции (реагирующих веществ), которые устанавливаются при химическом равновесии, называют равновесными. Обычно их обозначают при помощи квадратных скобок, например, [NO], [Cl2], [NOCl], в отличие от неравновесных концентраций, СNO, ССl2, СNOCl. Химическое равновесие является динамическим или подвижным. Это означает, что в системе, находящейся в состоянии химического равновесия, с равной скоростью идут прямой и обратный процессы, поэтому в системе видимых изменений не наблюдается, т.е. макроскопические параметры, в том числе концентрации веществ, остаются постоянными. Допустим, что в гомогенной системе протекает обратимая химическая реакция: аА + bВ D сС +dD. (1) В соответствии с законом действия масс: V® = k® · [А]a · [В]b, (2) V = k · [С]c · [D]d. (3) В состоянии химического равновесия V® = V или k® · [А]a · [В]b = k · [С]c · [D]d. (4)
После преобразования:
где К – константа равновесия химической реакции. Закон действия масс для обратимых химических процессов формулируется следующим образом: отношение произведения равновесных молярных концентраций продуктов реакции к произведению равновесных молярных концентраций исходных веществ, взятых в степени их стехиометрических коэффициентов, при данной температуре равно постоянной величине, называемой константой химического равновесия. Константа равновесия, как следует из выражения (5), равна отношению констант скоростей прямой и обратной реакций. Она показывает, во сколько раз скорость прямой реакции больше скорости обратной реакции, если концентрации каждого из реагирующих веществ равны 1 моль/л. В этом заключается физический смысл константы химического равновесия K. Константа равновесия зависит от температуры протекания процесса (поскольку k® и k зависят от температуры) и природы реагирующих веществ, но не зависит от их концентрации и наличия катализатора. Например, для гомогенной химической реакции синтеза и разложения йодоводорода: I2(г) + Н2(г) D2HI(г), выражение для константы химического равновесия будет иметь вид
Если в гетерогенной системе протекает обратимая химическая реакция, то к ней также применим закон действующих масс, но в выражение для константы химического равновесия не входят концентрации реагирующих веществ, находящихся в конденсированном состоянии (твердом или жидком), т.к. их концентрации остаются, как правило, постоянными и входят в значение соответствующих констант скоростей химической реакции. Например, для гетерогенной реакции (термического разложения) карбоната кальция: CaCO3(тв) D СaO(тв) + CO2(г), выражение для константы химического равновесия будет иметь вид К=[СО2]. Константа химического равновесия связана с изменением энергии Гиббса химической реакции (изобарно-изотермическим потенциалом) ΔG уравнением ΔG = - RT lnK или К = ехр где R – универсальная газовая постоянная (8,31 Дж/(моль∙К)); Т – абсолютная температура, К; К – константа равновесия. При стандартных условиях (Т = 298 К): ΔG0298 (кДж) = - 5,71·lgK298.
Приведенное уравнение позволяет по величине ΔG вычислить К, а затем и равновесные концентрации (парциальные давления) реагентов. Если: - K > 1, то ΔG < 0, в равновесной смеси преобладают продукты взаимодействия, равновесие смещено вправо (протекает прямая реакция); - K < 1, то ΔG > 0, в равновесной смеси преобладают исходные вещества, равновесие смещено влево (обратная реакция); - K = 1, то ΔG = 0, скорости прямой и обратной реакций равны между собой, состояние химического равновесия.
|
|||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 97; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.26.246 (0.006 с.) |

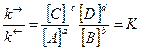 , (5)
, (5)
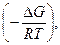 (6)
(6)


