
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теплоемкость гав и газовых смесей
2.2.1. Понятие теплоемкости Экспериментально установлено, что величина теплоты, необходимая для изменения температуры конкретного количества вещества системы, пропорциональна разности конечной и начальной температур: Q = C (T2 – T1), где С – коэффициент пропорциональности. В общем случае коэффициент С характеризует физическое свойство системы, которое называется т е п л о е м к о с т ь ю. Количественно теплоемкость равна теплоте, которой обменивается с окружающей средой система при изменении ее температуры на один кельвин. Аналитически это определение записывается в виде С = За единицу теплоемкости принят джоуль на кельвин (Дж/К). Теплоемкость, отнесенную к какой-либо количественной единице вещества, называют у д е л ь н о й. Для газов широко используются массовая, молярная и объемная удельные теплоемкости. Массовая теплоемкость численно равна количеству теплоты, необходимому для изменения температуры одного килограмма газа на один кельвин. Обозначают удельную массовую теплоемкость строчной буквой с и выражают в Дж/(кг· К). Теплоемкость одного моля газа называют м о л я р н о й теплоемкостью. Ее обозначают Теплоемкость единицы объема газа при нормальных физических условиях именуют о б ъ е м н о й теплоемкостью. Ее обозначают с′ и выражают Массовая, молярная и объемная теплоемкости связаны соотношением: с = где ρ – плотность газа при нормальных физических условиях. Численное значение теплоемкости газа так же, как и теплоемкость твердых и жидких тел, зависит от его природы и уровня температуры, при которой она определяется. Однако кардинальным отличием понятия теплоемкости газа от теплоемкости жидких и твердых тел является то, что на величину теплоемкости газа специфическое влияние оказывает характер процесса, в котором она вычисляется. Так, в адиабатном процессе, где dQ = 0, теплоемкость равна нулю. В процессе с постоянной температурой (T = const) теплоемкость равна бесконечности (c = ± ∞). Теплоемкость газа, присущую тому или иному процессу, принято обозначать индексом, характеризующим конкретный процесс. Если теплоемкость определяется в процессе при постоянном давлении, то ее обозначают cp и т.д.
2.2.2. Теплоемкости cp и cv В термодинамике широко используются две теплоемкости – cp (в процессе при постоянном давлении) и cv (в процессе при постоянном объеме).
Для цилиндра 1 запишем уравнение первого закона термодинамики в виде dqv = du + pdv. Разделим его на dT и, принимая во внимание, что dv = 0, получим:
откуда cv = Интегрированием уравнения (2.26) от начального до конечного состояния процесса получим связь между изменением внутренней энергии и температуры: ∆ u = cv ∆T. (2.27) Проделав аналогичные операции с уравнением первого закона термодинамики для газа, находящегося во втором цилиндре, получим: cp = Отсюда следует соотношение между изменениями энтальпии и температуры в виде ∆i = cp ∆T. (2.29) Теплоемкости в процессах при постоянном давлении и постоянном объеме имеют не только различные математические выражения, но и различные числовые значения. Так, доказывается, что cp >cv. Это видно из сравнения уравнений (2.26) и (2.28). Поскольку при одинаковом изменении температуры величина di > du, то, следовательно, cp > cv . Обращаясь к рассмотренному примеру, можно пояснить сущность неравенства cp > cv. Так, при одинаковом изменении температуры газа в цилиндрах величина теплоемкостей определяется количеством подведенной теплоты. Ко второму цилиндру необходимо подвести больше теплоты, так как требуется не только изменить температуру газа на одно и то же число градусов, но и совершить некоторую работу расширения. Можно определить, на сколько cp > cv. Для этого вычтем из (2.28) выражение (2.26) и, учитывая соотношение (1.6), получим: cp – cv = Дифференцируя уравнение состояния для 1 кг газа, будем иметь:
d(pv)=RdT Следовательно, cp – cv = R. (2.30) Выражение (2.30) называется у р а в н е н и е м М а й е р а. Оно показывает, что для любого газа разность между теплоемкостями при p =const и v =const численно равна величине газовой постоянной этого газа. Отношение теплоемкостей c p и c v называют п о к а з а т е л е м а д и а б а т ы и обозначают буквой к, т.е.
Величина к зависит от природы газа и всегда больше единицы. По известным значениям R и к можно вычислить как cp , так и cv, используя следующие выражения: сp = c v = 2.2.3. Зависимость теплоемкости от температуры Теоретические исследования и опытные данные показывают, что при повышении температуры газа колебательные движения атомов в молекуле становятся интенсивнее. При этом для повышения температуры газа на каждый градус необходимо все большее количество энергии в форме теплоты. Таким образом, теплоемкость газа представляет собой функцию температуры. В общем случае зависимость теплоемкости газа от температуры можно представить в виде степенного ряда c = c0 + α t + β t2 + где c0 – значение теплоемкости при t = 0 0 С; α, β, Значения c 0, α, β, В качестве примера приведем квадратичную зависимость молярной теплоемкости азота от температуры:
В диапазоне температур, имеющих место в современных тепловых машинах, зависимость теплоемкости от температуры с достаточной степнью точности можно считать линейной. Это значит, что в уравнении (2.34) можно учитывать только два первых слагаемых, т.е.: c = c0 +α t (2.35) Теплоемкость, соответствующую данной температуре, называют и с т и н н о й. и вычисляют по уравнению (2.34) или (2.35). В теплотехнических расчетах часто возникает необходимость знать с р е дн е е значение теплоемкости в определенном интервале температур. Средней теплоемкостью c ср данного процесса в интервале температур от t 1 до t2 называют отношение теплоты процесса q 1-2 к разности температур t 2 – t 1, т.е. c ср = После подстановки значений q 1-2 = с с р =с0 + α В Приложении табл.5 приведены значения истинной теплоемкости отдельных газов, а в табл. 6 – их средние значения в диапазоне температур от 0 до 2300 0С. При необходимости вычисления средней теплоемкости в диапазоне температур от t 1до t 2 можно применить формулу сср Показатель адиабаты к также зависит от температуры. Это можно показать, представив соотношение (2.31) в виде к = Экспериментальное изучение зависимости c = f (t) для идеальных газов показывает, что у каждого газа существует некоторый интервал температур, в котором его теплоемкость практически постоянна. Идеальный газ в том интервале температур, где теплоемкость не изменяется, называется с о в е р ш е н н ы м.. Соотношения (2.27) и (2.29) справедливы только для совершенного оаза Опытное изучение зависимости теплоемкости газов от давления показывает, что это влияние незначительное, и в практических расчетах его можно не учитывать.
2.2.4 Теплоемкость газовых смесей В справочной литературе приводятся теплоемкости только для отдельных газов, в то время как при тепловых расчетах приходится встречаться с газовыми смесями. Ниже приведены выражения для вычисления теплоемкости смеси газов, если она задана парциальными давлениями, массовыми или объемными долями.
сp см = cp см =
Для смеси газов справедливо уравнение Майера, которое будет иметь вид сp см – сv см = R см. (2.42)
Термодинамические процессы 2.3.1. Понятие термодинамического процесса Общее представление о состоянии системы и ее изменениях (процессах) изложено в подпункте 1.1.3. Термодинамический процесс – это определенная последовательность изменения параметров состояния рабочего тела системы. Термодинамические процессы могут быть равновесными и неравновесными, обратимыми и необратимыми. Если изменение состояния термодинамической системы протекает с нарушением ее внутреннего равновесия, то имеет место неравновесный термодинамический процесс. Реальные процессы, наблюдаемые в природе, в эксперименте, в машинах, являются неравновесными, их описание методами термодинамики невозможно. С целью изучения основных свойств систем при обмене энергией с окружающей средой используют подход научной абстракции, идеализируют реальные процессы, принимая их за равновесные. Термодинамический процесс, протекающий с бесконечно малым отклонением состояния системы от равновесного, называется р а в н о в е с н ы м. Понятие об обратимых и необратимых процессах изложено в подпункте 1.1.5. Ниже рассматриваются только равновесные и обратимые термодинамические процессы идеального совершенного газа. Для равновесной термодинамической системы связь между термодинамическими параметрами устанавливается уравнением состояния идеального газа (2.9). Следовательно, это уравнение справедливо и для равновесного термодинамического процесса не только в начальном и конечном состояниях системы, но и в любом промежуточном ее состоянии. В общем случае в процессе могут изменяться произвольно (независимо) два термодинамических параметра из трех. Изучение работы тепловых машин показывает, что наибольший интерес для практики представляют конкретные термодинамические процессы, а именно изменения состояния, протекающие при постоянных давлении, объеме, и температуре, а также без теплообмена с окружающей средой. Их характерной особенностью является то, что для совершенного газа величина теплоемкости на всем протяжении процесса остается неизменной. В термодинамике широко используются графические методы анализа процессов. При этом удобнее использовать не пространственные трехмерные изображения линий, описываемых функцией f(p,v,T), а их двухмерные проекции на одну из трех координатных плоскостей. Как правило, используется графическое изображение термодинамических процессов в координатах pv и Ts, а в особых случаях – в координатах i s; p i; id и др.
В pv и Ts – координатах на рис.2.3 и 2.4 показан произвольный термодинамический процесс изменения параметров от состояния 1 до состояния 2.
Рис 2.3 Рис. 2.4 На рис. 2.3 площадь, ограниченная кривой процесса 1-2, осью абсцисс и крайними ординатами a и b, как было показано в 1.2.5, численно равна работе расширения, а площадь, ограниченная кривой процесса, осью ординат и крайними абсциссами c и d, – технической работе. В Ts - координатах площадь, ограниченная кривой процесса 1-2, осью абсцисс и крайними ординатами а и b, выражается интегралом: F а-1-2- б = Поскольку dq = Tds или q = Так как указанные площади зависят от характера процесса, то теплота и работа являются его функциями. Независимо от особенностей процесс их анализа проводится в определенной последовательности, заключающейся в следующем: – устанавливается характер процесса, назначается постоянный параметр; – с использованием первого закона термодинамики и конкретных особенностей процесса выводится его уравнение; – из уравнения процесса и уравнения состояния выводятся соотношения между термодинамическими параметрами; – указывается способ построения графиков в координатах pv и Ts; – определяется изменение внутренней энергии, энтальпии и энтропии рабочего тела; – записываются выражения для работы расширения; работы технической и теплоты процесса; – устанавливается количественное соотношение между теплотой, изменением внутренней энергии и работой в процессе. Используя указанную последовательность, проведем анализ обобщенного для всех возможных процессов – п о л и т р о п н о г о.
2.3.2. Политропный процесс Определение процесса Термодинамический процесс, протекающий при неизменной теплоёмкости, называется п о л и т р о п н ы м. Название “политропный” происходит от греческих слов “поли” – много и “тропос” – направление, путь. В политропном процессе в общем случае могут изменяться все термодинамические и калорические параметры кроме теплоёмкости, которую обозначают через cп. Вывод уравнения процесса. Для вывода уравнения исполь\ зуем выражение первого закона термодинамики, записанное через энтальпию и внутреннюю энергию: dq = di - vdp и dq = du + pdv. Выразив через теплоемкости записанные выражения, получим: cп dT = cp dT – vdp и cпdT = cv dT + pdv. Отсюда (сп – сp)dT = -vdp и (cп –cv)dT = pdv. Разделим почленно первое уравнение на второе:
Здесь левая часть равенства определяется только теплоемкостью рабочего Разделим почленно первое уравнение на второе:
Проведя разделение переменных, получим:
n После интегрирования этого соотношения в пределах от начала до конца процесса и антилогарифмирования, будем иметь: p1 v1n = p2 v2n. Отсюда следует, что р vn = const. (2.44)
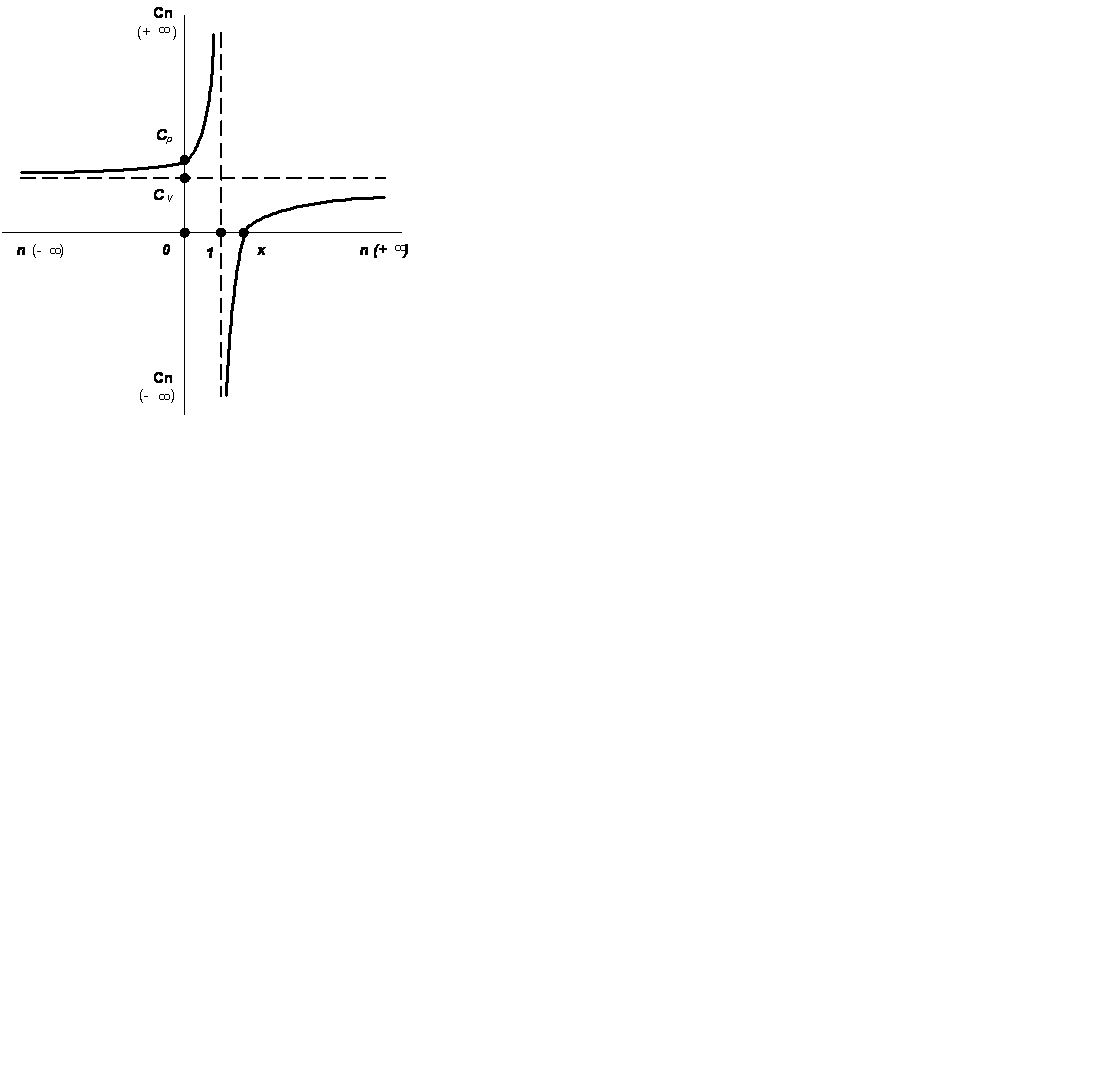
cn = const. Показатель степени n в уравнении называют п о к а з а т е - л е м п о л и р о п ы. Он принимает для каждого сn конкретное числовое значение и, как изображено на рис.2.5, может меняться от - ∞ до +∞. Здесь зависимость теплоемкости политропного процесса от показателя n получена из (2.43) в виде
Рис. 2.5
|
|||||||||||||||
|
Последнее изменение этой страницы: 2017-01-23; просмотров: 140; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.139.97.157 (0.061 с.) |

 . (2.24)
. (2.24) и выражают в Дж/(моль· К).
и выражают в Дж/(моль· К). , (2.25)
, (2.25) – молярная масса газа;
– молярная масса газа;
 . (2.26)
. (2.26) (2.28)
(2.28)
 . (2.31)
. (2.31) R, (2.32)
R, (2.32) R. (2.33)
R. (2.33) t3 +…, (2.34)
t3 +…, (2.34) – числовые коэффициенты.
– числовые коэффициенты. определяются эмпирическим путем.
определяются эмпирическим путем. = 29,02 + 0,00531 t + 0,000000127 t 2, кДж/(моль∙ К).
= 29,02 + 0,00531 t + 0,000000127 t 2, кДж/(моль∙ К). .
. и с из (2.35), получим:
и с из (2.35), получим: . (2.36)
. (2.36) (2.37)
(2.37) (2.38)
(2.38) , cv cм =
, cv cм =  . (2.39)
. (2.39)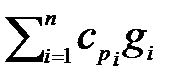 , cv cм =
, cv cм =  (2.40)
(2.40) .
. 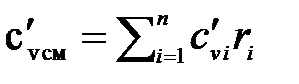 (2.41)
(2.41)
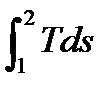 , то F а-1-2-б численно равна подведенной теплоте в процессе.
, то F а-1-2-б численно равна подведенной теплоте в процессе.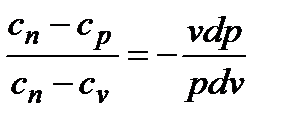 .
. . ( 2.43)
. ( 2.43) .
. Выражение (2.44) называется у р а в н е н и е м п о л и т р о п н ог о п р о ц е с с а. Оно устанавливает связь между параметрами состояния в процессе с теплоемкостью
Выражение (2.44) называется у р а в н е н и е м п о л и т р о п н ог о п р о ц е с с а. Оно устанавливает связь между параметрами состояния в процессе с теплоемкостью . (2.45)
. (2.45)


