
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы очистки коллоидных систем
Приготовленные золи необходимо очищать от содержащихся в них примесей электролитов. Электролиты понижают устойчивость золи и мешают изучению его свойств. Для очистки золей от примесей электролитов применяют несколько методов: диализ, электродиализ, ультрафильтрация, электроультрафильтрация, ультрацентрифу-гирование. Диализ осуществляется в специальных установках – диализаторах, имеющих полупроницаемые мембраны, через которые свободно проходят ионы и молекулы дисперсионной среды, но задерживаются более крупные по размеру коллоидные частицы. Коллоидная система контактирует через полупроницаемую мембрану с растворителем, при этом происходит диффузия ионов через мембрану в растворитель. Периодически меняя растворитель, можно добиться достаточно глубокой очистки коллоидной системы. Диализ протекает очень медленно. Процесс ускоряется под действием электрического поля и применения проточной воды. Подобные усовершенствованные установки называются электродиализаторами. Ультрафильтрацию проводят через полупроницаемые мембраны под давлением или создают разряжение для ее ускорения. При этом дисперсная фаза остается на фильтре, а дисперсионная среда с ионами образует фильтрат. Дисперсную фазу вновь можно перевести в другую чистую дисперсионную среду и получить очищенный золь. Ультрафильтрацию можно комбинировать с электродиализом. Этот комбинированный метод очистки получил название элек-троультрафильтрация. Отделение дисперсной фазы от дисперсионной среды, содер-жащей примеси ионов, можно осуществлять в ультрацентрифугах, ротор которых вращается со скоростью 60000 об/мин и выше. Кювета содержит всего 0,5 мл коллоидного раствора. После осаждения дисперсионную среду осторожно удаляют из кюветы и вносят в нее чистую дисперсионную среду. В современных ультрацентрифугах оседают не только частицы лиофобных золей, но и молекулы белков и другие высокомолекулярные вещества.
МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЕ СВОЙСТВА КОЛЛОИДНЫХ СИСТЕМ Молекулярно-кинетические свойства коллоидных систем связаны с движением частиц дисперсной фазы. Наиболее важными свойствами являются броуновское движения, диффузия, осмос и мембранное равновесие Доннана.
БРОУНОВСКОЕ ДВИЖЕНИЕ Броуновское движение – это беспорядочное, непрекращающееся движение частиц дисперсной фазы, вызываемое тепловым движе-нием молекул дисперсионной среды. Оно впервые описано английским ботаником Р.Броуном (1827). Интенсивность броуновского движения зависит только от температуры, вязкости среды и от размеров частиц. А.Эйнштейном и М.Смолуховским предложено уравнение для определения среднего значения среднеквадратичного смещения
где R – универсальная газовая постоянная; Т – температура золя, К; Вследствие беспорядочности движения необходимо усреднять не сами смещения или их проекции, а квадраты этих величин, так как смещения одинаковой величины, но противоположные по знаку, равновероятны и при усреднении дают нуль.
ДИФФУЗИЯ Диффузия – это самопроизвольный процесс переноса вещества в объеме, приводящий к установлению равновесного распределения концентраций в результате беспорядочного теплового движения частиц дисперсной фазы. Диффузия заканчивается с достижением равномерного распределения частиц по объему. Следовательно, она возможна только в системах, где имеется градиент концентрации. Процесс диффузии подчиняется закону Фика, который описывается следующим математическим уравнением: dm = –D где dm – масса переместившегося вещества; S – площадь сечения, через которое идет диффузия; dt – время; dC/dx – градиент концентрации в направлении переноса вещества; D – коэффициент диффузии. Коэффициент диффузии для шарообразных частиц определяется соотношением: D = где k – постоянная Больцмана; Т – температура; Из последней формулы видно, что коэффициент диффузии, характеризующий скорость диффузии, обратно пропорционален размеру диффундирующих частиц. По этой причине скорость диффузии коллоидных частиц в сотни и тысячи раз меньше, чем скорость диф-фузии в молекулярно (ионно)-дисперсных системах. Определив величину D опытным путем, из формулы для коэффициента диффузии можно найти размер коллоидных частиц.
Диффузия играет важную роль во многих технологических процессах: дублении кожи, выделке меха, крашении тканей и другие. Подчеркивая роль процесса диффузии, коллоидный раствор, образующийся после извлечения сахарозы из сахарной свеклы, называют диффузионным соком.
ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ В коллоидных системах, как и в молекулярно-дисперсных системах, наблюдается явление осмоса. Однако оно менее выражено в коллоидных системах. Например, осмотическое давление 1%-ного раствора сахарозы достигает 6,4∙104Па, а осмотическое давление 1%-ного золя As2S3 при той же температуре составляет всего3,5 Па. Осмотическое давление в коллоидных системах вычисляется по уравнению: Росм= где Небольшое осмотическое давление коллоидных систем позволяет провести процессы очистки различных растворов от содержания в них коллоидных частиц методом обратного осмоса. При этом к растворам, содержащим коллоидные частицы, прилагается внешнее давление, которое выше осмотического давления, вычисленного по приведенному выше уравнению. Дисперсионная среда проходит через полупроницаемую мембрану в другую ее сторону, очищаясь от коллоидных частиц. Обратный осмос используют и в случае, когда необходимо концентрировать коллоидный раствор путем удаления из него растворителя.
|
||||||
|
Последнее изменение этой страницы: 2017-01-26; просмотров: 243; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.218.147 (0.027 с.) |
 шарообразной частицы в определенном, но произвольно выбранном направлении:
шарообразной частицы в определенном, но произвольно выбранном направлении: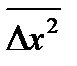 =
=  t,
t, – вязкость дисперсионной среды; r – радиус частицы; N А – число Авогадро; t – время наблюдения.
– вязкость дисперсионной среды; r – радиус частицы; N А – число Авогадро; t – время наблюдения. ,
, ,
, ,
,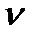 – число коллоидных частиц в объеме V; N А – число Авогадро (N А=6,02∙1023); R – универсальная газовая постоянная; Т – темпера-тура коллоидной системы. Отношение
– число коллоидных частиц в объеме V; N А – число Авогадро (N А=6,02∙1023); R – универсальная газовая постоянная; Т – темпера-тура коллоидной системы. Отношение 


