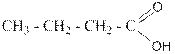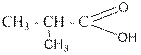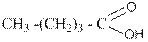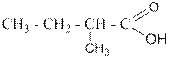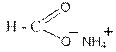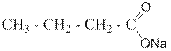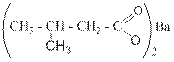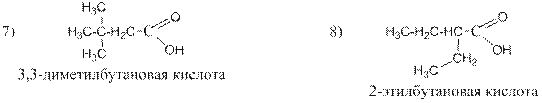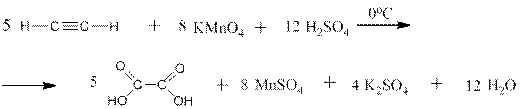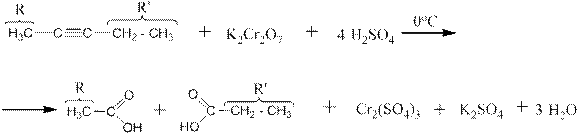Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Получение карбоновых кислот путем окисления органических соединений других классов.Стр 1 из 4Следующая ⇒
Номенклатура карбоновых кислот Таблица №1
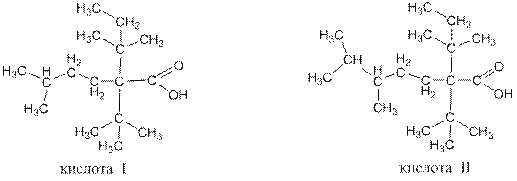
Приведём также пример карбоновой кислоты сложного строения, которую ещё можно назвать по рациональной номенклатуре, не вводя в название цифр (кислота I), и пример кислоты, которую следует называть только по номенклатуре ИЮПАК (кислота II):
Кислота I по рациональной номенклатуре называется трет -бутилизоамил- трет -амилуксусная кислота. По ИЮПАК – 5-метил-2- трет -бутил-2- трет -амилгексановая кислота. Так как в кислоте II радикал слева от карбокильной группы сложен и не имеет узаконенного названия, то эту кислоту можно назвать только по номенклатуре ИЮПАК – 5,6-диметил-2- трет -бутил-2- трет -амилгептановой кислотой. Все карбоновые кислоты образуют соли. Примеры названий солей некоторых карбоновых кислот приведены в таблице № 2 Таблица № 2
Изомерия карбоновых кислот рассмотрена на примере соединений с формулой C6H12O2:
У карбоновых кислот с числом атомов углерода от четырёх и более имеется множество межфункциональных изомеров. Вот некоторые из них с той же общей формулой C6H12O2:
1) Сложные эфиры:
2) Кетоспирты:
3) Альдегидоспирты:
4) Непредельные двухатомные спирты:
5) Непредельные диэфиры и эфиры-спирты:
6) Циклические спирты и эфиры, а так же циклические эфиры-спирты:
Электронное и пространственное строение карбоновых кислот на примере уксусной (этановой) кислоты
Способы получения карбоновых кислот
Номенклатура карбоновых кислот Таблица №1
Приведём также пример карбоновой кислоты сложного строения, которую ещё можно назвать по рациональной номенклатуре, не вводя в название цифр (кислота I), и пример кислоты, которую следует называть только по номенклатуре ИЮПАК (кислота II):
Кислота I по рациональной номенклатуре называется трет -бутилизоамил- трет -амилуксусная кислота. По ИЮПАК – 5-метил-2- трет -бутил-2- трет -амилгексановая кислота. Так как в кислоте II радикал слева от карбокильной группы сложен и не имеет узаконенного названия, то эту кислоту можно назвать только по номенклатуре ИЮПАК – 5,6-диметил-2- трет -бутил-2- трет -амилгептановой кислотой. Все карбоновые кислоты образуют соли. Примеры названий солей некоторых карбоновых кислот приведены в таблице № 2 Таблица № 2
Изомерия карбоновых кислот рассмотрена на примере соединений с формулой C6H12O2:
У карбоновых кислот с числом атомов углерода от четырёх и более имеется множество межфункциональных изомеров. Вот некоторые из них с той же общей формулой C6H12O2:
1) Сложные эфиры:
2) Кетоспирты:
3) Альдегидоспирты:
4) Непредельные двухатомные спирты:
5) Непредельные диэфиры и эфиры-спирты:
6) Циклические спирты и эфиры, а так же циклические эфиры-спирты:
Электронное и пространственное строение карбоновых кислот на примере уксусной (этановой) кислоты
Способы получения карбоновых кислот
Получение карбоновых кислот путем окисления органических соединений других классов. 1.1 Путём газофазного каталитического окисления алканов, например:
1.2 Путём окисления алкенов сильными окислителями в жидкой фазе в кислой среде, например:
1.3 Путём окисления алкинов в тех же условиях, например:
1.4 Путём окисления алкадиенов могут быть получены одновременно две монокарбоновые и одна дикарбоновая кислоты, например:
1.5 Путём окисления алкильных производных бензола, например:
1.6 Путём окисления первичных спиртов сильными окислителями в кислой среде, например:
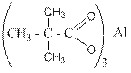
Из третичных спиртов можно получить кислоты наряду с кетонами и углекислым газом. В отличие от окисления первичных и вторичных спиртов, которые окисляются при 0оС, третичные реагируют с теми же окислителями только при нагревании и с разрывом С – С связей рядом со связью С – О, например:
1.7 Путём самопроизвольного окисления альдегидов кислородом воздуха (аутоокисление). Например:
1.8 Путём проведения реакции Канниццаро, например:
Как видно эта реакция является реакцией диспропорционирования альдегидов до кислот и спиртов.
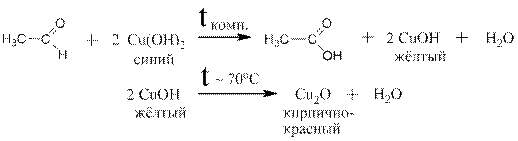
1.9 Путём окисления альдегидов гидроксидом меди (II), например:
Реакция является качественной на альдегиды. 1.10 Путём окисления альдегидов гидроксидом диамминсеребра, например:
Эта реакция носит название реакции «серебряного зеркала» и так же является качественной на альдегиды.
1.11 Путём окисления сложных эфиров. Если в спиртовой части сложного эфира остаток первичного спирта, то получаются две разные кислоты, например:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 980; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.160.154 (0.09 с.) |