Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Условия, необходимые для горения.
Известно, что для возникновения горения необходимо наличие: Воздух и горючее вещество составляют систему, способную гореть, а температурные условия обуславливают возможность самовоспламенения и горения системы. Наибольшая скорость горения получается при горении вещества в чистом кислороде, наименьшая (прекращение горения) – при содержании 14–15% кислорода. Горение веществ может происходить за счет кислорода, находящегося в составе других веществ, способных легко его отдавать. Такие вещества называются окислителями. Приведем наиболее известные окислители. · Бертолетова соль (KClO3). · Калийная селитра (KNO3). · Натриевая селитра (NaNO3). В составе окислителей содержится кислород, который может быть выделен путем разложения соли, например: 2 KClO3 = 2KCl + 3 O2 Разложение окислителей происходит при нагревании, а некоторых из них даже под воздействием сильного удара. 2. Продукты горения. Полное и неполное сгорание. Экологические аспекты процессов горения. В процессе горения образуются продукты сгорания. Состав usшвисит от горящего вещества и условий горения. Продукты сгорания, за исключением окиси углерода, гореть не способны. Дым, образующийся при горении органических веществ, содержит твердые частицы и газообразные продукты (углекислый газ, окись углерода, азот, сернистый газ и другие). В зависимости от состава веществ и условий их горения получается различный по содержанию дым. Дымы, образующиеся при горении разных веществ, отличаются не только составом, но цветом и запахом. По цвету дыма можно определить, какое вещество горит, хотя цвет дыма изменяется в зависимости от условий трения. При горении древесины дым имеет серовато-черный пнет; бумаги, сена, соломы — беловато-желтый; ткани и хлопка— бурый; нефтепродуктов — черный и т. д. Продукты горения – это газообразные, жидкие или твердые вещества, образующиеся в процессе горения. Состав продуктов сгорания зависит от состава горящего вещества и от условий его горения. Органические и неорганические горючие вещества состоят, главным образом, из углерода, кислорода, водорода, серы, фосфора и азота. Из них углерод, водород, сера и фосфор способны окисляться при температуре горения и образовывать продукты горения: СО, CO2, SO2, P2O5. Азот при температуре горения не окисляется и выделяется в свободном состоянии, а кислород расходуется на окисление горючих элементов вещества. Все указанные продукты сгорания (за исключение окиси углерода СО) гореть в дальнейшем больше не способны. Они образуются при полном сгорании, то есть при горении, которое протекает при доступе достаточного количества воздуха и при высокой температуре.
Углекислый газ или двуокись углерода (СО2) – продукт полного горения углерода. Не имеет запаха и цвета. Горение магния, например, происходит в атмосфере углекислого газа по уравнению: CO2 +2 Mg = C + 2 MgO. При концентрации углекислого газа в воздухе, превышающей 3-4.5%, нахождение в помещении и вдыхание газа в течение получаса опасно для жизни. Оксид углерода или угарный газ (СО) – продукт неполного сгорания углерода. Этот газ не имеет запаха и цвета, поэтому особо опасен. Сернистый газ (SO2) – продукт горения серы и сернистых соединений. Бесцветный газ с характерным резким запахом. Дым При горении многих веществ, кроме рассмотренных выше продуктов сгорания выделяется дым – дисперсная система, состоящая из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе. При неполном сгорании органических веществ в условиях низких температур и недостатка воздуха образуются более разнообразные продукты – окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные химические соединения. Они получаются при частичном окислении как самого горючего, так и продуктов его сухой перегонки (пиролиза). Эти продукты образуют едкий и ядовитый дым. Кроме того, продукты неполного горения сами способны гореть и образовывать с воздухом взрывчатые смеси. Такие взрывы бывают при тушении пожаров в подвалах, сушилках и в закрытых помещениях с большим количеством горючего материала. Рассмотрим кратко свойства основных продуктов горения.
Экологические аспекты процессов горения. Применение природного газа позволяет уменьшить загрязнение атмосферы оксидам серы, твердыми частицами и окисью углерода, однако в атмосферу поступает большое количество оксидов азота, окиси углерода и канцерогенных веществ (3,4-бенз(о)перен). Правильная организация горения, выбор рациональных способов сжигания позволяет свести к минимуму образование вредных веществ и выделение их в воздушный бассейн. Использование природного газа позволяет вести не только пассивную, но и активную борьбу за чистоту воздуха: использование установок для дожигания, использование выбросных газов для подачи в газовый горелки вместо соответствующего количества воздуха. Экологические проблемы горения. Задача – не навредить при сжигании топлив. Негативные проявления: -Техногенное тепловыделение соизмеримо с компонентами теплового баланса атмосферы; - Акустический шум турбулентных пламен при работе авиационных и ракетных двигателей – загрязнитель окружающей среды. - Выброс вредных продуктов сгорания – окислов азота, окислов металлов, угарного газа (при высоких Тг), окислов серы, канцерогенных веществ – продуктов неполного пиролиза органических горючих, сажи, углекислого газа (при низких Тг) – является причиной: изменения оптических свойств атмосферы и уменьшения потока солнечного излучения, возникновения кислотных дождей, усиления «парникового эффекта», разрушения озонового слоя Земли, негативного воздействия на флору и фауну, здания и конструкции. Общий итог: глобальное потепление, климатические катастрофы (циклоны, бураны, смерчи, цунами, наводнения, засухи, сходы лавин, сели).. 3. Уравнения горения веществ в кислороде и на воздухе, методика их составления. Термодинамика процессов горения. Тепловые эффекты реакций горения. Общее уравнение реакции горения любого углеводорода Тепловой эффект (теплота сгорания) Q — количество теплоты, выделяющееся при полном сгорании 1 кмоля, 1 кг или 1 м3 газа при нормальных физических условиях. Различают высшую Qв и низшую Qн теплоту сгорания: высшая теплота сгорания включает в себя теплоту конденсации водяных паров в процессе горения (в реальности при сжигании газа водяные пары не конденсируются, а удаляются вместе с другими продуктами сгорания). Обычно технические расчеты обычно ведут по низшей теплоте сгорания, без учета теплоты конденсации водяных паров (около 2400 кДж/кг).
1. Н + О2 —› ОН + О Итог единичного цикла: Термодинамика горения Исходный состав горючей смеси характеризуется молярными или массовыми долями компонентов и начальными давлением и температурой. Если состав смеси подобран так, что при её сгорании и горючее, и окислитель полностью преобразуются в продукты реакции, то такая смесь называется стехиометрической. Смеси с избытком топлива называются богатыми, а с недостатком топлива — бедными. Степень отклонения состава смеси от стехиометрического характеризуется коэффициентом избытка топлива (англ. equivalenceratio)[35]:
где YF и YO — массовые доли топлива и окислителя соответственно, а (YF / YO)st — их отношение в стехиометрической смеси. В русскоязычной литературе используется также коэффициент избытка окислителя (или воздуха), обратный коэффициенту избытка топлива.
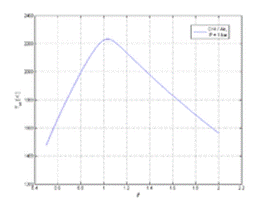
Адиабатическая температура горения смесей CH4 с воздухом в зависимости от коэффициента избытка топлива. P = 1 бар, T0 = 298,15 K. Если горение происходит адиабатически при постоянном объёме, то сохраняется полная внутренняя энергия системы, если же при постоянном давлении — то энтальпия системы. На практике условия адиабатического горения приближённо реализуются в свободно распространяющемся пламени (без учёта теплопотерь излучением) и в других случаях, когда потерями тепла из зоны реакции можно пренебречь, например, в камерах сгорания мощных газотурбинных установок или ракетных двигателей. Адиабатическая температура горения — это температура продуктов, достигаемая при полном протекании химических реакций и установлении термодинамического равновесия. Для термодинамических расчётов используются таблицы термодинамических функций[36] всех компонентов исходной смеси и продуктов. Методы химической термодинамики позволяют рассчитать состав продуктов, конечное давление и температуру при заданных условиях сгорания. В настоящее время доступно много программ, способных выполнять эти расчёты[37][38].
Теплота сгорания — это количество теплоты, выделившейся при полном сгорании исходных компонентов, то есть до CO2 и H2O для углеводородных топлив. На практике часть выделившейся энергии расходуется на диссоциацию продуктов, поэтому адиабатическая температура горения без учёта диссоциации оказывается заметно выше той, что наблюдается на практике[39]. Термодинамический расчёт позволяет определить равновесный состав и температуру продуктов, но не даёт никакой информации о том, с какой скоростью система приближается к равновесному состоянию. Полное описание горения требует знания механизма и кинетики реакций и условий тепло- и массообмена с окружающей средой.
4. Типы пламени и скорость горения. Теории горения: тепловая, цепная, диффузионная. В общем случае скорость горения зависит от скорости смешения исходных компонентов в зоне прогрева и зоне реакции (для гетерогенных систем), от скорости химических реакций между компонентами, от скорости передачи тепла и активных частиц из зоны реакции к исходной системе. Нормальная скорость горения (и тем более форма фронта горения) зависит от условий течения свежей смеси и продуктов горения (особенно при горении в двигателях). Поэтому в теории горения рассматривается несколько основных типов пламен. Они неодинаковы по своему научному и практическому значению и степени изученности. Неодинаковы параметры, представляющие наибольший интерес для данного типа пламени. Существенно отличается подход к теоретическому рассмотрению каждого типа пламени. Некоторые различия имеются и в экспериментальных методах. Перечислим наиболее важные для теории горения типы пламен: 1) ламинарное пламя в гомогенной газовой смеси. К этому же типу относится пламя при горении летучих взрывчатых веществ; 2) ламинарное диффузионное пламя при горении струи горючего газа в окислительной атмосфере. К этому типу примыкает пламя при диффузионном горении жидкого горючего, налитого в цилиндрический сосуд, и т. п.; 3) пламя при горении капли жидкого горючего или частицы твердого горючего в окислительной атмосфере; 4) турбулентные пламена в гомогенных или в предварительно не смешанных газовых смесях; 5) пламя при горении нелетучих взрывчатых веществ, порохов и т. д. в тех случаях, когда существенную роль играет реакция в конденсированной фазе. Коротко рассмотрим некоторые характеристики основных типов пламен в той мере, в какой это полезно для понимания закономерностей горения конденсированных смесей.
Предварительно следует остановиться на определении скорости горения. При ламинарном горении газовых смесей и гомогенных конденсированных систем большое принципиальное значение имеет понятие нормальной скорости горения (uн). По определейию, uн равна скорости перемещения пламени относительно свежей смеси в направлении, перпендикулярном поверхности пламени в данной точке. Размерность uн в системе СИ - м/сек, однако для скорости горения эта единица пока употребляется редко и только для газовых систем. Обычно величину uн для газовых систем выражают в см/сек, а для конденсированных систем в мм/сек (если выражать скорость горения конденсированных систем в м/сек, то в обычном диапазоне давлений получаются очень малые дробные числа). Для гомогенных конденсированных систем чаще всего измеряется скорость горения цилиндрических зарядов, горящих с торца, причем фронт горения полагается плоским (опыт показывает, что в большинстве случаев при наличии надлежащей оболочки это допущение справедливо, и искажения наблюдаются лишь на краях заряда). К тому же для твердых веществ (и достаточно вязких жидких веществ) исходное (твердое или жидкое) вещество неподвижно во время горения. Поэтому в данном случае нормальная скорость горения просто равна видимой скорости пламени (в лабораторной системе координат) и постоянна в различных точках заряда.
|
|||||||||||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 10842; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.190.167 (0.026 с.) |