Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методика применения двойного расходящегося штифта.
Требуемая длина и сечение штифта определяется заранее при помощи калибровочной пластины-линейки. Стержни, составляющие штифт, моделируются (изгибаются) при помощи
специального станка, выполненного в виде металлического бруска с прорезями (рис. 19). Затем штифт стерилизуется в разобранном виде. На операционном столе штифт собирается: упругие изогнутые стержни обращаются друг к другу выпуклой стороной, заостренные концы стержней скрепляются в замке. Противоположные концы „ _ Рис. 19. Моделирование стержня стержней сближаются с некоторым При помощи станка усилием вручную и скрепляются колпачком-насадкой. После осуществления доступа и репозиции штифт в собранном виде вводится в костномозговую полость центрального, а затем и периферического отломка (правильность вхождения контролируется по предложенному нами способу электроиндикации). При остеосинтезе двойным расходящимся штифтом с продольным каналом под проводник и кольцом на конце (2-й вариант) после репозиции в костномозговую полость вначале вводится проводник, проводится индикация правильности его вхождения, а затем по проводнику вводится штифт. После этого снимается колпачок-насадка, ударом по
стержню, имеющему на конце конусную шпонку (во 2-м варианте - кольцо), стержень (не имеющий кольца) продвигается вниз по костномозговой полости. Стержни освобождаются друг от друга, концы расходятся в стороны, принимая заданное пространственное расположение. Попеременными ударами молотка стержни раздельно окончательно низводятся в периферический фрагмент (рис.20).
I г Рис.20. Схема остеосинтеза: а - введение по проводнику; 6 разъединение стержней; в - остсосинтез завершен а б в Таким образом, двойной расходящийся штифт нашей конструкции, в собранном виде имея прямую форму, как бы обладает "памятью формы". Это позволяет, как показали наши экспериментальные и клинические исследования, надежно фиксировать диафизарные переломы различной локализации, включая часто встречающиеся переломы в нижней трети голени, за счет плотного прилегания упругих изогнутых стержней, имеющих различную, соответственно кривизне стенок костномозговой полости, пространственную направленность, к стенкам костномозговой полости периферического фрагмента.
Использование модифицированных стандартных штифтов. При поперечных и косопоперечных переломах в средней трети голени, наряду с двойным расходящимся штифтом, в клинике целесообразно использовать стандартные штифты. Их необходимо лишь предварительно подвергнуть несложной рационализации (рис.21).
ближе к заостренному концу на металлическом
прутке диаметром 3,5 мм. г~_^ 4f it
Такое техническое решение было предложе- НО и внедрено в Рис 2] Рационализация стандартных штифтов: и А.Г. Суваляном (1979) в виде самостоятельной конструкции. Наше предложение отличается лишь тем, что адаптация уже имеющегося в наличии стандартного штифта к проводнику осуществляется в течение нескольких минут в условиях отделения. (Внимание! Не следует сужать штифт слишком далеко от заостренного конца. Иначе между проводником и штифтом образуется «утиный клюв», в котором может ущемиться кортикальный слой периферического фрагмента синтезируемой кости.) Рационализация штифта Кюнчера производится путем сужения одного из концов на прутке диаметром 3,5 мм для предотвращения выхождения проводника в прорезь штифта при остеосинтезе. Кроме того, следует сточить противоположную прорези кромку конца штифта, иначе она может отталкивать периферический фрагмент. Другой конец необходимо изогнуть под утлом 15-20° rvia облегчения удаления штифта после срастания перелом. Таким образом, стандартный штифт Кюнчера для остеосинтеза бедра становится пригодным для закрытого интрамедуллярного остеосинтеза диафизарных переломов голени, особенно с диаметром костномозговой полости 10 и более мм. Необходимо отметить важность такой, казалось бы, незначительной "мелочи", как формирование данных изгибов. Отсутствие изгиба (или, как обычно бывает, недостаточный угол изгиба) кпереди на проксимальном конце не препятствует проведению остеосинтеза, но по завершении операции конец штифта неизбежно оказывается в полости сустава, смещаясь кзади, в зону межмыщелкового возвышения. Кроме неизбежного в таких случаях выраженного гемартроза коленного сустава
(поскольку нарушается принцип внесуставного доступа по Alms) возникают значительные трудности при удалении конструкции. Можно только посочувствовать и пациенту и оператору в данной ситуации, когда цена 2-3 ударов молотка год назад при подготовке к операции синтеза, неожиданно становится столь высокой. Простое удаление может превратиться в настоящий многочасовой кошмар. Впрочем, используя наши способы, и в данном случае можно добитьбся минимизации отрицательных эффектов (см. ниже раздел «Электроиндикатор»). Способы блокирования стандартных штифтов. Стандартные штифты могут использоваться и для остеосинтеза часто встречающихся переломов с локализацией ниже места сужения костномозговой полости, благодаря нашей методике блокирования их спицами. Разработаны два варианта блокирования.
Первый вариант показан для фиксации низких переломов с локализацией в расширенной части большеберцовой кости и позволяет добиться прочной фиксации при использовании обычных штифтов. В костномозговую полость дистального фрагмента по передневнутренней поверхности голени через один кортикальный слой предварительно засверливаются спицы. В последующем интрамедуллярный фиксатор, встречаясь со спицами, заклинивается, или блокируется (рис.22).
А 6 в Рис. 22. Вторично-открытый оскольчатый перелом голени (а). Произведен ЗИОС с блокированием штифта (б). Результат через гол (в). Больной Р-р, и.б.2239
Способ предельно прост и не требует создания (в отличие от зарубежных аналогов) сложных прицельных устройств, практически атравматичеи и обеспечивает быстрое востановление функции (рис. 23, 24).
Рис. 23. Функция через 4 дня после операции (рентгенограммы
представлены на рис.22)
При локализации перелома в верхней трети кости используется второй вариант блокирования, предложенный С.А.Карауловым. Последовательность проведения остеосинтеза следующая: вначале поперечно через оба кортикальных слоя кости во фронтальной плоскости засверливается блокирующая спица выше линии перелома на 2-2,5 см (рис. 25), которая делит костномозговую полость на два отдела: передний и задний (рис. 26, б). Пробойником проводится трепанация большеберцовой кости по Alms в положении сгибания голени. Конец пробойника должен попасть в передний отдел, между гребнем и блокирующей спицей. Затем в трепанационный канал вводится слегка изогнутый, согласно строению кости, металлический проводник, также проходящий между спицей и передней стенкой кости. По проводнику забивается штифт (рис.26, а). Такое взаимное расположение штифта и спицы препятствует типичному смещению центрального фрагмента кпереди из-за тяги четырехглавой мышцы за собственную связку надколенника (рис.27).
Рис. 26. Схема второго варианта блокирования: а - введение шитифта по проводнику; 6 - поперечный разрез на уровне блокирующей спицы
(увеличение 1:4), где 1 - проводник, 2 - штифт, 3 - блокирующая спица
Рис. 27. Остеосинтез «высокого» перелома завершен. Блокирующая спица предотвращает смещение центрального фрагмента кпереди (схема дана в двух проекциях) Успех обоих вариантов блокирования подтверждается электроиндикацией. Блокирующие спицы после отжатия мягких тканей скусываются и погружаются под кожу. При удалении конструкций после срастания перелома вначале следует удалить штифт, а затем блокирующую спицу. Сложная ситуация может возникнуть при нередко встречающейся анатомо-физиологической особенности строения большеберцовой кости - узкой костномозговой полости при тонкой кости вообще. Проблема заключается в том, что тонкий штифт (8-7 мм) не в состоянии обеспечить прочное скрепление фрагментов сломанной кости и операция теряет смысл. Для данных случаев нами, совместно с А.В.Марковым, разработан способ закрытого комбинированного остеосинтеза, когда после закрытого введения штифта накладывается облегченный аппарат внешней фиксации (Илизарова, Калнберза и др.). Проводник. Применялся в экспериментах при использовании 2-го варианта двойного расходящегося штифта, а в клинике используется и при использовании двойного расходящегося и модифицированных стандартных штифтов. В клинике применяется пруток диаметром 3 мм и длиной 800 мм. В качестве материала для его изготовления оптимальным является титановый сплав ВТ-14, обладающий необходимой упругостью и прочностью, однако он может быть изготовлен из нержавеющей стали (проволока). Если необходим проводник большего диаметра (4 мм), то самым приемлемым материалом может быть рамка для проявки рентгенограмм, соответственно отслужившая свой срок по прямому назначению. Электроиндикатор. Точное попадание проводника и затем штифта в костномозговую полость периферического фрагмента всегда являлось узловым и в то же время наиболее трудным элементом операции закрытого интрамедуллярного остеосинтеза, определяющим успех вмешательства (G.Kuntscher, 1953; 1964; K.Herzog, 1958). При использовании рентгенографии для контроля за ходом вмешательства необходимо произвести от 4 до 8, а в некоторых случаях и более, рентгеновских снимков на операционном столе (М.Я.Баскевич, 1969; Н.Я.Прокопьев, 1976; А.А.Овечкин, 1980; G.Kuntscher, 1950). Это занимает более 30% времени операции, затрудняет ее и ведет к большому расходу дорогостоящей серебросодержащей рентгеновской пленки.
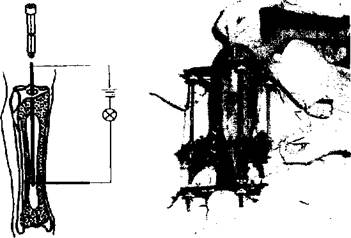
Применение электронно-оптических преобразователей (ЭОП) рентгеновских лучей позволило значительно облегчить контроль правильности вхождения, но не решило всех проблем- Так, если в начале применения преобразователей сообщалось о низкой лучевой нагрузке и больших удобствах для хирурга (N.R.Crozzoli, 1963; F.Baumgarti, 1964; J.Behler, 1965), то затем было установлено, что лучевая нагрузка остается, особенно при систематическом применении метода, достаточно высокой, поэтому необходимы меры предосторожности и защиты (N.Klatnek, 1965; K.Haage et al., 1976; M.Van der Chinst et al., 1977). Близкое расположение тубусов рентгеновской аппаратуры, как обычной, так и ЭОП, к операционному полю затрудняет соблюдение правил асептики (H.Colbke, H.R.Mittelbach, 1975; S.Banerle, 1976; U.Pfister, 1976). Немаловажным обстоятельством является также сложность и высокая стоимость электронно-оптических преобразователей. При решении проблемы нерентгеновского интраопера-ционного контроля был создан-способ закрытого интрамедуллярного остеосинтеза (авторы В.П.Бойков и С.П.Карпов, приоритет 30.03.1983) и его вариант для лечения переломов голени. Целью изобретения является облегчение и упрощение выполнения закрытого интрамедуллярного остеосинтеза, сокращение времени операции и предотвращение риска облучения больного и персонала путем исключения многократного рентгеновского обследования в ходе остеосинтеза. Суть способа заключается в том, что о ключевом моменте операции - правильном вхождении проводника и штифта в костномозговую полость периферического отломка -судят по замыканию электрической цепи (рис.28, а). Для этого, после закрытой аппаратной или ручной репозиции отломков, в костномозговую полость периферического фрагмента вводится контактная спица. Вводимый затем проводник соприкасается с ней, что регистрируется туг же, на операционном столе. Затем по проводнику вводится штифт и аналогично по срабатыванию электроиндикатора определяется правильность его вхождения. После этого удаляется контактная спица и производится окончательное низведение штифта. Таким образом, исключается сложное, длительное и дорогостоящее неоднократное рентгеновское обследование в ходе операции, неизбежное при
электроиндикатора. Кроме того, при использовании стандартных модифицированных штифтов индикаторные спицы являются одновременно блокирующими. В то же время между спицами по вертикали должно быть некоторое расстояние, около 5 мм, для исключения их контакта между собой.
Электроиндикатор состоит из источника тока (1 -2 элемента питания типа МАРС, КВАНТ и т.п. напряжением 1,45-1,5 вольт), индикатора тока (возможно использование электрической лампочки или звонка), проводов и контактной спицы. В качестве индикатора можно использовать электрический карманный фонарь, в качестве контактных проводов - любой металлический провод с изоляцией, возможно применение стоматологической или медицинской серкляжной проволоки. В качестве контактной спицы используются спицы, выпускающиеся медицинской промышленностью, диаметром 1,5-2 мм. Методика электроиндикации. Отступив 1,5-2 см ниже периферического фрагмента, войти в костномозговую полость и упереться в следующий слой, что ощущается как «провал» с последующим упором. Затем'через трепанационное отверстие сверху заводится проводник и после ручного сопоставления отломков продвигается через линию перелома в костномозговую полость периферического фрагмента. Свободные концы проводника и контактной спицы присоединяются проводами к электроиндикатору стерилизованными проводами. При правильном вхождении проводника он соприкасается в костномозговой полости периферического фрагмента с контактной спицей, что регистрируется по загоранию лампочки или срабатыванию электрического звонка индикатора. Затем контакт от проводника отсоединяется и при максимально согнутой в колене конечности по проводнику забивается прямой одиночный или двойной расходящийся штифт до соприкосновения с контактной спицей. Контакт электроиндикатора присоединяется к выступающему концу штифта. По загоранию лампочки определяется правильность вхождения штифта. Затем удаляется контактная спица, отсоединяется контакт от штифта и производится окончательный остеосинтез. Использование электроиндикации не ограничивается контролем попадания проводника и штифта в периферический фрагмент. Ею удобно пользоваться для интраоперационной диагностики возможного диастаза (рис. 31) и при поиске конца штифта при его удалении после перелома (рис. 32). Возможно применение электроиндикаторов двух типов: со световой и звуковой индикацией. Например, световой индикатор, состоящий из источника постоянного тока (1 -2 элемента питания типа МАРС, КВАНТ) и электрической лампочки, находится вне операционного поля и присоединяется к контактной спице и проводнику (а затем к штифту) стерилизованными проводами. Звуковой индикатор (рис.28, о) во время операции оборачивается стерильным материалом и используется непосредственно на операционном столе. В последние годы мы используем стерилизацию в парах формалина. * * * Таким образом, проведенные экспериментальные и клинические исследования позволили создать высокоэффективные способы, инструментарий и приспособления для осуществления закрытого интрамедуллярного остеосинтеза диафизарных переломов голени. Закрытый интрамедуллярный остеосинтез требует наличия специального инструментария и приспособлений для подготовки к выполнению операции. Несомненно, это вызывает определенные трудности при внедрении методики в практику работы специализированного отделения. В то же аремя прогресс медицины вообще, и травматологии в ч#еюности, немыслим без создания нового высокоэффективного инструментария. Только его наличие позволяет добиться качественного улучшения результатов лечения. Разрабатывая собственную методику закрытого интрамедуллярного остеосинтеза диафизарных переломов голени, мы стремились создать не только набор специального инструментария, но и достичь максимальной эффективности, универсальности и простоты предлагаемых нами конструкций. Поэтому при помощи этого инструментария можно производить остеосинтез не только диафизарных переломов голени, но и, с небольшими изменениями методики по его использованию, производить закрытую интрамедуллярную фиксацию других длинных трубчатых костей. Так, в клинике нами с успехом используется способ репозиции при помощи репонирующе-фикси- рующего аппарата для закрытого остеосинтеза бедренной, аче-чевой кости и костей предплечья; для остеосинтеза переломов бедра использовался двойной расходящийся штифт, широко использовалась при этих операциях электроиндикация, а для подготовки к остеосинтезу - калибровочная пластина-линейка. Данные наблюдения не включены нами в настоящее исследование и приводятся с целью показать универсальность основных положений созданной методики и инструментария для ее выполнения. 2.2. Методика остеосинтеза Проведенные нами теоретические исследования, а также разработанные способы, инструменты и приспособления позволили не только решить проблемы, возникающие при лечении диафизарных переломов голени закрытым способом, но и создать собственную методику закрытого интрамедуллярного остеосинтеза. В основу методики были положены следующие основные принципы, отличающие ее от других известных методик закрытого интрамедуллярного остеосинтеза диафизарных переломов голени (Кюнчера, Раша, Лоттеса, Охотского, Ключевского и др.): 1. Одновременное предварительное определение основных размеров синтезируемой кости и фиксатора. 2. Аппаратная управляемая закрытая репозиция при осколь-чатых, двойных и несвежих (более 3 недель) переломах со смещением. 3. Использование интрамедуллярных фиксаторов, адаптированных к кости, а также способов стабильного остеосинтеза при помощи обычных фиксаторов, при безусловном отказе от рассверливания костномозговой полости. 4. Минимальный объем рентгеновского контроля в ходе операции (применение электроиндикации). 5. Использование оригинальной методики мануальной терапии в системе ранней послеоперационной реабилитации. Начало разработки движений в суставах оперированной конечности при функциональном раннем лечении опережает по срокам начало осевой нагрузки. Предлагаемая нами методика имеет два варианта: 1) остеосинтез свежих переломов; 2) остеосинтез переломов с нарушенной консолидацией. 2.2.1. Остеосинтез свежих переломов При выработке показаний и противопоказаний к применению нашей методики учитывалось как наличие высокоэффективного специального инструментария, так и состояние больного, с учетом общих и местных факторов. Показания 1. Все виды безоскольчатых закрытых диафизарных переломов голени на различных уровнях - поперечные, косопоперечные, косые, винтообразные. 2. Те же виды переломов с наличием одного крупного осколка или при сохранности одной стенки "трубки" болыиеберцовой кости даже при многооскольчатом переломе. 3. Двойные переломы диафиза (несмещенные и со смещением). 4. Вторично и первично-открытые переломы с теми же характеристиками, что и в пп. 1 и 2, после первичного заживления раны мягких тканей голени. Противопоказания можно условно разделить на противопоказания общего и местного характера. Общие противопоказания 1. Общее тяжелое состояние больного, обусловленное декомпенсацией функции внутренних органов. 2. Применение интрамедуллярного остеосинтеза в возрасте до 16 лет может привести к повреждению ростковых зон болыиеберцовой кости с последующим нарушением ее роста. Противопоказания местного характера \. Многоосколь'*а:ые, мелкооскольчатые и раздробленные переломы. 2. Переломы, сопровождающиеся повреждением сосудов и нервов в зоне перелома, что требует оперативной ревизии сосудисто-нервного пучка. 3. Первично и вторично-открытые переломы с незажившей раной мягких тканей. 4. Плохое состояние кожи в зоне предполагаемого разреза (область коленного сустава). Плохое состояние кожи в зоне перелома - варикоз, осад нения, пузыри, кожные заболевания без гнойного отделяемого, не является противопоказанием к операции. Это важное преимущество закрытого интрамедуллярного остеосинтеза перед другими оперативными способами лечения диафизарных переломов голе- ни. В наших наблюдениях у 62 больных в зоне перелома к моменту операции наблюдались осаднения, что не помешало успешно произвести остеосинтез. Малотравматичность и незначительная шокогенность метода позволила расширить показания к его применению у лиц пожилого возраста, а также у ряда больных, страдающих тяжелыми хроническими заболеваниями (гипертоническая болезнь, ревматоидный полиартрит, туберкулез, хроническая неспецифическая пневмония), которые наблюдались у 43 наших больных. Методика может быть применена по сокращенным показаниям в случае неполного набора инструментария и приспособлений. Поперечные и косопоиеречные, с короткой линией излома, переломы в средней трети диафиза большеберцовой кости могут быть репонированы вручную и фиксированы стандартными и модифицированными штифтами ЦИТО или Кюнчера. При поступлении больному накладывается скелетное вытяжение или гипсовая лонгета в зависимости от характера перелома, определяющего с,мещаемость или относительную устойчивость отломков. В большинстве случаев, за редкими исключениями, наиболее целесообразно наложить именно скелетное вытяжение. Во-первых, вытяжение в возвышенном положении ликвидирует смещение по длине и частично другие виды смещений, что благоприятно сказывается на состоянии травмированной конечности в виде снижения болевого синдрома, уменьшения отека. Во-вторых, конечность доступна наблюдению за наличием фликтен, состоянием швов при открытых переломах и соответственно манипуляциям. В-третьих, больной на собственном опыте в течение относительно короткого промежутка времени убеждается в субъективных (здесь мы не говорим об объективных) недостатках такого метода лечения. И, наконец, данный метод лечения может оказаться основным по субъективным (отказ от оперативного лечения) или объективным причинам. В этом плане особо хочется отметить необходимость тщательного выполнения всех классических правил этого устаревшего, отошедшего на второй план, но зарекомендовавшего себя метода консервативного лечения. Операция производится, как правило, на 3-5-й день со дня поступления. За это время проходят боли, уменьшается отек конечности, улучшается общее самочувствие больного. Этот период используется для подготовки к операции: готовится необходимый инструментарий, совместно с анестезиологом производится лабораторное и клиническое обследование больного. В ряде случаев операция может быть произведена в более поздние сроки. При сочетанной или множественной травме (56 случаев) больных чаще всего оперировали через 2-4 недели после выхода тяжелого состояния и нормализации основных показателей гомеостаза организма. При вторично-открытых переломах (47 случаев), когда рана мягких тканей чаще всего является небольшой по размерам или точечной, уже на 5-е сутки при отсутствии признаков воспаления становится очевидным, что противопоказаний к операции нет. Однако необходимо отметить, что полноценная первичная хирургическая обработка с обкалыванием раны антибиотиками является обязательной. Естественно, что лечение идет под постоянным прикрытием антибиотиками. Часто при этом швы на коже еще не сняты и поэтому после обработки кожных покровов зона швов изолируется подшиванием салфетки, смоченной спиртом. Если у больного имеется первично-открытый перелом, то методом выбора является, несомненно, аппаратная внешняя фиксация после первичной хирургической обработки. При подготовке к операции ЗИОС основные параметры большеберцовой кости определяются при помощи калибровочной пластины-линейки (см. рис. 1-6), что дает возможность подобрать штифт необходимых размеров. На операцию стерилизуется минимум еще 2 штифта, с диаметрами сечения на 1 мм больше и меньше основного. Репонирующе-фиксирующий аппарат также монтируется заранее, соответственно локализации перелома и размерам голени. Больного доставляют в операционную с вытяжением на шине или в гипсовой лонгете, наложенной при поступлении. Операцию целесообразно производить под общим интубационном наркозом, но вполне уместно использование перидуральной или спинномозговой анестезии, особенно при противопоказаниях к интубации. Нами только у 3 пациентов была применена внутрикостная регионарная анестезия. Мы
убедились в преимуществах общего иитубационного наркоза при выполнении остеосинтеза по нашей методике, как наиболее управляемого и обеспечивающего наилучшую глубину анестезии. Однако профессионально выполненная перидуральная или спинномозговая анестезия также имеет свои преимущества. Во время операции больной находится в положении на спине. В дистальный фрагмент кости по передневнутренней поверхности в перпендикулярном направлении под разными углами засверливаются от 2 до 5 контактных спиц Киршнера через один кортикальный слой. Упор спицы в противоположный слой после ощущения «провала» служит сигналом к прекращению сверления. Чем шире костномозговая полость, тем большее количество спиц требуется засверлить; при переломах в нижней трети используется максимальное число спиц. Спицы не должны соприкасаться, и поэтому они засверливаются в разных плоскостях, т.е. примерно на 0,5 см друг от друга по вертикали, иначе могут быть ошибки при электроиндикации (рис.33). При использовании прямого штифта некоторые из этих спиц в ходе операции станут блокирующими. Не следует лользоваться толстыми (1,8-2 мм) спицами, для блокирования наиболее удобны именно спицы Киршнера диаметром 1,5 мм. Небходимо обязательно дополнительно сделать 3-5 сквозных, через оба кортикальных слоя, отверстия в дистальном фрагменте с целью превентивной декомпрессии (профилактика жировой эмболии). Доступ к «площадке», расположенной экстрасиновиально в области переднего края проксимального эпифиза болынеберцовой кости, производится по Alms: конечность максимально согнута в коленном суставе. Через разрез мягких тканей вдоль собственной связки надколенника длиной не более 2-3 см трепанируется костномозговая полость большеберцовой кости. Расположение разреза медиально или латерально от связки зависит от направленности линии излома большеберцовой кости, на что указывал еще автор доступа M.Alms (1962). Например, если линия излома расположена классически, снаружи кнутри, доступ должен осуществляться медиально от собственной связки и в последующем возможность выхода проводника в щель перелома будет минимальной, и наоборот. Мы установили, что имеется зависимость также от возможного наличия и характера расположения крупных осколков (рис.29). В нижнем углу раны рассекается фиброзная капсула сустава на протяжении 1-1,5 см. Пробойником вскрывается костномозговая полость большеберцовой кости. При этом, с целью профилактики перфорации задней стенки кости, пробойник вначале устанавливается под углом примерно 60° к оси кости и внедряется в эпифиз на 2-3 см. Затем противоположный конец пробойника отводится назад, с целью некоторого выдвижения голени вперед, и трепанируется костномозговая полость. Пробойник устанавливают строго по оси большеберцовой кости (рис.30 и 34). Затем, после удаления трепана, при помощи слегка изогнутой на тупом конце спицы производится «ощупывание» стенок костномозговой полости (обязательно всех трех!), при этом слышен характерный хруст. Этот момент операции очень важен, мы назвали его «контроль трепанирования», поскольку он позволяет убедиться, что трепан прошел в костномозговую полость центрального фрагмента. В противном случае ложное попадание делает дальнейший ход операции бессмысленным. В дальнейшем методика операции имеет два варианта: с использованием ручного сопоставления или аппаратной репозиции. При ручной репозиции, которая показана в большинстве случаев свежих ДПКГ, ассистент осуществляет растяжение фрагментов по длине (конечность по-прежнему согнута в коленном суставе), прижимая одной рукой стопу к столу и осуществляя противотягу локтевым сгибом другой руки. Может потребоваться значительное усилие, поэтому ассистент должен быть физически сильным, либо нужно иметь двух ассистентов. Оператор вручную устраняет боковое смещение, одновременно низводя по костномозговой полости проводник (рис.30). Попадание проводника в полость дистального фрагмента сопровождается ощущением хруста кости. Обязательно дополнительное прикладывание снаружи проводника-двойника. Срабатывание электроиндикатора подтверждает успех данного этапа ЗИОС (рис.28 и 35). Однако следует все же исключить контакт «спица-про вод ни к» в мягких тканях. Для этого выше «сработавшей» контактной спицы и параллельно ей, отступив 3-5 мм, вручную вводится контрольная спица или инъекционная игла до упора в кость. Отсутствие сигнала электроиндикатора делает несомненным факт правильного расположения проводника. По
проводнику забивается штифт, состоявшийся остеосинтез определяется исчезновением подвижности в зоне перелома (рис.36). При забивании штифта ассистент должен поддерживать небольшое вытяжение по длине и после прохождения штифтом зоны перелома (контроль штифтом-двойником путем прикладывания снаружи). После этого проводник необходимо удалить, чтобы провести электроиндикацию штифта (рис.37). Низведение штифта при этом следует осуществлять короткими ударами молотка при подключенных контактах индикатора, постоянно ориентируясь по длине штифта-двойника, прикладываемого к конечности снаружи. После срабатывания сигнала индикатора забивание штифта в случае необходимости блокирования следует продолжить (определяя заклинивание электроиндикацией) до конца. Если необходимости в блокировании нет (при переломах в средней трети), то спицы следует удалить и после этого завершить низведение штифта. Затем при помощи электроиндикатора (ЭИ) диагностируется наличие возможного диастаза (рис.31), который ликвидируют поколачиванием по пятке при выпрямленной ноге. При этом имеются некоторые технические особенности: - необходимо попросить кого-либо из медицинских работников, находящихся в операционной (чаще всего анестезиолога) осуществить противоупор в горизонтальном положении на надплечья пациента; - следует полностью выпрямить оперированную конечность и дать встречное напряжение («нреднапряжение»), ухватив кистью левой руки подошву стопы выше пятки; - двумя-тремя короткими сильными ударами ладонью правой руки по пятке на фоне предна л ряжения следует компрессировать фрагменты. Ликвидация диастаза подтверждается отсутствием срабатывания сигнала ЭИ. Блокированные спицы скусывают при максимальном отжатии мягких тканей. В завершение операции накладываются два-три шва на кожу в месте доступа с дренированием резиновой полоской (рис.38). Удаление штифта производится в среднем через год после операции. При этом для поиска конца штифта удобно воспользоваться электро индикацией (рис. 32).
Рис. 29. Схема вариантов доступа к костномозговой полости в зависимости от направления линии излома кости; пунктиром обозначено направление введения проводника: а - при типичном смешении, б- при атипичном смешении, в - оскольчатом переломе
Рис. 32. Схема индикации конца штифта при удалении конструкции после срастания перелома
Рис 33. Засверливание контактных и (или) блокирующих спиц в периферический фрагмент
Основные этапы методики ЗИОС; 1. Засверливание контактных спиц в дистальный фрагмент (рис.33). Перфорация дистального фрагмента для профилактики жировой эмболии. 2. Трепанирование костномозговой полости через «площадку» большеберцовой кости no Alms конечность согнута в коленном суставе и выдвинута вперед как при определении "симптома переднего выдвижного ящика" (рис.34). 3. Ощупывание стенок центрального фрагмента изнутри 4. Ручная репозиция (при максимально согнутой в коленном суставе голени) (рис. 30). 5. Введение проводника. 6. ЭИ проводника (рис.35). 7. Забивание по проводнику штифта (ниже линии перелома, но выше расположения контактной спицы) (рис.36). 8. Удаление проводника. 9. Дальнейшее забивание штифта до соприкосновения с 10. Окончательное забивание и блокирование штифта (в 11. ЭИ возможного диастаза (рис.31). 12. Ликвидация диастаза. 13. Контроль с помощью ЭИ успешной ликвидации 14. Скусывание блокирующих спиц (они же контактные) и 15. Наложение швов на место доступа, дренирование,
|
||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-18; просмотров: 159; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.131.178 (0.082 с.) |