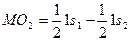Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Метод молекулярных орбиталей (МО)
Молекулярная орбиталь (MO1), включающая сумму 1sволновых функций одного и второго атомов водорода называется связывающей МО, а молекулярная орбиталь (MO2), включающая разность волновых функций атомов, называется разрыхляющей МО. Уровень энергии связывающей МО всегда ниже уровней энергии атомных орбиталей (АО), на основе которых формируется МО, а уровень энергии разрыхляющей МО выше энергетического уровня атомных орбиталей. Так же как и АО молекулярные орбитали (МО) на схемах иногда изображают клетками. МО заселяют электронами в соответствии с принципом минимума энергии, принципом Паули и правилом Хунда. Так, два электрона молекулы водорода следует поместить на связывающую МО. Спины электронов при этом антипараллельны (Рис.5.6.).
По симметрии различают σ- и π-орбитали. Например, σ- и π-орбитали, образованные из s, р d AO представлены на рисунке 5.7.
σ π π Рис.5.7. Образование сигма (σ) и пи-орбиталей (π) из различных АО
Основные положения метода молекулярных орбиталей: 1. Вся молекула рассматривается как единое целое, состоящее из ядер и электронов бывших атомов. 2. Всe электроны являются общими для всех ядер, т.е. химические связи являются многоцентровыми и простираются между ядрами всей молекулы. 3. Для решения уравнения Шредингера, как и в случае расчета атомных систем, вводится понятие одноэлектронного приближения, которое предполагает, что можно рассматривать каждый электрон движущимся в поле ядер и усредненном поле остальных электронов молекулы. В молекуле образуется собственная система молекулярных орбиталей, на которых находятся все электроны данной молекулы. 4. Распределение электронов по орбиталям подчиняется тем же принципам что и по АО: принцип минимума энергии, принцип Паули, правило Хунда. Логично предположить, что движение электрона вблизи некоторого ядра будет приблизительно таким как и в атоме в отсутствие других атомов. Поэтому вблизи этого ядра МО должна быть похожа на АО. Поэтому МО можно представить в виде линейной комбинации (cуммы) АО, т.е. ЛКАО: Ψi = Ci1Φ1 + Ci2Φ2 …CijΦj, где Ψi – волновая функция соответствущая i-той молекулярной орбитали, Φj – волновые функции соответствующие атомным орбиталям включенным в молекулярную, Cij – численные коэффициенты, которые находятся решением уравнения Шредингера и выражают долю (0 < |Cij|> 1) данной атомной (j) волновой функции в данной молекулярной (i). По физическому смыслу квадраты данных коэффициентов определяют вероятность нахождения электрона на данной МО (i) в области пространства данного атома (j). Общее количество таким образом построенных МО равно общему количеству базисных АО, из которых они сформированы. Кроме связывающих и разрыхляющих выделяют несвязывающие МО, которые локализованы на одном из атомов, не участвуют в образовании связи и соответствуют в первом приближении АО. Так, в молекуле НF из орбитали атома водорода и орбитали атома фтора образуются одна связывающая (σсв) и одна разрыхляющая (σраз.) орбитали молекулы, причем, связыающая орбиталь ближе по энергии к уровню 2рх АО фтора, а разрыхляющая – к уровню энергии 1s АО водорода. 2py и 2pz орбитали фтора трансформируются в несвязывающие молекулярные орбитали HF и, по существу, локализованы на атоме фтора. С 1s орбиталью они не взаимодействуют из-за разной симметрии волновых функций. Хотя волновые функции1s орбитали водорода и 2s фтора одинаковы по симметрии (интеграл перекрывания функций отличен от нуля), взаимодействие этих орбиталей практически отсутствует, потому что велика разность уровней энергии этих орбиталей. 2s орбиталь формально трансформируется в несвязывающую орбиталь. На несвязывающих орбиталях обычно находятся неподеленные пары электронов (Рис.5.8.).
Рис.5.8. Энергетическая диаграмма атомных и молекулярных уровней фтороводорода НF
Из двух 1s АО атомов водорода 2s и 2рх АО атома бериллия получают две сигма-связывающие (σсв), на которые помещают четыре валентных электрона атомов водорода и бериллия, и две сигма-разрыхляющие (σраз.) МО (Рис.5.9.).
Рис. 5.9. Энергетическая диаграмма исходных атомных (Ве, Н) и молекулярных уровней гидрида бериллия ВеН2.
Диаграмма уровней энергии МО метана (СН4) включает по три (σсв) и (σраз.), вырожденных МО (Рис.5.10.).
Рис. 5.10. Энергетическая диаграмма исходных атомных (С, Н) и молекулярных уровней метана СН4.
|
||||||
|
Последнее изменение этой страницы: 2016-12-30; просмотров: 1058; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.202.45 (0.006 с.) |
 и
и