
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Радиология - комплексная наука об ионизирующих излучениях.Стр 1 из 24Следующая ⇒
Введение
Сельскохозяйственная радиобиология относится к вариативной части математического и естественно – научного цикла ООП ВПО. Основу сельскохозяйственной радиобиологии составляют закономерности и механизмы действия ионизирующего излучения на биоорганические вещества, вирусы, бактерии, клетки ткани, целостные организмы, популяции, биогеоценозы, их сообщества и биосферу в целом. Знания по сельскохозяйственной радиобиологии являются базовыми для изучения дисциплин: кормопроизводство кормление животных; безопасности жизнедеятельности при ЧС; акушерство и гинекология; биотехнология. Сельскохозяйственная радиобиология является наукой направленной на формирование у студентов профессиональной компетенции: владеть способностью осуществлять сбор, анализ и интерпретацию материалов в области животноводства.
Лекция 1. КРАТКАЯ ИСТОРИЯ РАЗВИТИЯ РАДИОБИОЛОГИИ, ЦЕЛЬ, ЗАДАЧИ, СТРУКТУРА КУРСА. ОСНОВНЫЕ ПОНЯТИЯ, ОПРЕДЕЛЕНИЯ, ТЕРМИНЫ. 1.1. Цели изучения дисциплины Научить студента выполнять радиационную экспертизу объектов ветеринарного надзора и использовать на практике методы клинического и лабораторного исследования при лучевых поражениях. Ø Получить знания о роли, значении и месте эксплуатации основных типов радиометрических и дозиметрических приборов. Ø Овладеть методами рациональной экспертизы объектов ветеринарного надзора. Ø Овладеть методами клинического и лабораторного исследования при лучевых поражениях животных. Вопросы для самоконтроля 1. Дать определение, что такое радиобиология, ее связь с другими дисциплинами. 2. Цель и задачи, структура курса. 3. Вклад отечественных ученых в развитие науки. 4. Основоположники развития ридиологии и радиобиологии. 5. Задачи зооветеринарных специалистов в случаях загрязнении окружающей среды радионуклидами. Список литературы Основная 1. Гребенюк, А. Н., Основы радиобиологии и радиационной медицины: учебник/ А.Н. Гребенюк О. Ю. Стрелова, В. И. Легеза. – Спб.: Фолиант, 2012 - ISBN 5-93929-223-2 2. Лысенко, Н. П. Радиобиология: учебник/ Н.П. Лысенко, В.В. Пак, Л.В. Рогожина. – СПб.: Лань, 2012 – ISBN 978-5-8114-1330-0
Дополнительная 1. Сахаров, В. К. Радиоэкология./ Сахаров, В. К.- СПб: Лань.- 2006.- 320 с.
2. Анненков, Б.Н. Основы сельскохозяйственной радиологии: учебник / Б.Н. Анненков, E.B. Юдинцева. - M.: Агропромиздат, 1991. – 287с
Лекция 2. ЭЛЕМЕНТЫ ЯДЕРНОЙ ФИЗИКИ. СТРОЕНИЕ АТОМА. ИЗОТОПЫ, ИЗОБАРЫ, ИЗОМЕРЫ. ЯВЛЕНИЕ РАДИОАКТИВНОСТИ И ЕДИНИЦЫ ЕЕ ИЗМЕРЕНИЯ. ЗАКОН РАДИОАКТИВНОГО РАСПАДА. Строение атома
Окружающий нас мир построен из бесчисленного множества атомов различных элементов. Размеры атомов чрезвычайно малы. Достаточно сказать, что диаметр самого легкого атома водорода составляет всего лишь одну стомиллионную часть сантиметра (10−9см). Атом (гр. Слово atomos - неделимый) представляет собой элементарную частицу, которая сохраняет все физические и химические свойства данного элемента. До конца 19 века считалось, что атом неделим. Однако как показали исследования в области атомной физики, атом — это сложная система, состоящая из более мелких элементарных частиц. Итак, Мельчайшую частицу химического элемента, которая является носителем его химических свойств, называется атомом. В природе только инертные газы обнаруживаются в виде атомов, т. к. их внешние оболочки замкнутые, все остальные вещества существуют в виде молекул. Атом любого элемента можно разделить на субатомные (элементарные) частицы, и в этом случае он утратит свойства, характерные для данного элемента. К элементарным частицам относят электроны, протоны, нейтроны, мезоны, нейтрино и ряд других. Определение «элементарные»- не означает, что эти частицы простейшие бесструктурные элементы материи. Например, электрон, так же многообразен, как и атом. Атомы всех элементов, входящих в периодическую систему, состоят из электронов, протонов, и нейтронов. Один элемент отличается от другого только числом и расположением этих частиц. В начале XX в. было выдвинуто несколько теорий строения атома, которые называли моделями атома. В 1911 г. Э. Резерфорд предложил планетарную модель атома, которая более глубже была развита Н. Бором (1913). Согласно этой модели, в центре атома расположено ядро, имеющее положительный электрический заряд. Вокруг ядра перемешаются по электрическим орбитам электроны, образующие элиптическую оболочку атома.
Электронная оболочка — оболочка атома образованная электронами. Электрон представляет, собой элементарную частицу с поперечным сечением порядка 10−18 см. Его масса равна 9.1*10−28 гг, или 0,000548 ат.ед. массы, е энергетический эквивалент электрона составляет 0,000543*931 = 0,511 МэВ. (энергию частиц выражают в электровольтах - эВ). эВ - энергия, которую приобретает электрон проходящий в электрическое поле с разностью потенциалов в 1В. Электрон несет один элементарный отрицательный заряд электричества 1.602* 10−19 кулона и поэтому его обозначают символом е. Число электронов в нейтральном атоме каждого элемента равно его порядковому номеру в таблице Д.И. Мендилеева. Каждый электрон вращается в определенной зоне вокруг ядра. Если электронов 3 и больше, то вращаются на орбитах разных радиусов или, как говорят, на разных уровнях. Орбиты группируются в определенные электронные слои, окружающие ядро, они создают его оболочку. Таких слоев максимально может быть семь. Их обозначают буквами латинского алфавита: К,L,M,N,O,P,Q, причем ближайший к ядру является слой - К. Соответственно числу электронных слоев в периодической системе все элементы размещаются в семи периодах. Сумма отрицательных зарядов электронов оболочки уравновешивается равновеликим, но положительным зарядом ядра. Поэтому в невозбужденном состоянии атом в целом электрически нейтрален. Чем ближе к ядру вращается электрон, тем меньше уровень энергии вращения (кинетическая энергия), но тем больше его энергия связи с ядром (потенциальная энергия). Например, энергия К - электрона Sr90 (стронций) равно 16,15 кэВ (килоэлектрон вольт), а альфа- электрон только 1.95 кэВ.Энергия связи электрона на внешней орбите часто не превышает 1-2 эВ. И отсюда его сорвать легче. Здесь он легче вступает во взаимодействие с окружающей средой, чем электроны других орбит обуславливают электрические, химические, оптические и др. свойства атома. Поскольку в каждом слое электроны имеют свой уровень энергии, то перескок отдельного электроне с орбиты на орбиту всегда связан с поглощением или освобождением энергии. Но так как орбиты имеют строго определенные диаметры, то изменения энергии электрона совершаются ступенчато, определенными порциями. Строение атома. Атом, обладающий избытком энергии называется ВОЗБУЖДЕННЫМ, а переход электронов с одного энергетического уровня на другой, более удаленным, от ядра - процессом ВОЗБУЖДЕНИЯ. Поскольку в природе всякая система стремится перейти в положение, при котором ее энергия будет наименьшей то и атом из возбужденного состояния переходит первоначальное. Возращение атома в обычное состояние сопровождается делением избыточной энергии. Переход электронов из внешних орбит на внутренние сопровождается рентгеновым излучением с длиной волны, характерной для каждого энергетического уровня данного атома (характеристическое рентгеновское излучение). Переходы электронов в пределах внешних орбит дают оптический спектр, который состоит из ультрафиолетовых, световых и инфракрасных лучей. При сильных электрических воздействиях электроны вырываются из атома и удаляются за его пределы. Атом, лишившийся одного или нескольких электронов, превращается в положительный ион, а присоединивший к себе один или несколько электронов - в отрицательный.
Следовательно, на каждый положительный ион образуется один отрицательный ион, т. е. возникает пара ионов. Процесс образования ионов из нейтральных атомов называется ионизацией. Атом в состоянии иона существует в обычных условиях чрезвычайно короткий промежуток времени. Свободное место на орбите положительного иона заполняется свободным электроном, и атом вновь становится электрически нейтральной системой. Этот процесс носит название рекомбинации ионов (деионизация) и сопровождается выделением избыточной энергии в виде излучения. Энергия, выделяющаяся при рекомбинации ионов, количественно примерно равно затраченной на ионизацию. Таким образом, с положением электронов в электронной оболочке связано ряд свойств атома: возбуждение, ионизация и излучение энергии. Процесс ионизации атомов имеет важное практическое значение для обнаружения и дозиметрии излучений, а также для понимания биологического действия ионизирующей радиации. Строение ядра. Ядро атома имеет главное, определяющее значение для атома и в частности, обуславливает строение его электронных оболочек. Вещество ядра чрезвычайно плотно упаковано. Ядро обладает зарядом положительного электричества и состоит из протонов и нейтронов. Обе эти частицы рассматриваются как разные состояния одной и той же тяжелой частицы, называемой нуклоном (гр. нуклеус - ядро). Протон и нейтрон имеют массу, близкую к единице (1 а.е.м.) причем протон имеет единичный элементарный положительный электрический заряд, а нейтрон электрического заряда не имеет. Число протонов в ядре равно порядковому номеру элемента в периодической системе, иначе называемому атомным номером или зарядовым числом - Z (зета). Число нуклонов, т.е. протонов и нейтронов вместе, соответствуют атомному весу элемента, округленному до целых единиц. Это число называется массовым числом и обозначают буквами М или А. Очевидно, число нейтронов в ядре равно разности между массовым числом и атомным номером элемента N= М (А) - Z Диаметр ядра атома равен примерно 10-13...10-12 см и составляет 0,0001 диаметра всего атома. Однако практически вся масса атома (99,95 - 99,98%) сосредоточено в ядре, рассчитано, что если бы удалось получить 1 см3 чистого ядерного вещества, то оно весило бы 100 - 200 млн. т. Масса электронной оболочки незначительна, поэтому масса ядра почти совпадает с массой атома.
При обозначении атомов обычно пользуются символом элемента, которому принадлежит атом, и указывают сверху массовое число, а внизу — порядковый номер(Z) в форме индекса Порядковый номер иногда опускают, так как символ элемента вполне определяет его место в периодической системе. Энергия связи частиц в атоме. Внутри ядра между одноименно заряженными протонами существуют силы взаимного отталкивания (кулоновское отталкивание). Но наряду с ними тут действуют гораздо более мощные ядерные силы взаимопритяжения, удерживающие протоны и нейтроны в ядре. Считают, что наиболее вероятно ядерные силы возникают в процессе непрерывного обмена между нуклонами и особыми частицами (квантами ядерного поля), которые называют ПИ - мезонами или пионами. Ядерные силы - короткодействующие. Они значительны только на очень малых расстояниях, сравнимых с поперечником самих ядерных частиц (10-13 см). С увеличением расстояния между ядерными частицами ядерные силы очень быстро уменьшаются и становятся практически равными 0. Ядерные силы обладают свойством насыщения, т.е. каждый нуклон взаимодействует только с ограниченным числом соседних нуклонов. Поэтому при увеличении числа нуклонов в ядре ядерные силы значительно ослабевают. Этим объясняется меньшая устойчивость ядер тяжелых элементов, в которых содержится значительное количество протонов и нейтронов. Чтобы разделить ядро на составляющие его протоны а нейтроны и удалить их из поля действия ядерных сил надо совершить работу, т.е. затратить энергию. Эта энергия называется энергией связи ядра. При образовании ядра из нуклонов выделяется энергия связи. Если, например, рассчитать массу ядра атома гелия по формуле: m m Фактически, масса ядра гелия = 4,003 а.е.м. Т.к. масса ядра гелия оказывается меньше массы своих составных частей, взятых в отдельности, на величину 0,03 а.е.м. В этом случае говорят, что ядро имеет дефект массы(недостаток массы). Разница между массой ядра расчетной и массой ядра фактической называется дефектом массы ( Дефект массы показывает, насколько прочно связаны частицы в ядре, а так же сколько выделилось энергии при образовании ядра из отдельных нуклонов. Этот расчет можно произвести на основании уравнения взаимосвязи между массой и энергией, разработанного А. Эйнштейном: Е = Е- энергия в эргах; m - масса в г; с - скорость света, равная 3*10 В соответствии с этим законом масса и энергия представляет собой разные формы одного и того же явления. Ни масса, ни энергия не исчезают, а при соответствующих условиях переходят из одного вида в другой, т.е. любому изменению массы
Использовав это уравнение, подсчитаем энергию, которая выделится при образовании ядра гелия из отдельных нуклонов:
За единицу энергии принят электронвольт, поэтому энергию связи ядра можно выразить в электрон-вольтах исходя из того, что энергетический эквивалент 1 а.е.м. составляет 931 МэВ
Если бы существовал способ разделения ядра атома гелия на 2 протона и 2 нейтрона, то для этого потребовалось бы затратить не меньше 28 М эВ энергии. Средняя энергия связи, приходящиеся на один нуклон, называется удельной энергиейсвязи (сила атома). Для гелия оно составляет 28:4 = 7 МэВ. Следовательно, зная дефект массы, можно легко вычислить энергию связи ядра. Энергия связи ядер соразмерно возрастает с увеличением числа нуклонов, однако нестрого пропорционально их числу. Например, энергия ядре дейтерия составляет 2,2 МэВ, азота - 104,56, а урана - 1800 МэВ. Если не считать самых легких ядер (дейтерий, тритий), это энергия связи на 1 нуклон составляет для всех ядер примерно 8 МэВ. Для сравнения необходимо напомнить что химическая энергия связи атомов в молекулах в расчете на 1 атом равно нескольким электровольтам (2 - 5 эВ). Именно этим объясняется, что ядерные реакции характеризуются в миллион раз большими энергиями, чем обычные химические реакции. Таким образом закон взаимосвязи массы и энергии показывает, откуда возникает та колоссальная энергия, которая выделяется при синтезе и делении ядер.
Единицы радиоактивности. Радионуклиды трудно получить в абсолютно чистом виде. Обычно они находятся в смеси с нерадиоактивмыми веществами и, как правило в количестве, зачастую не поддающимся всеобщему определению. Поэтому мерой количества радионуклида служит не вес, выраженный в граммах, а активность. Активностью радиоактивного препарата называется количество атомов, распадающихся в нем за секунду. Следовательно, активность определяется числом распадов в единицу времени. Активность радионуклида характеризует абсолютную скорость его радиоактивного распада. Как следует из закона радиоактивного распада, активность радионуклида пропорциональна числу радиоактивных атомов, т.е. возрастает с увеличением количества данного вещества. Поскольку скорость распада разных радионуклидов различна, то одинаковые весовые количества различных радионуклидов имеют разную активность. Так если взять с одинаковой массой радионуклиды Единицей активности в абсолютной системе единиц (СИ) служит распад в секунду (расп/с). Этой единице присвоено наименование беккерель (БК); 1Бк =1с Наиболее употребительная является внесистемная международная единица кюри (Ки). Кюри - это такое количество любого радиоактивного вещества, в котором число радиоактивных распадов в секунду равно 3,7*10 Милликюри (мКи) = 10 Микрокюри (мкКи)= 10 Нанокюри (нКи) = 10 Пикокюри (пКи)= 10 На практике часто пользуются числом распадов в секунду, тогда единица радиоактивности кюри и дробные от нее принимают следующие значения: 1 Ки = 2,22*10 1 мКи =2,22*10 1 мкКи=2,22*10 1 иКи =2,22*10 1 пКи =2,22расп/мин. В 1946 г Е. Кондон и Л. Куртис предложили новую единицу активности резерфорд (рд =10 Радиоактивные вещества характеризуются величиной удельной активности или концентрации, т.е. активностью, приходящейся на единицу массы (объема). Единицами удельной активности являются: Ки/мл, К и/л, Ки/г, К и/кг и их производные. Убыль активности любого радиоактивного препарата определяется по формуле, соотв. Основному закону радиоактивного распада: Аt = Aо*e*(0.693*t/T). At - активность препарата через t времени; А – исходная активность препарата; Т – период полураспада значения Т и t должны иметь одинаковую размерность (минуты, часы, дни и т.д.) Пример: Активность (Ао) At = 5*2,72*(0,693*7/14,3) = 5*2,72-0,24= 3,55 мКи. Миллиграмм - эквивалент радия - это активность. любого радиоактивного препарата, гамма-излучение которого при идентичных условиях измерения создают такую же мощность экспозиционной дозы, как гамма – излучение. Единица (мг-экв. радия) не установлены, существующими стандартами, но широко используются на практике.
Вопросы для самоконтроля
1. Диалектическое представление о строении атома. 2. Какой атом называется возбужденным и что такое процесс возбуждения. 3. Что такое рекомбинация ионов. 4. Дать характеристику строению ядра. 5. Что такое энергия частиц в атоме. 6. Что такое изотопы, изобары, изомеры. 7. Что такое радиоактивность и единица ее измерения. 8. Перечислите типы ядерных превращений. 9. Закон радиоактивного распада и что он показывает.
СПИСОК ЛИТЕРАТУРЫ
Основная 1. Гребенюк, А. Н., Основы радиобиологии и радиационной медицины: учебник/ А.Н. Гребенюк О. Ю. Стрелова, В. И. Легеза. – Спб.: Фолиант, 2012 - ISBN 5-93929-223-2 2. Лысенко, Н. П. Радиобиология: учебник/ Н.П. Лысенко, В.В. Пак, Л.В. Рогожина. – СПб.: Лань, 2012 – ISBN 978-5-8114-1330-0 Дополнительная 1. Оробец, В.А. Радиоэкология: курс лекций/В.А. Оробец, О.А. Рыбальченко: СтГАУ.- Ставрополь: АГРУС, 2007. -204 с. 2. Ярмоленко, С.П. Радиобиология человека и животных: учебник для биологических спец. ВУЗов / С.П. Ярмоленко. – М.: Высшая школа, 1988. – 424 с. 3. Кузин, А.М. Прикладная радиобиология. / А.М. Кузин, Д.А. Каушанский.- М.: Энергоатомиздат, 1991 г., 221 с.
Лекция 3 ХАРАКТЕРИСТИКА АЛЬФА, БЕТА-ЧАСТИЦ И ΓАММА-ЛУЧЕЙ. ВЗАИМОДЕЙСТВИЕ ИЗЛУЧЕНИЙ С ВЕЩЕСТВОМ. 3.1. Характеристика α-, бета-частиц и γ-лучей. Радиоактивное излучение невидимо, но обнаруживается рядом объективных явлений. Наиболее характерными из них являются: фотохимические действие, возбуждение, люминесценции и ионизации вещества, в котором излучение поглощается. Было обнаружено, что радиоактивное излучение в поперечном магнитном поле разделяется обычно на три пучка. Один из них в магнитном поле не отклоняется и, следовательно, не имеет электрического заряда, два других в магнитном поле отклоняются в противоположные стороны, следовательно, они состоят из электрически заряженных частиц различного знака. Лучи, отклоняющиеся к (-) заряженной пластинке, условно были названы альфа — лучами, отклоняющиеся к положительно заряженной пластинке - бета-лучами, а лучи, которые совсем не отклонялись были названы гамма-лучами (истинные). Альфа-излучение - поток положительно заряженных частиц (ядер атомов гелия), движущихся со скоростью 20000 км/с. Альфа - частицы имеют большую массу и обладают значительной энергией, но их проникающая способность не велика – их пробег в твердых и жидких средах составляет сотые доли мм. Они вызывают сильно выраженные эффекты, ионизации и флуоресценции. Потому вся энергия альфа - частиц (на 1 см пути альфа- частицы образуют 100-250 тыс. пар ионов) передаются клеткам организма - нанося вред. Вследствие малой проникающей способности альфа частицы могут быть полностью задержаны листом плотной бумаги, одеждой, слоем резины и хирургических перчаток, эпидермисом. Альфа- частицы - ядро, состоящее из 2-х протонов и 2-х нейтронов. Альфа - излучение - поток ядер атомов гелия (альфа-частиц). Бета-излучение - поток отрицательно заряженных частиц (электронов). В электрическом поле они отклоняются к положительному полюсу. Их скорость приближается к скорости, света. Бета- частицы имеют небольшую массу (они в 1840 раз легче протонов), но отличаются большой проникающей способностью — в воздухе они могут пробегать путь длинной, измеряемой десятками сантиметров и даже несколькими метрами (в мягких тканях максимальный пробег бета — частиц достигает нескольких сантиметров). Бета — частицы средних энергий задерживаются оконным стеклом, подошвой обувью и т.п., но бета — частицы с энергией 0,07 МэВ (электронвольт) уже могут пробить эпидермис. Поэтому даже при работе с мягкими (бета - излучателями руки должны быть защищены перчатками, а от жестких (бета - частиц с энергией 0,5 МэВ и выше) следует защищаться экраном. Гамма-излучение представляет собой коротковолновое электромагнитное излучение. Гамма - лучи не отклоняются ни в электрическом, ни в магнитном поле. По свойствам это излучение близко к рентгеновскому, но обладает значительно большей скоростью и энергией. Оно распространяется со скоростью света. Характерная особенность гамма-излучения - исключительно высокая проникающая способность. Пробег гамма - квантов в воздухе может достигать 100 м, в мягки тканях — десятки сантиметров. Гамма - излучение в поглотителе тем сильнее, чем меньше энергия квантов и больше масса, т.е. объем, плотность и порядковый номер поглотителя. По воздуху γ-кванты свободно пролетают 100 м. При этом слой полуослабления (1/2) для квантов с энергией 2,5 МэВ составляет в воздухе 200 м, в свинце только — 1,8 см, в бетоне-10 см, а в дереве - 25 см. Слой свинца толщиной 40 см ослабляет энергию таких γ -квантов в 107раз. С целью противорадиационной защиты должны проводиться мероприятия по предупреждению попадания и резобции радионуклеидов и ускорение их выведения из организма. С этой целью используется большое количество химических веществ, сорбирующих радионуклиды или переводящие их в прочные комплексы. Гамма-кванты — высвечиваемое излучение, испускаемое при радиоактивном распаде ядрами с избытком энергией, не захваченной альфа и бета - частицами. Вопросы для самоконтроля
1. Дайте характеристику α - частицы и возможная защита от них. 2. Дайте характеристику бета - частицы и возможная защита от них. 3. Дайте характеристику γ - лучей и возможная защита от них. 4. Что понимается под воздействием ядерных излучений с веществом. 5. Перечислите основные эффекты взаимодействия нейтронов с веществом.
СПИСОК ЛИТЕРАТУРЫ Основная 1. Гребенюк, А. Н., Основы радиобиологии и радиационной медицины: учебник/ А.Н. Гребенюк О. Ю. Стрелова, В. И. Легеза. – Спб.: Фолиант, 2012 - ISBN 5-93929-223-2 2. Лысенко, Н. П. Радиобиология: учебник/ Н.П. Лысенко, В.В. Пак, Л.В. Рогожина. – СПб.: Лань, 2012 – ISBN 978-5-8114-1330-0 Дополнительная 1. Сахаров, В. К. Радиоэкология./ Сахаров, В. К.- СПб: Лань.- 2006.- 320 с. Лекция 4. Фотографический метод. При воздействии излучений на фотографическую пленку или фотоэмульсию в результате ионизации происходят фотохимические процессы воздействия. По числу следов в фотоэмульсии можно судить об интенсивности потока излучения, а по длине следа определяютют энергию частицы. Доза гамма-излучения измеряется по суммарному почернению фотопленки. Фотографические пленки широко используются в дозиметрии для определения дозы гамма-излучения, полученной каждым работником. Люминесцентный (сцинтилляционный) метод: Некоторые вещества, например сернистый цинк, стиблен, антрацен и другие светятся (люминесцируют) под влиянием излучения. Слабые световые вспышки, которые преобразуются с помощью фотоумножителя, могут быть затем зарегистрированы измерительным прибором. Прибор состоящий из люминесцентного кристалла и фотоумножителя, называется люминесцентным или сцинтиллационным счетчиком. Химический метод Под воздействием излучений химические вещества изменяют свои свойства: изменяется цвет растворов, выделяются газы из соединений, происходит осаждение коллоидов и т.п.. Степень этих изменений зависит от дозы излучения. Химические методы дозиметрии являются малочувствительными и используются в основном для измерения больших доз излучения. Классификация приборов для измерения излучений. Методы измерения. Приборы для измерения ионизирующих излучений можно условно разделить на 3 категории радиометрические (радиометры), дозиметрические (дозиметры), и устройства для ядерно-физических исследований. Радиоактивность препаратов можно определить абсолютным, расчетным и относительным (сравнительным) методами. Наиболее широкое применение в практике имеет последний. Относительный (сравнительный) метод определения радиоактивности основан на сравнении активности исследуемого препарата с активностью стандартного препарата (эталона) содержащее известное количество изотопа. Достоинства метода: простота, оперативность, достоверность. В качестве эталона используют естественный радиоизотоп 40К, 90Sr.
Вопросы для самоконтроля 1. Что понимается под радиометрией и дозиметрией? 2. Перечислите и дайте характеристику методам и средствам дозиметрии и радиометрии. 3. Что понимается под дозой излучения? 4. Назовите единицы измерения доз излучения. 5. Как рассчитать дозу при внешнем облучении? 6. Как рассчитать дозу при внутреннем облучении?
СПИСОК ЛИТЕРАТУРЫ Основная 1. Гребенюк, А. Н., Основы радиобиологии и радиационной медицины: учебник/ А.Н. Гребенюк О. Ю. Стрелова, В. И. Легеза. – Спб.: Фолиант, 2012 - ISBN 5-93929-223-2 2. Лысенко, Н. П. Радиобиология: учебник/ Н.П. Лысенко, В.В. Пак, Л.В. Рогожина. – СПб.: Лань, 2012 – ISBN 978-5-8114-1330-0 3. Фокин, А. Д. Сельскохозяйственная радиобиология: учебник/ А. А. Лурье, С. П. Торшин. - СПб: Лань, 2011- ISBN: 978–5–8114–1123–8 Дополнительная 1. Ярмоленко, С.П. Радиобиология человека и животных: учебник для биологических спец. ВУЗов / С.П. Ярмоленко. – М.: Высшая школа, 1988. – 424 с. 2. Дорожко, С.В. Защита населения и хозяйственных объектов в чрезвычайных ситуациях. Радиационная безопасность: учебное пособие. Часть 3. Радиационная безопасность / С.В. Дорожко, В.П. Бубнов, В.Т. Пустовит. – Мн.: УП «Технопринт», 2003. – 209 с. 3. Ильин, Л.А. Радиационная гигиена: учебник / Л.А. Ильин, В.Ф. Кириллов, И.П. Коренков. – М.: Медицина,1999. – 384 с.
Лекция 5
Вопросы для самоконтроля
1. Перечислите основные факторы, обуславливающие токсичность радионуклидов. 2. Дайте характеристику молодым продуктам деления. 3. Назовите группы радиотоксичности радионуклидов. 4. Метаболизм и токсикология йода 131 5. Токсикология стронция 90 6. Токсикология цезия 137
СПИСОК ЛИТЕРАТУРЫ Основная 3. Гребенюк, А. Н., Основы радиобиологии и радиационной медицины: учебник/ А.Н. Гребенюк О. Ю. Стрелова, В. И. Легеза. – Спб.: Фолиант, 2012 - ISBN 5-93929-223-2 4. Лысенко, Н. П. Радиобиология: учебник/ Н.П. Лысенко, В.В. Пак, Л.В. Рогожина. – СПб.: Лань, 2012 – ISBN 978-5-8114-1330-0 5. Фокин, А. Д. Сельскохозяйственная радиобиология: учебник/ А. А. Лурье, С. П. Торшин. - СПб: Лань, 2011- ISBN: 978–5–8114–1123–8 Дополнительная 4. Ярмоленко, С.П. Радиобиология человека и животных: учебник для биологических спец. ВУЗов / С.П. Ярмоленко. – М.: Высшая школа, 1988. – 424 с. 5. Постник, М.И. Защита населения и хозяйственных объектов в чрезвычайных ситуациях: учебник / М.И. Постник. – Минск: Вышейшая школа, 2003. – 398 с. 6. Анненков, Б.Н. Основы сельскохозяйственной радиологии: учебник / Б.Н. Анненков, E.B. Юдинцева. - M.: Агропромиздат, 1991. – 287с. 7. Кузин, А.М. Прикладная радиобиология. / А.М. Кузин, Д.А. Каушанский.- М.: Энергоатомиздат, 1991 г., 221 с. Лекция 6. Вопросы для самоконтроля
1. Назовите природные источники ионизирующего излучения. 2. Назовите искусственные источники излучения. 3. Что понимается под временно допустимыми уровнями (ВДУ) и допустимыми уровнями (ДУ)? 4. Назовите ВДУ суммарной активности цезия-134, 137, стронция -90 в продуктах питания и воде. 5. Что понимается под поверхностным загрязнением? 6. Что такое структурное загрязнение? 7. Назовите пути поступления радионуклидов в организм.
СПИСОК ЛИТЕРАТУРЫ Основная 1. Гребенюк, А. Н., Основы радиобиологии и радиационной медицины: учебник/ А.Н. Гребенюк О. Ю. Стрелова, В. И. Легеза. – Спб.: Фолиант, 2012 - ISBN 5-93929-223-2 2. Лысенко, Н. П. Радиобиология: учебник/ Н.П. Лысенко, В.В. Пак, Л.В. Рогожина. – СПб.: Лань, 2012 – ISBN 978-5-8114-1330-0 3. Фокин, А. Д. Сельскохозяйственная радиобиология: учебник/ А. А. Лурье, С. П. Торшин. - СПб: Лань, 2011- ISBN: 978–5–8114–1123–8 Дополнительная 1. Постник, М.И. Защита населения и хозяйственных объектов в чрезвычайных ситуациях: учебник / М.И. Постник. – Минск: Высшая школа, 2003. – 398 с.
Лекция 7
Исходные положения после выпадения радиоактивных осадков
1. Исходные положения после выпадения радиоактивных осадков. В условиях радиоактивного загрязнения сельскохозяйственное производство должно осуществиться при условии полной радиационной безопасности для работающих на этой территории людей. 2. Основной вклад в радиоактивные продукты ядерного деления вносят короткоживущие радионуклиды -изотопы йода. В первые дни, недели, вероятность серьезного радиационного поражения людей и животных наибольшая, что предопределяет необходимость осуществления жесткого контроля за соблюдением мер безопасности в этот период. 3. Радиоактивное загрязнение местности обычно носит неравномерный характер, это имеет важное значение с хозяйственной точки зрения (некоторый маневр - пастбища животных, сбор кормов). 4. В следующий сельскохозяйственный год - необходимо следить за содержанием радиологически допустимых радионуклидов стронция и цезия- (Чернобыле). В принципе любая сельскохозяйственная. продукция, полученная на загрязненной территории, может быть использована для тех, или иных хозяйственных целей: непосредственно (без предварительной переработки) для питания людей, и для переработки в пищевой промышленности (получение крахмала, спирта, масла и т.д.) 5. Вопрос о перепрофилировании хозяйства (в зоне радиационного загрязнения)- решается после всестороннего экономического обоснования.
6) Систему ведения сельского хозяйства на загрязненной территории следует разрабатывать по зональному типу: a) Учитывать плотность загрязнения 90Sr, Cs137 b) Почвенно- климатические условия c) Материально технические возможности хозяйства Конечная цель- получение нужной сельскохозяйственной продукции с допустимыми уровнями загрязнения радионуклидами
7) Сельскохозяйственное производство должно вестись так, чтобы исключить возможность увеличения загрязнения относительно «чистых» угодий радионуклидами, обеспечить максимальное снижение миграции радионуклидов во всех звеньях пищевой цепи (почва-растение- сельскохозяйственные животные - продукты животноводства). 8) Увеличение урожайности сельскохозяйственных культур и продуктивности животных позволяет при прочих равных условиях снизить концентрацию радионуклидов в сельскохозяйственных продукции.
Вопросы для самоконтроля
1. Назовите исходные положения после выпадения радиоактивных осадков. 2. Особенности ведения сельскохозяйственного производства в ближайший период после выпадения радиоактивных осадков. 3. Чем отличается характер работ в зимний период от весенне-летнего периода.
|
|||||||||
|
Последнее изменение этой страницы: 2017-01-20; просмотров: 374; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.132.223 (0.181 с.) |
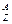 Х где Х - символ элемента, например, ядро углерода
Х где Х - символ элемента, например, ядро углерода 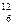 С содержит 12 нуклонов, из них 6 протонов, ядро натрия 23
С содержит 12 нуклонов, из них 6 протонов, ядро натрия 23 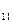 Na имеет 23 нуклона, из них 11 протонов.
Na имеет 23 нуклона, из них 11 протонов. = m
= m 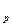 N
N 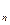 N
N  m)
m) 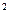 , где
, где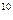 см/с.
см/с.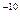 )
) 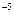 эрг.
эрг. U,
U,  Р и
Р и  Li, обладающие различными периодами полураспада (4,5*10
Li, обладающие различными периодами полураспада (4,5*10  лет), 14,3 дня, и 0,89 с соответственно., то самая высокая активность будет у лития и фосфора и очень малая у урана, т.к. наибольшее количество распадов в 1 с будет у первых двух изотопов.
лет), 14,3 дня, и 0,89 с соответственно., то самая высокая активность будет у лития и фосфора и очень малая у урана, т.к. наибольшее количество распадов в 1 с будет у первых двух изотопов.
 Ки = 3,7*10
Ки = 3,7*10  рас п/с;
рас п/с;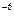 Ки =3,7*10
Ки =3,7*10  расп/c;
расп/c; Ки = 3,7*10-1 расп/с;
Ки = 3,7*10-1 расп/с; Ки = 0,037 расп/с.
Ки = 0,037 расп/с. расп/мин;
расп/мин; расп/мин
расп/мин расп/мин
расп/мин


