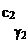Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Действие электролитов на коагуляцию
Установлен ряд эмпирических закономерностей воздействия электролитов, которые известны под названием правил коагуляции: 1. Любые электролиты могут вызвать коагуляцию, однако заметное воздействие они оказывают при достижении определенной концентрации. Порог коагуляции – минимальная концентрация электролита, вызывающая коагуляцию (g, моль/л; иногда Ск). Порог коагуляции определяют по помутнению, изменению окраски или по началу выделения дисперсной фазы в осадок. 2. Правило Шульце-Гарди (правило значности, эмпирическое): Коагулирующим действием обладает тот ион электролита, который имеет заряд, противоположный заряду потенциалопределяющих ионов мицеллы (гранулы), причем, коагулирующее действие тем сильнее, чем выше заряд.
где К – коагулирующая способность (примем ее за единицу). По правилу Шульца – Гарди значение порогов коагуляции для противоионов с зарядами 1, 2 и 3 соотносятся как 1:1/20:1/500, т.е. чем выше заряд, тем меньше требуется электролита, чтобы вызвать коагуляцию. Например, коагулируем золь сульфида мышьяка (As2S3): или Fe(OH)2
NaCl (Na+) g=5 моль/л KBr (Br-) g=12,5 MgCl2 (Mg2+) g=0,72 K2SO4 (SO42-) g=0,205 AlCl3 (Al3+) g=0,092
Правило Шульце – Гарди имеет приближенный характер и описывает действие ионов лишь неорганических соединений.
3. В ряду органических ионов коагулирующее действие возрастает с повышением адсорбционной способности. 4. В ряду неорганических ионов одинаковой зарядности их коагулирующая активность возрастает с уменьшением гидратации. Лиотропные ряды или ряды Гофмейстера – это порядок расположения ионов по их способности гидратироваться (связывать воду). Слово ''лиотропный'' значит ''стремящийся к жидкости'' (более подходящий термин для случая водных сред – гидротропный).
Li+; Na+; K+; Rb+; Cs+
Теплота гидратации: 140 117 93 86 (ккал/г-ион)
5. Очень часто началу коагуляции соответствует снижение дзета-потенциала до критического значения (около 0,03 В).
6. В осадках, получаемых при коагуляции электролитами, всегда присутствуют ионы, вызывающие ее.
Совместное действие электролитов При коагуляции Смеси электролитов при коагуляции золей редко действует независимо. Наблюдаемые при этом явления можно свести к трем следующим: аддитивность, антагонизм и синергизм электролитов. Указанные явления при использовании смесей электролитов приведены на рис.5.2.
Зависимость 1 – характеризует аддитивное действие электролитов. Коагулирующее действие в смеси определяют по правилу простого сложения: KCl+KNO3; NaCl+KCl Кривая 2 – антагонизм электролитов – содержание каждого электролита в смеси превышает его собственную пороговую концентрацию Al(NO3)3+K2SO4; Ti(NO3)4+Na2SO4 Синергизм действия электролитов демонстрирует кривая 3. Усиливается действие каждого из электролитов – для коагуляции их требуется меньше в смеси, чем каждого по отдельности. LiCl+CaCl2 действуют на гидрозоль H2S
Рис. 5.2. Совместное действие электролитов при коагуляции.
|
|||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 231; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.69.152 (0.004 с.) |

 (As2S3) Fe(OH)2
(As2S3) Fe(OH)2 возрастание коагулирующей активности
возрастание коагулирующей активности возрастание степени гидратации
возрастание степени гидратации