Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Электрокинетический потенциал.
Потенциал на поверхности - φ называется термодинамическим потенциалом и характеризует скачок потенциала на поверхности раздела между фазами. Потенциал на поверхности раздела φ и потенциал так называемой плоскости максимального приближения (расположенной на расстоянии Δ порядка молекулярных размеров) φ0 принадлежат к разряду практически неизмеримых величин. Для характеристики электрических свойств поверхности используют ζ-потенциал – потенциал границы скольжения фаз, определяемый экспериментально различными методами (метод потенциала протекания, электрофоретический метод и др.). ζ-потенциал можно представить как работу, необходимую для переноса единичного заряда из бесконечно удаленного элемента объема раствора на поверхность скольжения. ζ-потенциал по знаку совпадает с φ-потенциалом. Из рис. 4.1 видно, что потенциал границы скольжения ниже чем потенциал на поверхности, тем не менее величина ζ-потенциала широко используется для характеристики свойств поверхности при рассмотрении адсорбции, адгезии, агрегативной устойчивости дисперсных систем и других важных процессов.
Влияние электролитов на электрокинетический потенциал Как видно из рис. 4.1, значение электрокинетического потенциала зависит от числа нескомпенсированных на поверхности скольжения зарядов адсорбционного слоя, т.е. от числа ионов в диффузном слое. Толщина двойного электрического слоя и значение электрокинетического потенциала зависят от концентрации электролита в растворе. Изменение электрокинетического потенциала с изменением концентрации ионов разных валентностей показано на рис. 4.2.
Рис. 4.2. Зависимость электрокинетического потенциала от концентрации электролита для одно (1), двух (2) и трех (3) зарядных противоионов.
Изменение толщины ДЭС при добавлении электролита к раствору объясняется тем, что при этом в растворе изменяются соотношения между влиянием электростатического притяжения и диффузии, определяющими распределение ионов в наружной обкладке двойного слоя. Катионы оказывают тем более понижающее действие (при отрицательном знаке заряда поверхности), чем выше их валентность. Такое действие можно объяснить тем, что с увеличением заряда иона возрастает сила электростатического притяжения его к поверхности и ионы большей валентности могут ближе подойти к поверхности, вызывая тем самым более сильное сжатие диффузного слоя и, соответственно, понижение ζ-потенциала.
Многовалентные ионы могут не только уменьшить величину электрокинетического потенциала, но и изменить его знак, т.е. произвести перезарядку поверхности. Это объясняется их высокой специфической адсорбционной способностью: сильно электростатически притягиваясь к поверхности, многовалентные катионы нейтрализуют ее заряд, дальнейшая сверхэквивалентная адсорбция катионов поверхностью приводит к появлению избыточного положительного заряда на поверхности раздела, который вновь будет компенсироваться отрицательными противоионами, вследствии чего на поверхности возникнет новый двойной электрический слой с положительной внутренней обкладкой и отрицательным слоем противоионов. Четырехвалентные металлы, например цирконий, обеспечивают уже в незначительном количестве резкое снижение электрокинетического потенциала, минимальное увеличение концентрации металла приводит к перезарядке поверхности и увеличению значений ζ-потенциала.
Строение мицеллы. Согласно общепринятой мицеллярной теории строения коллоидных растворов, золь состоит из 2-х частей: 1. Мицелла – структурная коллоидная единица (частица дисперсной фазы), окруженная двойным электрическим слоем. 2. Интермицеллярная жидкость – дисперсионная среда, разделяющая мицеллы, в которой растворены электролиты, неэлектролиты и ПАВ.
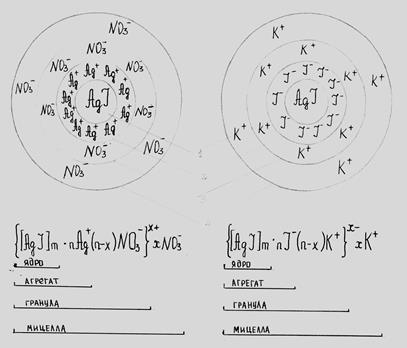
Строение мицеллы может быть рассмотрено лишь в первом приближении, т.к. она не имеет определенного состава. В настоящее время нет возможности учесть влияния на строение мицеллы всех процессов, обусловленных сложными ионно-молекулярным взаимодействием на поверхности раздела двух фаз в растворе. Рассмотрим, без учета влияния интермицеллярной жидкости, упрощенные схемы мицеллы иодида серебра, полученные по реакции:
Элементарная коллоидная частица – мицелла (4) – имеет следующее строение:
- в центре находится ядро (1), представляющее собой микрокристалл или агрегат из микрокристаллов; поверхность ядра обладает запасом свободной энергии и избирательно адсорбирует ионы из окружающей среды. Правило Панета-Фаянса: на поверхности твердого тела предпочтительно адсорбируются ионы, способные достраивать его кристаллическую решетку или образующие с ионами, входящими в состав кристаллической решетки наиболее труднорастворимые соединения. Определяется это избытком тех или иных ионов. - ядро вместе с потенциалопределяющими ионами образуют агрегат (2); - после возникновения заряда агрегат начинает притягивать из раствора ионы с противоположным знаком (противоионы) – образуется двойной электрический слой; - при этом, некоторые ионы очень прочно притягиваются к агрегату, образуя адсорбционный (плотный) слой противоионов. Агрегат вместе с противоионами плотного слоя составляет гранулу или частицу (3). Частица характеризуется двойным электрическим слоем, состоящим из потенциалопределяющих ионов и противоионов плотного слоя, алгебраическая сумма которых определяет заряд системы; - противоионы не входящие в плотный слой и находящиеся на более далеком расстоянии от ядра образуют диффузный слой противоионов. Все вместе составляет мицеллу (4), электрический заряд которой равен нулю.
|
||||||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 505; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.69.152 (0.007 с.) |