
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Поглощение (адсорбция) света.
В 1760 г. Ламберт установил зависимость между интенсивностью прошедшего света и толщиной среды, через которую он прошел:
Поглощение во всех слоях, на которые мысленно может быть разделена данная среда проходит одинаково: каждый последующий слой поглощает ту же долю света, что и предыдущий. Беер показал, что
Закон Ламберта-Беера:
Логарифмируя уравнение Ламберта-Беера получаем:
Это выражение называют экстинкцией (Е), поглощением или оптической плотностью раствора.
Выражение Принимая Закон Ламберта-Беера справедлив для гомогенных систем.
Лекция 4. Электрокинетические свойства дисперсных систем. Теории образования и строения двойного электрического слоя (ДЭС) Электрокинетический потенциал Влияние электролитов на электрокинетический потенциал Строение мицеллы Электрокинетические явления Практическое использование электрокинетических явлений Теории образования и строения ДЭС. Существование двойного электрического слоя (ДЭС) ионов и скачка потенциала на границе раздела двух фаз играет важную, а иногда – основную роль во многих явлениях важных для теории и практики. К ним относятся: электродные процессы, электрокапиллярные и электрокинетические явления, явления связанные с электростатическим взаимодействием коллоидных частиц, в значительной степени определяющие устойчивость дисперсной системы. Все эти явления, взаимосвязанные посредством ДЭС, называются электроповерхностными.
Рассмотрим явление, имеющее место на границе раздела фаз – возникновение двойного электрического слоя, обусловливающего различные электроповерхностные явления. Различают три возможных механизма образования ДЭС: - в результате перехода ионов или электронов из одной фазы в другую (поверхностная ионизация); - в результате избирательной адсорбции в межфазном слое ионов электролитов; - в результате ориентирования полярных молекул сопряженных фаз при их взаимодействии.
По первому механизму, заряд на поверхности может образовываться в результате электролитической диссоциации молекул поверхности твердой фазы, в результате чего ионы одного знака остаются в фиксированном положении на этой поверхности, а противоионы (ионы противоположного знака) поступают в прилегающий раствор. По такому механизму ДЭС возникает в растворе целого ряда высокомолекулярных соединений. По второму механизму, ионы одного знака необменно адсорбируются поверхностью, а ионы противоположного знака, в силу электростатического притяжения, располагаются около нее. Величина и знак заряда поверхности зависит от природы твердых частиц адсорбента и от природы жидкости, с которой он соприкасается. Рассмотрим схемы строения ДЭС согласно различным теориям. Впервые представление о ДЭС было высказано Квинке (1859) и развито в работах Гельмгольца (1879). Теория ДЭС получила развитие в трудах ученых СССР А.Н. Фрумкина и Б.В. Дерягина. Первой теорией строения ДЭС была теория Гельмгольца: ДЭС состоит из двух плоских зарядов, расположенных на молекулярном расстоянии один от другого и взаимодействующих между собой только за счет электростатических сил притяжения. Структура подобна плоскому конденсатору, падение потенциала между слоями происходит линейно. Модель Гуи-Чепмена предполагала диффузионное расположение противоионов, находящихся под воздействием сил, действующих в противоположных направлениях: электростатических сил притяжения к поверхности и сил теплового движения ионов, приводящих к диффузии и размыванию внешнего слоя. Теория вводит понятие диффузионного слоя, ионы рассматриваются как точечные заряды, не имеющие собственных размеров.
По современным представлениям (теория Штерна) строение ДЭС представляется следующим образом: ионы входящие в состав твердой фазы, образуют внутреннюю обкладку двойного слоя; ионы противоположного знака, т.е. противоионы образуют внешнюю обкладку, при этом часть противоионов находится в непосредственном соприкосновении с ионами твердой фазы, образуя плотный слой (слой Гельмгольца, адсорбционный слой), другая часть противоионов составляет диффузный слой (слой Гуи). Система в целом всегда является электронейтральной, то есть число зарядов внутренней обкладки должно быть равно числу зарядов противоионов (плотный слой + избыток в диффузном слое). В пределах ДЭС действует электрическое поле, интенсивность которого характеризуется значением потенциала. Изменение потенциала в ДЭС в зависимости от расстояния показано на рис. 4.1. При этом падение потенциала в пределах плотного слоя происходит линейно, а в диффузном слое – по экспоненте. В настоящее время учение о ДЭС продолжает развиваться, т.к. оно имеет большое значение для понимания и усовершенствования таких практически важных процессов как коагуляция коллоидов, флотация, ионный обмен и др.
Рис. 4.1. Схема строения двойного электрического слоя и изменение потенциала.
Образование двойного слоя ионов приводит к появлению определенных электрических потенциалов на границе твердой и жидкой фаз. На твердой поверхности возникает заряд, называемый φ-потенциал. Знак φ-потенциала совпадает со знаком заряда потенцалобразующих ионов. φ-потенциал можно рассчитать по уравнению Нернста:
где
φ-потенциал равен работе переноса единичного (элементарного) заряда из бесконечно удаленной точки объема раствора на поверхность твердой фазы.
|
||||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 324; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.143.9.115 (0.01 с.) |
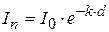
 - интенсивность прошедшего света;
- интенсивность прошедшего света;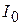 - интенсивность падающего света;
- интенсивность падающего света; - коэффициент поглощения;
- коэффициент поглощения; - толщина слоя.
- толщина слоя.

 - молярная концентрация растворенного вещества;
- молярная концентрация растворенного вещества; - молярный коэффициент поглощения вещества (не зависит от концентрации, но изменяется с длиной волны, температурой и природой растворителя).
- молярный коэффициент поглощения вещества (не зависит от концентрации, но изменяется с длиной волны, температурой и природой растворителя).
 - относительная прозрачность раствора.
- относительная прозрачность раствора. называется относительное поглощение раствора.
называется относительное поглощение раствора. и
и  , молярный коэффициент поглощения имеет вид
, молярный коэффициент поглощения имеет вид  , следовательно, если
, следовательно, если  , то раствор не адсорбирует свет.
, то раствор не адсорбирует свет.
 Для коллоидных систем применим при некоторых допущениях:
Для коллоидных систем применим при некоторых допущениях: :
:


 ,
, - электрический потенциал на поверхности;
- электрический потенциал на поверхности;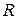 - универсальная газовая постоянная;
- универсальная газовая постоянная; - абсолютная температура;
- абсолютная температура; - заряд потенциалобразующих ионов;
- заряд потенциалобразующих ионов; - постоянная Фарадея (
- постоянная Фарадея ( )
) и
и  - активность ионов на поверхности и в растворе.
- активность ионов на поверхности и в растворе.


