
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Витебский государственный ордена Дружбы народовСтр 1 из 2Следующая ⇒
Витебский государственный ордена Дружбы народов медицинский университет Кафедра токсикологической и аналитической химии
по токсикологической химии для студентов 5 курса фармацевтического факультета
Витебск 2012
Методические указания по токсикологической химии для студентов 5 курса фармацевтического факультета составлены проф. Жебентяевым А.И. и обсуждены на заседании кафедры токсикологической и аналитической химии 31 августа 2012 года, протокол №1 ЗАНЯТИЕ № 1.Основные закономерности поведения токсических веществ в организме. Методы детоксикации организма при острых отравлениях Цель занятия: 1) Изучить механизмы всасывания, распределения и выведения токсических веществ, а также общие принципы диагностики острых отравлений; 2) Изучить методы детоксикации организма при острых отравлениях. ВОПРОСЫ К ЗАНЯТИЮ 1. Пути поступления токсических веществ в организм. 2. Основные виды транспорта токсических веществ через мембрану. Механизмы повреждения мембран. 3. Распределение токсических веществ в организме. Взаимодействие токсических веществ с рецепторами. 4. Пути выведения токсических веществ из организма. 5. Виды диагностических мероприятий при острых отравлениях. 6. Особенности клинической диагностики. 7. Лабораторная токсикологическая диагностика. 8. Основные этапы химико-токсикологического исследования. 9. Классификация основных методов детоксикации организма. 10. Методы усиления естественной детоксикации. 11. Методы искусственной детоксикации. 12. Методы антидотной детоксикации. Литература: [1] С.34-62, [8], [10]. ЗАНЯТИЕ № 2. Острые отравления, токсикокинетика и метаболизм чужеродных соединений в организме Цель занятия: выявить уровень знаний студентов по основным закономерностям поведения и метаболизму токсических веществ в организме, общим принципам диагностики острых отравлений и методам детоксикации организма при острых отравлениях. ВОПРОСЫ К ЗАНЯТИЮ 1. Пути поступления токсических веществ в организм. 2. Основные виды транспорта токсических веществ через мембрану. Механизмы повреждения мембран. 3. Распределение токсических веществ в организме. Взаимодействие токсических веществ с рецепторами.
4. Основные пути метаболизма токсических веществ в организме: классификация метаболических превращений, окисление микросомальными ферментами и немикросомальное окисление и восстановление, реакции биосинтеза. Факторы, влияющие на метаболизм. 5. Пути выведения токсических веществ и их метаболитов из организма. Кинетика выведения чужеродных соединений (период полувыведения, почечный клиренс). 6. Виды диагностических мероприятий при острых отравлениях. 7. Особенности клинической диагностики. 8. Лабораторная токсикологическая диагностика. 9. Основные этапы химико-токсикологического исследования. 10. Классификация основных методов детоксикации организма. 11. Методы усиления естественной детоксикации. 12. Методы искусственной детоксикации. 13. Методы антидотной детоксикации. Литература: [1] С.34-80, [8], [10]. ЗАНЯТИЕ №3. Группа веществ, изолируемых полярными растворителями. Цель занятия: Изучить основные методы изолирования лекарственных веществ кислотного, слабоосновного и основного характера. ВОПРОСЫ К ЗАНЯТИЮ 1. Классификация и токсикологическое значение лекарственных веществ, изолируемых полярными растворителями. 2. Физико-химические свойства и состояние лекарственных веществ кислотного и основного характера в растворах. 3. Особенности определения лекарственных веществ в биологических объектах. 4. Отбор и подготовка проб. 5. Основные этапы изолирования лекарственных веществ при общем и направленном анализе. 6. Качественные и количественные факторы, влияющие на изолирование лекарственных веществ из внутренних органов (твердо-жидкостная экстракция). 7. Способы концентрирования лекарственных веществ. Жидкость-жидкостная экстракция. 8. Сорбционное концентрирование. Условия и основные этапы. 9. Общие методы изолирования лекарственных веществ полярными растворителями (методы Стаса-Отто, Драгендорфа, Васильевой, Крамаренко). Литература: [1] 172-234, [2] С.119-160, [4]. ХОД ЗАНЯТИЯ Лабораторная работа При подготовке к занятию заполнить лабораторный журнал. Для идентификации лекарственных веществ кислотного и слабоосновного характера проводят следующие реакции:
ПРОИЗВОДНЫЕ КСАНТИНА
ПРОИЗВОДНЫЕ ПИРАЗОЛОНА
Литература: [1] С.197-231, [2] С.133-153,227-231,236-239, [3] C.60-79, [4]. ХОД ЗАНЯТИЯ Лабораторная работа Выполнить реакции качественного обнаружения изучаемых веществ в соответствии с нижеприведенным перечнем. ХИНИН 1. С общеалкалоидными реактивами; 2. Обнаружение по флуоресценции; 3. Талейохинная проба; 4. Эритрохинная проба. ПАПАВЕРИН 1. С общеалкалоидными реактивами; 2. С реактивами Марки, Фреде, Манделина, Эрдмана; 3. С раствором хлорида кадмия (МКС). НОВОКАИН 1. Реакция образования азокрасителя; 2. С реактивом Драгендорфа; 3. Реакция Витали-Морена (оранжево-желтое окрашивание). НОВОКАИНАМИД 1. С реактивом Драгендорфа; 2. Реакция образования азокрасителя; 3. Реакция Витали-Морена (желто-коричневое окрашивание); 4. С хлоридом платины (МКС). ПРОИЗВОДНЫЕ ФЕНОТИАЗИНА (АМИНАЗИН, ДИПРАЗИН, ЛЕВОМЕПРОМАЗИН, ТИОРИДАЗИН) 1.С конц. серной ( азотной ) кислотой; 2. С реактивом Марки; 3. С реактивом Манделина; 4. С реактивом ФПН. АТРОПИН 1.С общеалкалоидными реактивами (р-вы Бушарда, Драгендорфа, Майера); 2. Реакция Витали-Морена; 3. Реакция с солью Рейнеке; 4. Реакция с пикриновой кислотой; 5. С п-диметиламинобензальдегидом. СКОПОЛАМИН 1. С общеалкалоидными реактивами; 2. Реакция Витали-Морена; 3.Реакция с солью Рейнеке; 4. С золотобромистоводородной кислотой. КОКАИН 1. С общеалкалоидными реактивами; 2. С перманганатом калия; 3. Реакция образования бензойно-этилового эфира; 4. Изолирование экгонина из биоматериала. МОРФИН 1. С общеалкалоидными реактивами; 2. С реактивами Марки, Фреде, Эрдмана, Манделина; 3. С хлоридом железа (111); 4. Реакция образования берлинской лазури. КОДЕИН 1. С общеалкалоидными реактивами; 2. С реактивом Марки; 3. Фотометрическое определение с тропеолином 00. ГЕРОИН 1. С общеалкалоидными реактивами; 2. С селеновой кислотой в серной кислоте (зеленая окраска); 3. С молибдатом натрия в конц.серной кислоте (фиолет.-зелен.-розов). ЭФЕДРИН 1. С реактивом Драгендорфа; 2. С сульфатом меди и сероуглеродом; 3. С 2,4-динитрохлорбензолом. СТРИХНИН 1. С реактивом Драгендорфа; 2. Реакция окисления дихроматом калия в конц. серной кислоте; 3. С реактивом Манделина; 4. Реакция Витали-Морена. ПРОМЕДОЛ 1. С общеалкалоидными реактивами; 2. С реактивом Марки. Литература: [1] С.112-171, [2] С.65-118, [4]. ЗАНЯТИЕ №6. Изолирование, методы обнаружения, количественного определения и метаболизм производных 1,4-бензодиазепина Цель занятия: изучить физико-химические свойства, спектральные характеристики и особенности химико-токсикологического анализа производных 1,4-бензодиазепина. ХОД ЗАНЯТИЯ Учитывая частые случаи отравления лекарственными препарами, относящимися к группе производных 1,4-бензодиазепина, а также отсутствие в учебной литературе достаточных сведений о свойствах, методах обнаружения, количественного определения лекарственных веществ этой группы на занятии необходимо изучить особенности химико-токсикологического анализа производных 1,4-бензодиазепина.
ВОПРОСЫ К ЗАНЯТИЮ 1. Структура и химические свойства производных 1,4-бензодиазепина. 2. Гидролиз производных 1,4-бензодиазепина. 3. Поведение производных 1,4-бензодиазепина в организме. 4. Химико-токсикологическое исследование на производные 1,4-бензодиазепина (схема исследования, основные этапы анализа по продуктам гидролиза и по нативному соединению). Литература: [1] С.285-292, [7] С.28-39. ХОД ЗАНЯТИЯ Каждому студенту предлагается ситуационная задача, при решении которой необходимо правильно выбрать метод изолирования и очистки анализируемого вещества, применить характерные реакции обнаружения, выбрать метод количественного определения. ПРИМЕРЫ ЗАДАЧ 1. Найден труп гр. Х, который длительно состоял на учете по поводу употребления наркотиков. Провести исследование внутренних органов и остатков порошка на кодеин. 2. В ванне с водой обнаружен труп женщины 52 лет, рядом найдена конвалюта из-под барбамила. Провести химико-токсикологическое исследование внутренних органов. 3. В больницу доставлен мужчина с признаками отравления тропановыми алкалоидами. Провести химико-токсикологическое исследование промывных вод, мочи и крови. 4. В больницу доставлен гр. Х в коматозном состоянии, наблюдавшийся в психоневрологическом диспансере по поводу шизофрении. Провести химико-токсикологическое исследование промывных вод, крови, мочи на аминазин. Литература: [1] С.172-295, [2] С.119-241, [4], [6] C.110-195. ХОД ЗАНЯТИЯ Лабораторная работа Составить схему химико-токсикологического исследования экстрактов из кислого и щелочного растворов. Получить биоматериал у преподавателя. Проверить рН среды (при необходимости подкислить 20% раствором щавелевой кислоты до рН 2,5-3), перенести в делительную воронку и экстрагировать 5 мл хлороформа. Хлороформный экстракт поместить в сухой флакон с надписью «№... –К». Водный остаток в делительной воронке довести 25% раствором аммиака до рН 8,5-9 и экстрагировать 5 мл хлороформа. Хлороформный экстракт поместить в сухой влакон с надписью «№... –Щ». На этом занятии выполняется анализ экстракта из кислого раствора.
Литература: [1] С.197-234, [2] С.119-160, [3] С.56-79. [4]. ХОД ЗАНЯТИЯ На три предметных стекла нанести по 3-4 капли хлороформного экстракта из щелочной среды и выпарить досуха, на сухие остатки нанести по 1 капле 0,1 М раствора НС1 и по капле общеалкалоидных осадительных реактивов (раствор йода в иодиде калия, йодида висмута в иодиде калия, фосфорномолибденовой или фосфорновольфрамовой кислоты). Положительные реакции с общеалкалоидными реактивами указывают на необходимость проведения качественных реакций на алкалоиды и синтетические лекарственные вещества основного характера. Реакции на алкалоиды проводятся после удаления хлороформа. Литература: [2] С.119-160, [3] С.56-79, [4], [6]. ЗАНЯТИЕ №10. Составление заключения эксперта по результатам определения лекарственных веществ в биологическом материале. ЦЕЛЬ ЗАНЯТИЯ: составление заключения эксперта по результатам анализа биологического материала на наличие лекарственных веществ.
ХОД ЗАНЯТИЯ ВОПРОСЫ К КОЛЛОКВИУМУ 1. Классификация и токсикологическое значение лекарственных веществ, изолируемых полярными растворителями. 2. Физико-химические свойства и состояние лекарственных веществ кислотного и основного характера в растворах. 3. Особенности анализа биологических объектов на наличие лекарственных веществ. 4. Отбор и подготовка проб. 5. Основные этапы изолирования лекарственных веществ при общем и направленном анализе. 6. Качественные и количественные факторы, влияющие на изолирование лекарственных веществ из внутренних органов (твердо-жидкостная экстракция). 7. Способы концентрирования лекарственных веществ. Жидкость-жидкостная экстракция. 8. Сорбционное концентрирование. Условия и основные этапы. 9. Общие методы изолирования лекарственных веществ полярными растворителями (методы Стаса-Отто, Драгендорфа, Васильевой, Крамаренко). 10. Частные методы изолирования лекарственных веществ (методы Швайковой, Поповой, Валова, Саломатина, Крамаренко, Карташова) 11. Особенности изолирования морфина, производных ксантина, фенотиазина. 12. Классификация алкалоидов и синтетических лекарственных веществ основного характера. 13. Общеалкалоидные осадительные реактивы. 14. Подтверждающие методы определения лекарственных веществ. 15. Деление веществ, изолируемых полярными растворителями на две группы. Характеристика групп. 16. Изолирование, обнаружение, метаболизм производных барбитуровой кислоты (барбитал, фенобарбитал, бутобарбитал, этаминал натрий, барбамил), производных ксантина (кофеин, теобромин, теофиллин),производных пиразолона (антипирин, амидопирин, анальгин),производных 1,4-бензодиазепина (элениум, диазепам, нитразепам, оксазепам), производных фенотиазина (аминазин, дипразин, левомепромазин, тиоридазин),производных пиперидина (промедол),производных п-аминобензойной кислоты (новокаин, новокаинамид), алкалоидов группы тропана (атропин, скополамин, кокаин), алкалоидов группы фенантренизохинолина (морфин, кодеин,героин –синтетический аналог), алкалоидов группы индола (стрихнин), алкалоидов группы хинолина и бензилизохинолина (хинин, папаверин), ациклических алкалоидов (эфедрин).
Литература: [1] С.172-295, [2] С.119-241, [4]. ХОД ЗАНЯТИЯ Лабораторная работа Таблица 1. Значения Rf и RS (по барбиталу) для веществ кислотного и слабоосновного характера
Таблица 2. Значения Rf и RS (по аминазину) для веществ основного характера
Литература: [4]. ХОД ЗАНЯТИЯ · Контроль исходного уровня знаний 1. Правила работы на спектрофотометре, фотоэлектроколориметре и флуориметре. 2. Основные требования, предъявляемые к методам количественного определения токсических веществ в биологических жидкостях. 3. Применение физико-химических методов в химико-токсикологическом анализе. · Лабораторная работа Методика фотометрического определения папаверина (аминазина) В биожидкостях В пенициллиновый флакон с анализируемой пробой прибавляют 10 мл воды очищенной, перемешивают. Фильтруют в мерную колбу вместимостью 25 мл, прибавляют 1 мл 0,1% раствора поливинилового спирта (ПВС), 1 мл 0,07% раствора эозина, 2 мл 0,01 М раствора серной кислоты и доводят водой до метки. Параллельно готовят раствор сравнения, содержащий все реактивы за исключением определяемых соединений. Для приготовления раствора стандартного образца в мерную колбу вместимостью 25 мл помещают 2 мл стандартного раствора папаверина (аминазина) - 10 мкг/мл, прибавляют вышеуказанные реактивы и доводят водой до метки. Измеряют оптическую плотность раствора на ФЭКе при длине волны 540 нм, в кювете с толщиной слоя 2 см относительно раствора сравнения. Концентрацию папаверина (аминазина) в мкг/мл рассчитывают по формуле:
где АХ – оптическая плотность анализируемого раствора; где АСТ – оптическая плотность стандартного раствора. Методика количественного определения хинина в биожидкостях В пенициллиновый флакон с анализируемой пробой прибавляют 10 мл 0,01 М раствора серной кислоты, встряхивают 5 минут и фильтруют в пенициллиновый флакон. В качестве стандарта используют раствор хинина с концентрацией 1 мкг/мл. Измеряют интенсивность флуоресценции анализируемого и стандартного растворов. Концентрацию хинина в мкг/мл в анализируемой биожидкости рассчитывают по формуле:
где IХ – интенсивность флуоресценции анализируемого раствора; где IСТ - интенсивность флуоресценции стандартного раствора. Методика спектрофотометрического определения производных барбитуровой кислоты в биожидкостях В пенициллиновый флакон с анализируемой пробой прибавляют 10 мл воды очищенной. Встряхивают 5 минут. Фильтруют в пенициллиновый флакон. В кювету спектрофотометра с толщиной слоя 1 см помещают фильтрат и добавляют 3 капли 0,2 М раствора серной кислоты. Перемешивают. Измеряют оптическую плотность раствора при 240 нм. В качестве раствора сравнения используют воду очищенную. Затем в кювету с анализируемым раствором прибавляют 3 капли 30% спиртового раствора NaOH, перемешивают и измеряют оптическую плотность. В качестве раствора сравнения используют воду очищенную. Аналогично измеряют оптическую плотность стандартного раствора барбитала с концентрацией 10 мкг/мл. Концентрацию барбитуратов (мкг/мл) в анализируемой биологической жидкости рассчитывают по формуле:
где где Литература: [4]. ВОПРОСЫ К ЗАНЯТИЮ 1. Общая характеристика и классификации ядохимикатов. 2. Методы изолирования ядохимикатов из секционного материала и биологических жидкостей. 3. Химические методы обнаружения ядохимикатов. Элементный анализ. 4. Использование биохимических методов для анализа ядохимикатов (холинэстеразная проба). 5. Экологическое значение хлорсодержащих ядохимикатов (гептахлор, гексахлорциклогексан, полихлорбифенилы). 6. Токсикокинетика и ХТА фосфорсодержащих пестицидов (хлорофос, дихлорфос, карбофос, метафос). 7. Токсикокинетика и ХТА производных карбаминовой кислоты (севин). 8. Химико-токсикологический анализ синтетических пиретроидов. Литература: [1] С.393-414, [2] С.246-277, [5] С.20-30, [9], [11]. ЛИТЕРАТУРА 1. Крамаренко В.Ф. Токсикологическая химия. Киев, 1989. 2. Швайкова М.Д. Токсикологическая химия. М., 1975. 3. Белова А.Б. Руководство к практическим занятиям по токсикологической химии. М.,1976. 4. Жебентяев А.И. Лекции по токсикологической химии. 5. Крамаренко В.Ф., Туркевич Б.М. Анализ ядохимикатов. М.,1978. 6. Крамаренко В.Ф. Химико-токсикологический анализ. Киев, 1982. 7. Учебно-методическая разработка по теме «Группа веществ, изолируемых экстракцией полярными растворителями». М.,1987. 8. Лужников Е.А. Клиническая токсикология. М.,1994. 9. Информационный материал «Пестициды». 10. Информационный материал «Острые отравления и токсикокинетика ядов». 11. Методы определения микроколичеств пестицидов в продуктах питания, кормах и внешней среде: Справочник, т.1 и 2: 1992 г.
Витебский государственный ордена Дружбы народов медицинский университет Кафедра токсикологической и аналитической химии
по токсикологической химии для студентов 5 курса фармацевтического факультета
Витебск 2012
Методические указания по токсикологической химии для студентов 5 курса фармацевтического факультета составлены проф. Жебентяевым А.И. и обсуждены на заседании кафедры токсикологической и аналитической химии 31 августа 2012 года, протокол №1 ЗАНЯТИЕ № 1.Основные закономерности поведения токсических веществ в организме. Методы детоксикации организма при острых отравлениях Цель занятия: 1) Изучить механизмы всасывания, распределения и выведения токсических веществ, а также общие принципы диагностики острых отравлений; 2) Изучить методы детоксикации организма при острых отравлениях. ВОПРОСЫ К ЗАНЯТИЮ 1. Пути поступления токсических веществ в организм. 2. Основные виды транспорта токсических веществ через мембрану. Механизмы повреждения мембран. 3. Распределение токсических веществ в организме. Взаимодействие токсических веществ с рецепторами. 4. Пути выведения токсических веществ из организма. 5. Виды диагностических мероприятий при острых отравлениях. 6. Особенности клинической диагностики. 7. Лабораторная токсикологическая диагностика. 8. Основные этапы химико-токсикологического исследования. 9. Классификация основных методов детоксикации организма. 10. Методы усиления естественной детоксикации. 11. Методы искусственной детоксикации. 12. Методы антидотной детоксикации. Литература: [1] С.34-62, [8], [10].
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-17; просмотров: 165; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.58.247.31 (0.097 с.) |




 и
и  - оптические плотности анализируемого раствора в щелочной и кислой средах;
- оптические плотности анализируемого раствора в щелочной и кислой средах; и
и 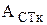 - оптические плотности стандартного раствора в щелочной и кислой средах;
- оптические плотности стандартного раствора в щелочной и кислой средах;


