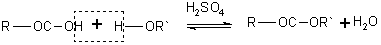Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Карбоновые кислоты. Номенклатура. Строение. Способы получения карбоновых кислот. Химические свойства. Механизм этерификации. Отдельные представители и их применение.
Органические соединения, содержащие карбоксильную группу СООН. По кол-ву этих групп различают одно-, двух- и многоосновные кислоты. Могут содержать Hal, а также группы NH2, С=О, ОН. Алифатические кислоты, у которых число атомов С в молекуле больше 6, относят к высшим жирным кислотам. По номенклатуре ИЮПАК, кислоты называют, выбирая за основу наибольшую длинную цепь, содержащую группу СООН, и добавляя к названию соединения-основы окончание "овая" и слово "кислота"; атому С карбоксильной группы приписывают номер 1, например СН3(СН2)4СН(СН3)СООН - 2-метилгептановая кислота. Часто к названию соединения-основы добавляют слова "карбоновая кислота", например С6Н11СООН - циклогексанкарбоновая кислота. При использовании этого способа наименования в алифатическому ряду атом С карбоксильной группы в нумерацию цепи не включается. Многие кислоты имеют тривиальные названия. В свободном состоянии кислоты находятся в плодах некоторых растений, крови, выделениях животных; они входят в состав жиров, эфирных и растительных масел, восков. Важную роль карбоновые кислоты играют в обмене веществ.
Свойства. Карбоксильная группа имеет строение, промежуточное между двумя предельными структурами:
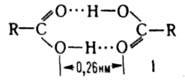
Группа планарна; длина связи С=О в различных кислотах составляет 0,118-0,126 нм, связи С=О - 0,121-0,137 нм; угол ОСО 118-125,5°; m 5,4.10-30 Кл.м. В твердом и жидком состоянии кислоты в результате возникновения водородных связей образуют устойчивые циклические димеры.
Атомы, образующие цикл, лежат практически в одной плоскости, а водородные связи (энергия 29 кДж/моль) почти линейны.
Получение: 1) Окисление альдегидов и первичных спиртов. В качестве окислителей применяются KМnО4 и K2Сr2О7. R-CH2-OH → R-CH=O → R-CO-OH спирт альдегид кислота 2) Гидролиз галогензамещенных углеводородов:
R-CCl3 + 3 NaOH → [R-C(OH)3] → R-COOH + Н2О + 3NaCl
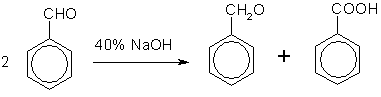
3) Получение карбоновых кислот из цианидов (нитрилов) CH3CN + 2Н2О → CH3COONH4. CH3COONH4 + HCl → СН3СООН + NH4Cl 4) Использование реактива Гриньяра по схеме: R-MgBr + СО2 → R-COO-MgBr + H2O → R-COOH + Mg(OH)Br 5) Гидролиз сложных эфиров: R-COOR1 + КОН → R-COOK + R'OH, R-COOK + HCl → R-COOH + KCl. 6) Получение бензойной кислоты:
Химические свойства. 1) В водном растворе карбоновые кислоты диссоциируют:
RCOOH 2) Образование солей: 2RCOOH + Мg → (RCOO)2Mg + Н2, 2RCOOH + СаО → (RCOO)2Ca + Н2О, RCOOH + NaOH → RCOONa + Н2О, RCOOH + NaHCO3→ RCOONa + Н2О + СО2↑. 3) Сложные эфиры:
4) Действие галогенов: СН3-СН2-СООН + Вr2 → СН3-СНВr-СООН + НВr 5) Непредельные кислоты: СН2=СН-СООН + Н2 → СН3-СН2-СООН, СН2=СН-СООН + Сl2 → СН2Сl-СНСl-СООН, СН2=СН-СООН + HCl → СН2Сl-СН2-СООН, СН2=СН-СООН + Н2O → НО-СН2-СН2-СООН,
6) Реакции декарбоксширования: CH3-CH2-COONa + NaOH → С2Н6↑ + Na2CO3
Механизм этерификации:
Представители:
Кислоты исходные соединения для получения промежуточных продуктов органического синтеза, в частности кетенов, галогенангидридов, виниловых эфиров, галогенкислот. Соли карбоновых кислот и щелочных металлов применяют как мыла, эмульгаторы, смазочные масла; соли тяжелых металлов - сиккативы, инсектициды и фунгициды, катализаторы. Эфиры кислот - пищевые добавки, растворители; моно- и диэфиры гликолей и полигликолей пластификаторы, компоненты лаков и алкидных смол; эфиры целлюлозы - компоненты лаков и пластмассы. Амиды кислот эмульгаторы и флотоагенты.
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 266; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.82.167 (0.008 с.) |

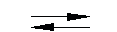 RCOO- + Н+
RCOO- + Н+