Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
И их выявление в биологических средах ⇐ ПредыдущаяСтр 2 из 2
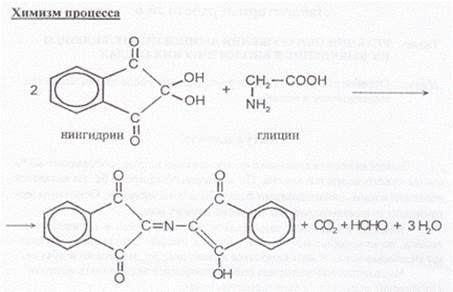
Цель: Отработать умения экспериментально исследовать свойства аминокислот и белков. Опыт № 1 Нингидриновая проба Реакция характерна для α-аминокислот и их остатков. Растворы α- аминокислот и белков при нагревании с нингидрином приобретают фиолетовое окрашивание. Методика эксперимента В одну из двух пробирок прилить 3 - 5 капель 1 % раствора яичного белка, в другую 3 – 5 капель 0,1 % раствора глицина. В каждую пробирку наливают по 2 – 3 капли 0,1 % водного раствора нингидрина. Содержимое пробирок осторожно нагреть. Описать наблюдения, сделать выводы.
Наблюдения__________________________________________ Выводы___ ___________________________________________ Опыт 2 Обнаружение серосодержащих α -аминокислот (реакция Фоля) Реакция Фоля позволяет обнаружить в белке аминокислоты, содержащие слабосвязанную серу, например:
Методика эксперимента В пробирку поместить 5 – 10 капель раствора яичного белка и вдвое больший объем 10 % раствора гидроксида натрия. Содержимое пробирки перемешать, нагреть до кипения (1 – 2 мин). К полученному щелочному раствору добавить 3 – 5 капель 10 % ацетата свинца и вновь прокипятить. Описать наблюдения. Химизм процесса При кипячении белка со щелочью α-содержащие аминокислоты образуют сульфид натрия.
Интенсивность окраски зависит от количества серосодержащих аминокислот в белке и от концентрации белка в растворе. Наблюдения__________________________________________ Выводы___ ___________________________________________ Опыт №3 Амфотерные свойства α-аминокислот Амфотерность α-аминокислот обусловлена наличием в молекулах карбоксильной и аминогрупп, за счет которых они образуют цвиттер-ион:
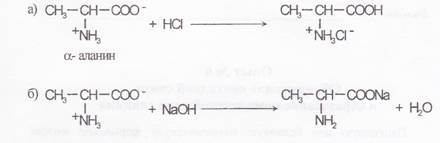
Методика эксперимента а) В одну пробирку поместить 3 – 5 капель 1 % раствора α-аланина и добавить по каплям 0,1 % раствор хлороводородной кислоты, подкрашенной конго. б) Во вторую пробирку поместить 3 – 5 капель 1 % раствора α -аланина и по каплям добавить 0,1 % раствора гидроксида натрия, подкрашенного фенолфталеином. Запасать наблюдения. Химизм процесса
Наблюдения__________________________________________ Выводы___ ___________________________________________ Опыт №4 Реакция глицина с формальдегидом Реакция позволяет защитить аминогруппу и используется для количественного определения карбоксильных групп в α-аминокислотах путем кислотно-основного титрования.
Методика эксперимента В пробирку поместить 5 капель 1 % раствора глицина и добавить 1 каплю метилового красного, раствор окрашивается в желтый цвет. К полученной смеси добавляют 3 – 5 капель формалина. При этом происходит изменение окраски. Химизм процесса
Блокируя аминогруппу формальдегид одновременно освобождает карбоксильную группу, которую далее можно анализировать методом титрования щелочью. Наблюдения__________________________________________ Выводы___ ___________________________________________
Опыт №5 Обнаружение пептидной связи и образование комплексной соли глицина Пептидную или белковую макромолекулу формально можно представить как продукт поликонденсации α-аминокислот, протекающей с образованием пептидной (амидной) связи между мономерными звеньями. Методика эксперимента В две пробирки прилить 3 – 5 капель 1 % раствора сульфата меди, добавить по каплям 10 % раствор гидроксида натрия до образования осадка. Далее в одну из двух пробирок приливают по каплям 1 % раствор глицина, а во вторую – раствор белка до растворения.
Наблюдения__________________________________________ Выводы___ ___________________________________________ Опыт №6
|
|||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 610; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.8.141 (0.006 с.) |