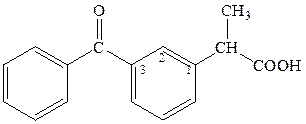Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Е.А. Краснов, А.А. БлинниковаСтр 1 из 5Следующая ⇒
СИБИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ФЕДЕРАЛЬНОГО АГЕНТСТВА ПО ЗДРАВООХРАНЕНИЮ И СОЦИАЛЬНОМУ РАЗВИТИЮ
Е.А. Краснов, А.А. Блинникова Номенклатура органических
УЧЕБНОЕ ПОСОБИЕ
Рекомендовано Учебно-методическим объединением по медицинскому и фармацевтическому образованию вузов России в качестве учебного пособия для студентов,обучающихся по специальности 040500(060108) -фармация.
Томск – 2008
УДК 615.015 (083.72) (075) ББК Р282 я7 К 782
Краснов Е.А., Блинникова А.А. Номенклатура органических лекарственных веществ. Учебное пособие. Томск: Сибирский государственный медицинский университет, 2008 – 124 с.
В учебном пособии представлены данные, связанные с построением химической структуры и формированием названий органического соединения. Рассмотрены виды номенклатур, принятые правилами ИЮПАК и основные классы соединений. В заданиях для самоподготовки на примерах распространенных лекарственных средств требуется построить формулу по химическому названию и наоборот, по указанной структурной формуле препарата дать его химическое название в соответствии с международной номенклатурой. Для проверки правильности выполнения задания приведены ответы на поставленные вопросы. Пособие снабжено 6 приложениями, и рассчитано на студентов фармацевтических факультетов высших учебных заведений. Табл.4. Библиогр. 16 назв.
Рецензенты: Заведующий кафедрой фармацевтической химии фармацевтического факультета ММА им. Сеченова, академик РАМН, д.ф.н. профессор А.П.Арзамасцев
Заведующая кафедрой фармацевтической химии очного факультета ГОУ ВПО «Пермская государственная фармацевтическая академия», д.ф.н., профессор Л.М.Коркодинова
Утверждено и рекомендовано к изданию методической комиссией фармацевтического факультета (протокол №1 от 7 февраля 2007 г.) и центральным методическим советом СибГМУ (протокол № 12 от 15 февраля 2007 г.).
© Е.А.Краснов, А.А.Блинникова, 2008 © Сибирский государственный медицинский университет, 2008 Содержание
Введение 4 Виды номенклатур, принятые правилами ИЮПАК 5
1. Заместительная номенклатура 5 1.1. Главные (старшие) группы в заместительной номенклатуре 6 2. Радикально-функциональная номенклатура 7 3. Алфавитный порядок расположения заместителей 10 4. Принципы правил ИЮПАК, применяемые для построения химических названий 11 Классы соединений 13 Алифатические соединения 1. Ациклические алканы, их галоген- и кислородсодержащие соединения 13 1.1. Ациклические радикалы 13 1.2. Галогенпроизводные 14 1.3. Спирты 14 1.4. Простые эфиры 15 1.5. Альдегиды 16 1.6. Кетоны 17 1.7. Кислоты и их производные 19 1.8. Аминокислоты 20 1.9. Амиды, имиды 21 1.10. Амины 22 Лактоны, лактамы 23 Терпены 24 Фенолы 25 Ароматические кислоты 26 Понятие ''обозначенный'' водород 26 Производные азепина и бензодиазепина 27 Глициды 29 Стероиды 32 Задания для самоподготовки 35 Ответы к заданию для самоподготовки 74 Приложение 1 110 Приложение 2 115 Приложение 3 116 Приложение 4 118 Приложение 5 121 Приложение 6 123 Литература 124 Введение В реальной жизненной ситуации в своей деятельности провизору приходится решать ряд задач, исходя из аннотации на лекарственное средство. 1. Построить формулу по химическому названию или соотнести его структуру с химическим названием. 2. Исходя из химической структуры, дать прогноз физико-химических свойств (агрегатное состояние, растворимость в воде, полярных и неполярных органических растворителях, слабых кислотах и основаниях). 3. Установить, какие из нижеперечисленных констант и почему могут быть использованы для характеристики фармацевтического препарата: температура плавления и кипения, 4. Охарактеризовать реакционную способность молекулы по отношению к слабым и сильным кислотам, щелочам, окислителям, восстановителям, кислороду воздуха, углекислоте, воде, нагреванию. 5. Обосновать возможные реакции идентификации препарата. 6. Выбрать и обосновать возможные методы количественного определения данного препарата. 7. Представлять, какие вещества (исходя из структуры препарата) могут быть или возникнуть в качестве примесей в процессе хранения лекарственного средства. 8. Знать требования к хранению препарата, исходя из его физико-химических свойств.
9. Знать вопросы взаимосвязи ''структура-действие'' и характер фармакофоров. Для решения данных задач важное значение приобретает знание химической структуры лекарственного вещества, умение дать правильное название, исходя из представленной структурной формулы и наоборот. Это позволяет умело использовать аннотации на зарубежные препараты и другие информационные материалы. Процесс формирования названия органического соединения включает следующие этапы: 1) определяют тип номенклатуры (заместительная, радикально-функциональная, заменительная и т.д.); 2) определяют тип характеристической группы, которую следует принять за главную; 3) определяют родоначальную структуру (главную цепь, старшую циклическую систему); 4) дают название исходной структуре и основным группам; 5) дают название префиксам; 6) проводят нумерацию; 7) объединяют частичные названия в общее полное название, придерживаясь алфавитного порядка для всех определяемых префиксов. Номенклатура – это совокупность названий веществ, их групп и классов, а также система правил, обеспечивающих одинаковую связь названий и формул, выражающих строение молекул. Основой для названий служит структурная формула.
Тип номенклатуры – заместительная; главная группа – СООН, карбоксильная; родоначальная структура – алифатическая цепь.
Виды номеклатур, принятые правилами ИЮПАК* (Международный союз теоретической и прикладной химии) Заместительная номенклатура
По этой номенклатуре определяется старшая (главная) группа, а также родоначальная структура вещества, лежащего в основе называемого соединения, к которой непосредственно присоединена старшая группа. Родоначальную структуру нумеруют так, чтобы главная группа получила наименьший локант. Локантами называют цифры или буквы, указывающие расположение составных частей строения вещества, т.е. они играют роль адресов.
Указанное соединение называют: 3-(4-Аминофенил)-3-метилбутановая кислота; здесь родоначальная структура – алифатическая цепь, с ней связана старшая характеристическая группа (карбоксильная старше аминогруппы). ИЮПАК (International Union Pure Applied Chemistry) – Международный союз чистой и прикладной химии
Соединение структуры
называют 3-(4-Аминобутил-2)-бензойная кислота; старшая группа – карбоксил, связанная с бензольным ядром. При выборе родоначальной структуры учитывается следующее: I. Для ациклических структур: 1) максимальное число старших характеристических групп; 2) максимальная ненасыщенность по совокупности двойных и тройных связей; 3) максимальная длина цепи. II. Для циклических структур: 1) все гетероциклы старше карбоциклов; 2) старшинство гетероциклов определяется природой гетероатома: N>О>S; 3) максимальное число циклов; 4) наличие в системе большого цикла; 5) максимальное число узловых атомов.
Классы соединений Алифатические соединения Лактоны, лактамы
Внутримолекулярные сложные эфиры, образующиеся в результате взаимодействия гидроксильной и карбоксильной групп гидроксикислот, сопровождающегося выделением молекулы воды с образованием циклической системы, называют ЛАКТОНАМИ.
Лактоны, получаемые из моногидроксикислот, помимо названий с окончанием ''-лактон'', можно называть с добавлением суффикса ''-олид'' к названию соответствующего углеводорода.
Если полигидроксикислота имеет тривиальное название, то образующийся из нее лактон может быть назван, исходя из этого названия, как в случае D-глюконо-1,4-лактона
Соединения, содержащие группы –CO-NH- или –C(OH)=N-, включенные в цикл, предпочтительно называют как гетероциклические соединения, но они могут быть названы с окончанием ''-лактам'' или ''лактим'' соответственно. Многие соединения имеют тривиальные названия, например:
кумарин изокумарин фталид
Терпены
Ациклические терпены (С10Н16) получают систематические названия, в то время как для родоначальных циклических монотерпенов ИЮПАК признают полусистематические названия. Структурам приписана фиксированная нумерация, например:
п-ментан пинан борнан
п-ментандиол-1,8 гидрат (терпингидрат) Широко известный препарат камфора, исходя из вышеизложенного, может быть назван борнанон-2 или 2-оксоборнан,
а для ментола
название будет 3-гидроокси-n-ментан (ГФ Х: 2-изопропил-5-метилциклогексанол-1) Для сесквитерпенов, дитерпенов и тритерпенов применяются систематические названия. Производные тетратерпенов, витамины группы А номенклатурой ИЮПАК рекомендуется называть ретинол, ретиналь, ретиновая кислота и т.п.
R=CH2OH – ретинол R=COH – ретиналь R=COOH – ретиновая кислота Фенолы
Имеется множество тривиальных названий:
ванилин пикриновая кислота фенол
и другие, которые допускаются правилами ИЮПАК. Название фенолятов образуется добавлением к названию исходного соединения суффиксов (''-олят'') и названия металла. Например: С6Н5ОNа – фенолят натрия. С другой стороны, название этих соединений может быть составлено из названия катиона и радикала с добавлением суффикса ''-оксид'', например С6Н5ОNа – феноксид натрия.
Ароматические кислоты
бензол-1,2-дикарбоновая пирролкарбоновая-1 кислота кислота (пиррол-1-карбоновая кислота) (фталевая кислота) Среди названий кислот циклических структур нет строгой последовательности в окончаниях, например: бензойная кислота, фталевая кислота, никотиновая кислота. Такое использование полутривиальных названий разрешается. Например:
(кислота дигидроксибензойная)
Глициды (углеводы)
У моносахаридов от С3 до С6 (см. Приложение 6) применяют тривиальные названия (арабиноза, рибоза, глюкоза, галактоза, манноза, фруктоза). Однако можно составлять и систематические наименования. Для этого используют: 1) один или несколько префиксов, описывающих конфигурацию; 2) цифровой слог, определяющий число атомов углерода в цепи; 3) суффиксы ''-оза'' (для альдоз) и ''-улоза'' (для кетоз). Каждый префикс соединения состоит из написанного курсивом наименования альдозы без окончания ''-за'' (рибо-, глюко- и т.д.). префиксу предшествует описание конфигурации хирального атома углерода (обозначенного наибольшим локантом) буквами D и L, и аномерного буквами На примере глюкозы рассмотрим составление систематического названия. Для установления связи между структурой и названиями моносахаридов удобны проекции Фишера.
D-глицериновый альдегид D-глюкоза L-глюкоза
Обозначение D получает тот из стереоизомеров, конфигурация последнего хирального центра которого соответствует конфигурации правовращающего глицеринового альдегида (т.е. если НО – группа нижнего хирального центра расположена справа используют префикс D, а если слева – префикс L). При нумерации моносахаридов карбонильная группа получает наименьший локант. Если это СНО – группа – это номер 1. Если это СО – группа, то нумерацию начинают с ближнего к ней конца цепи. В случае моносахаридов в циклической форме (карбонильная группа и один из гидроксилов реагируют друг с другом, образуя полуацеталь или полукеталь). Карбонильный углерод 1 становится хиральным (аномерным) центром. Для указания его конфигурации используют обозначения Обозначение Аномерные префиксы
В циклических формах моносахаридов почти всегда имеются пяти- или шестичленные кольца (включая атом кислорода), очень редко – семичленные (например: гептрозы, содержащиеся в семействе толстянковых). Для указания размера колец существуют два способа.
1. Две последние буквы названия моносахарида (''за'') замещают на окончание ''фураноза'' в случае пятичленного кольца и ''пираноза'' в случае шестичленного. Фураноидные циклы почти плоские, у пираноидных – наиболее устойчива конформация кресла.
2. Для обозначения размера цикла пользуются локантами. Они указывают номера двух атомов углерода, с которыми связан находящийся в цикле кислород: первым ставят номер С-атома потенциальной карбонильной группы, номера разделяют запятой, помещают в скобки и располагают в конце названия ациклической формы. Разность между локантами составляет 3 – для фураноз и 4 – для пираноз. Недостатком проекций Фишера является отсутствие представлений о действительной форме колец. Для этих целей получили распространение формулы Хеуорса. В них углеродная цепь изображается горизонтальной, потенциальная карбонильная группа должна находится справа. Углеродная цепь находится как бы перед плоскостью бумаги, а кислородный мостик – за ней.
Правило для Для моносахаридов
кольца) (выше плоскости кольца)
Дисахариды называют тривиальными названиями: сахароза, лактоза и т.д. Однако можно использовать и систематические названия. Например, сахарозу можно назвать как
Систематические названия более информативны, т.к. они указывают места соединения, величину циклов, стереометрическое семейство, конфигурацию каждой составной части. Так, из систематического названия сахарозы видно, что оба углевода, входящие в состав дисахарида, отличаются друг от друга величиной цикла и аномерной конфигурацией:
Стероиды
В основе стероидов лежит насыщенная кольцевая система циклопентано[а] фенантрена, называемая стераном. Символ [а] указывает порядок сочленения циклопентановой и фенантреновой циклической систем. Вследствие сложности их стереохимии и наличия большого числа стероидов для этих соединений разработана обширная специализированная номенклатура. Применение же систематической номенклатуры со стероидным соединениям привело бы к непомерно длинным и трудным для понимания названиям. Поэтому в соответствии с номенклатурой ИЮПАК основные скелеты стероидов обозначены следующими тривиальными названиями: Холестан – корневое название скелета стеринов. Холан – название скелета желчных кислот. Андростан – название скелета андрогенов. Прегнан – корневое название скелета гестагенов и гормонов надпочечников. Эстран – название скелета эстрагенов. Для удобства отдельные кольца обозначают латинскими буквами от А до D. В стероидах кольца, за исключением эстрогенных гормонов, алифатические. Нумерация в кольцах А и В идет по знаку Нумерация и стереохимия скелета стероидных соединений представлены на формуле:
Следовательно, например в холестерине гидроксильная группа у С-3 находится в цис -положении по отношению к ангулярной СН3-группе в положении 10, а в экдистероне ОН-группы у С-3 и С-14 находятся в транс -положении по отношению друг к другу. У стероидов обычно включают конфигурацию всех центров, кроме С-5. Конфигурацию в положении С-5 следует указывать особо, т.к. может встречаться как 5
урсан
Атом Н или, соответственно, СН3-группа при С-13 расположены над плоскостью листа бумаги. Для обозначения конфигурации других атомов Н или заместителей применяют Кольца А и В могут быть связаны по цис- или транс-типу. При транс-сочленении атом водорода при С-5 имеет
5 (транс-сочленение) (цис-сочленение)
Для стероидных производных, имеющих тривиальные названия, употребляют суффиксы, взятые из систематической номенклатуры. Так, эстрадиол имеет две гидроксильные группы, тестостерон – кетонную группу и т.д.
Задания для самоподготовки 1) По предложенному химическому названию написать структурную формулу препарата. 2) По структурной формуле препарата дать его химическое название в соответствии с международной номенклатурой.
Список обозначений и сокращений ** Общепринятое международное непатентованное название (МНН), зарегистрированное ВОЗ или INN (International Nonproprietary Names). * МНН, рекомендуемое ВОЗ q Химическое название, принятое в соответствии с международной терминологией. ■ Химическое название отечественных препаратов в соответствии с действующей в нормативном документе терминологией. Авс. Австрия Бол. Болгария Бг. Бельгия Вел. Великобритания ВР Венгрия Голл. Голландия Гер. Германия Дан. Дания Изр. Израиль Инд. Индия Исп. Испания Ит. Италия Кан. Канада Нор. Норвегия ПР Польша Рум. Румыния РФ Российская Федерация Слов. Словения США Соединенные Штаты Америки Тур. Турция Фин. Финляндия Фр. Франция Чех. Чехия Хор. Хорватия Шв. Швеция Швр. Швейцария Эст. Эстония Яп. Япония Алифатические соединения Ароматические соединения Фенолы, хиноны и их производные 19.
20. Урегит (ВР) Кислота этакриновая** q [2,3-Дихлор-4-(2-метилен-1-оксобутил) феноксиуксусная кислота 21. Клотам (Фин.) Кислота толфенамовая** q 3-[(3-Хлор-2-метилфенил)амино] бензойная кислота 22. Кислота мефенаминовая**(РФ) q 2-[(2,3-Диметилфенил)амино] бензойная кислота ■ N-(2,3-Диметилфенил) антраниловая кислота
23.
24.
25. Бенорал (Вел.) Бенорилат** q 4-(Ацетиламино) фениловый эфир 2-(ацетокси) бензойной кислоты 26. Буфенокс (РФ) Буметанид** □ 3-(Аминосульфанил)-5-(бутиламино)-4-феноксибензойная кислота
27.
28.
29. Дибунол (РФ) Бутилейтед Гидрокситолуен* q 2,6-Бис(1,1-диметилэтил)-4-метилфенол ■ 2,6-Ди-трет-бутил-4-метилфенол 30. Фепранон (РФ) Амфепрамон* □ 2-(Диэтиламино)-1-фенил-1-пропанон (и с гидрохлоридом) ■ 2-(Диэтиламино)-1-фенилпропанон-1 31. Ормидол (Слов.) Атенолол** (Хор., Герм., Рум., Бол.), Ормидол (Слов.), Тенормин (Вел.), Тенолол (Инд.) q 4-[2-Гидрокси-3-[(1-метилэтил)амино] пропокси] бензолацетамид 32. Хлоракон (РФ) Бекламид** q 3-Хлор-N-(фенилметил) пропионамид ■ Бензиламид- 33. Фенилин (РФ) Фениндион** q 2-Фенил-1 Н -инден-1,3(2 Н)-дион ■ 2-Фенилиндандион-1,3 34. Практолол* (ПР) q N-[4-[2-Гидрокси-3-[(1-метилэтил)амино]пропокси]-фенил] ацетамид 35. Коронтин (ВР) Прениламин** q N-(1-Метил-2-фенилэтил)-3,3-дифенилпропанамин 36.
37. Калипсол (ВР), Кеталар (Вел.) Кетамин Гидрохлорид* q (±)-2-(2-Хлорфенил)-2(метиламино)-циклогексанон ■ 2-Метиламин-2(2-хлорфенил)-циклогексанона гидрохлорид
38.
39.
40.
41. Зитазониум (ВР), Нольвадекс (Вел.) Тамоксифен* (Фин., Хор., Авс., РФ) q (z)-2-[4-(1,2-Дифенил-1-бутенил)фенокси]-N,N-диметилэтанамина цитрат 42.
43.
44.
45.
46.
47.
48.
49. Ритмонорм (Герм.), Пролекофен (Слов.) Пропафенона гидрохлорид** ¨ 1-[2-[2-Гидрокси-3-(пропиламино)-пропокси]фенил]-3-фенил-1-пропанона гидрохлорид 50.
51.
52.
53.
54.
55. Допафлекс (ВР), Л-Допа (Допаркин) (Фин.) Леводопа** (Инд.) ¨ 3-Гидрокси-L-тирозин
56.
57. Вентолин (Вел., Слов.), Сальбувент (Фин.), Сальбупарт (ПР) Сальбутамол* (ПР, РФ) ¨ α- [[(1,1-Диметилэтил)амино]метил]-4-гидрокси-1,3-бензолдиметанол (и в виде сульфата) 58.
59.
60. Бимарал (Слов.) Бромоприд** ¨ 4-Амино-5-бром-N-[2-(диэтиламино)этил]-2-метоксибензамид 61. Новокаинамид (РФ) Прокаинамид Гидрохлорид** ¨ 4-Аамино-N-[2-(диэтиламино)этил]-бензамида гидрохлорид ■ ß- Диэтиламиноэтиламида-n-аминобензойной кислоты гидрохлорид 62.
Йодированные производные ароматических и арилалифатических аминокислот 63. Фалигност (Гер.) Кислота иомегламиковая** q 5-[(3-Амино-2,4,6-трийодфенил)-метиламино]-5-оксопентановая кислота 64. Йопагност (Чех.) Кислота иопаноевая** q 3-Амино-2,4,6-трийодбензол- 65. Димер-икс (Гер.) Кислота иокармик** q 3,3-[(1,6-Диоксо-гександиил)диимино]-бис[2,4,6-трийод-5-(метиламино)карбонил] бензойная кислота
66.
67.
Бензосульфокислоты Бензосульфаниламиды и их производные 68. Букарбан (ВР) Карбутамид** ¨ 4-Амино-N-[(бутиламино)карбонил]-бензолсульфонамид
69.
70. Манинил (Герм., Ит.), Глибенкламид ABD 5 (Хор.), Гилемал (ВР), Глибамид (Изр.) Глибенкламид** (РФ, Эст.) ¨ 5-Хлор-N-[2-[4-[[[(циклогексиламино)карбонил] амино]сульфонил]фенил]этил]-2-метоксибензамид ■ N-{4-[2-(5-Хлор-2-метоксибензамидо)-этил]-бензосульфанил}- N- циклогексилмочевина 71. Кальций Добезилат** (РФ, Гер.) ¨ Кальциевая соль 2,5-дигидрокси-бензосульфоновой кислоты ■ Кальция 2,5-дигидрокси-бензолсульфоната дигидрат 72. Диакарб (ПР) Ацетозоламид** ¨ N-[5-(Аминосуфонил)-1,3,4-тиадиазол-2-ил]ацетамид 73. Фтазин (РФ). Фталилсульфапиридазин** ¨ 2-[[[4-[[(6-Метокси-3-пиридазинил)амино]сульфонил]фенил]амино]карбонил] бензойная кислота ■ 6(n-Фталиламинобензолсульфаниламидо)-3-метоксипиридазин 74.
75.
Элементоорганические соединения 76. Осарсол (РФ) Ацетарсол** Akritоin ¨ 3-(Ацетамино)-4-гидроксифениларсиновая кислота ■ 3-Ацетамино-4-гидроксифенилмышьяковая кислота Л и т е р а т у р а
1. Бенкс Дж. Названия органических соединений – М.: Химия. 1980.–302с. 2. Гауптман З., Грефе Ю., Ремане Х. органическая химия. – М.: Химия, 1979. – С. 687 – 694. 3. Государственная фармакопея СССР. Х изд. – М.: Медицина, 1986. – 1079с. 4. Джилкрид Т. Химия гетероциклических соединений: Пер. с англ. – М.: Мир, 1996. – 464с. 5. Кан Р., Дермер О. Введение в химическую номенклатуру. – М.: Химия, 1983. – 223с. 6. Лепахин В.К., Шашкова Г.В. Справочник синонимов лекарственных средств. –М.: ВЦНФИ, 1991. – 172с.; Изд. 3-е, перераб. и доп. – М.: РЦ «фармединфо», 1995, – 112с. 7. Машковский М.Д. Лекарственные средства. – 14-изд., перераб. и доп. – М.: ООО «Изд-во Новая Волна», 2002. – Т.1. – 540с. 8. Международная фармакопея: 3-е изд Т.3. Спецификации для контроля качества фармацевтических препаратов. – Женева, 1990. – 435с. 9. Морисон Р., Бойд Р. Органическая химия. – М.: Мир, 1974. – 1132с. 10. Номенклатурные правила ИЮПАК по химии. Т. 3, полутом 2. – М., 1983. – 404с. 11. Органическая химия: Учеб. для вузов: В 2 кн./В.Л.Белобородов, С.Е. Зурабян, А.П. Лузин, Н.А. Тюкавкина; Под ред. Н.А. Тюкавкиной. – М.:Дрофа,2002 12. Регистр лекарственных средств России: Энциклопедия лекарств. – М., 2003. – 1438с. 13. Степаненко Б.Н. Курс органической химии. Ч. I. – М.: Высшая школа. 1981. – 464с. 14. Стоддарт Дж. Стереохимия углеводов. – М.: Мир, 1975. – 304с. 15. Цуркан А.А., Платонова Н.А. Построение химической формулы лекарственного средства органического строения по его химическому названию. – Рязань, 1987. – 68с. 16. The United States pharmacopeia. USP 26, 2002. – 2921p.
СИБИРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-08; просмотров: 664; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.200.226 (0.405 с.) |



 ,
,  ,
,  ,
,  , n,
, n,  .
. Например:
Например: 




 -валеролактон или пентанолид-5
-валеролактон или пентанолид-5

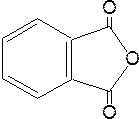




 При наличии заместителей родоначальные названия модифицируют, например:
При наличии заместителей родоначальные названия модифицируют, например:



 При составлении названий ароматических кислот используют способ 2 (см. раздел кислоты и их производные):
При составлении названий ароматических кислот используют способ 2 (см. раздел кислоты и их производные):
 2,3-дигидроксибензойная кислота
2,3-дигидроксибензойная кислота и
и  .
.


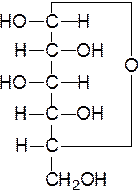
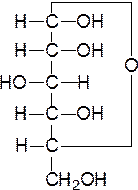
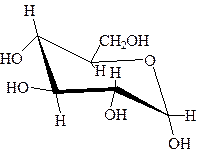
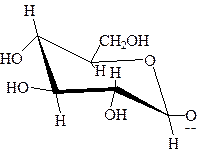



 над
над под (ниже плоскости
под (ниже плоскости

 над
над под
под
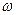 (омега), а у С и D – по знаку ~. Вертикальными линиями у С-10 и С-13 обозначены ангулярные метильные группы. Пространственная направленность заместителей помечается греческими буквами
(омега), а у С и D – по знаку ~. Вертикальными линиями у С-10 и С-13 обозначены ангулярные метильные группы. Пространственная направленность заместителей помечается греческими буквами 



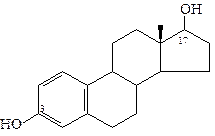 Эстратриен-1,3,5(10)-диол-3,17
Эстратриен-1,3,5(10)-диол-3,17