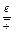Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Наследственности и изменчивостиСтр 1 из 6Следующая ⇒
ГЕНЕТИКА И ЭВОЛЮЦИЯ
ГЕНЕТИКА И СЕЛЕКЦИЯ
Учебно-методическое пособие
Специальность: 020200.62;020400.62-биология
ЧЕРЕПОВЕЦ Рассмотрено на заседании кафедры Биологии 12.10.2012 г., протокол № 3. Одобрено редакционной комиссией ФБиФК ФГБОУ ВПО ЧГУ, протокол № 2 от 16.10.2012 г.
Рецензенты: Н.А.Пакляшова – канд. биол. наук, доцент (ЧГУ); А.А. Артеменков – канд. биол. наук, доцент (ЧГУ)
Научный редактор: А.П. Добрынин, д-р биол. наук, профессор
© Петрова В.В., 2012 © ФГБОУ ВПО «Череповецкий государственный университет», 2012 Введение
Учебно-методическое пособие предназначено для студентов специальности 020200.62; 020400.62.- «Биология» как руководство по лабораторному практикуму, а также для организации самостоятельной работы по генетике. В пособии рассматриваются вопросы биологии разведения дрозофилы, строения ее хромосом, сравнительная характеристика мутаций дрозофилы, а так же, правила постановки гибридологических опытов с ней. Дрозофила – удобный объект для теоретических и практических исследований. Она легко размножается в лабораторных условиях, имеет короткий цикл развития, плодовита, обладает четко выраженными морфологическими признаками. Благодаря небольшому числу хромосом, большому числу спонтанных и индуцированных мутантных рас, часто характеризующихся четким проявлением измененных признаков, она может служить модельным объектом при проведении ряда лабораторных работ со студентами. Кроме этого часть пособия посвящена методике решения генетических задач. Таким образом, курс лабораторных работ направлен на усвоение студентами лекционной программы по генетике, а также способствует развитию практических навыков самостоятельной постановки студентами генетических опытов.
Д розофила как объект изучения закономерностей Биология развития дрозофилы В лаборатории дрозофилу (Drosophila melanogaster) разводят на специальной питательной среде. Яйцо дрозофилы длиной около 0,5 мм, снабжено двумя отростками, при помощи которых оно держится на поверхности среды. Самки откладывают яйца вскоре после оплодотворения. В благоприятных условиях каждая самка откладывает до 50–80 яиц в сутки, в течение 3–4 сут. она может отложить более 200 шт.
В лабораторных условиях личинки появляются из яиц через 20–24 ч после оплодотворения. Личиночный период состоит из трех возрастов. Первый и второй возрасты заканчиваются линьками, третий – окукливанием, которое начинается примерно через 4 сут. после вылупления из яйца. Первое время после вылупления из яйца личинки находятся на поверхности среды, затем уходят вглубь, интенсивно питаются, а перед окукливанием покидают среду, перестают питаться и некоторое время ползают по стенкам стаканчика или пробирки. Затем они становятся неподвижными, значительно сокращаются в длину и приобретают характерную для куколки форму. В состоянии куколки они находятся примерно 4 сут. За это время разрушаются личиночные органы, за исключением гонад и нервной системы, и формируются органы взрослой мухи. В конце стадии куколки сквозь оболочку просвечивают темные участки тела, хорошо видны глаза, особенно если они имеют яркую окраску.
Рис. 1. Дрозофила: 1 — самка; 2 — самец
Молодые, только что вылупившиеся мухи, имеют длинное желтоватое тело, почти лишенное пигмента, короткие, еще не расправленные крылья. Через 8 ч самки уже способны к оплодотворению. Для скрещивания необходимо брать девственных самок, не старше 8 ч после вылупления. Самки начинают откладывать яйца с конца вторых суток и продолжают до конца жизни. Самки дрозофилы отличаются от самцов по величине и ряду других морфологических признаков (рис. 1). Они обычно несколько крупнее самцов; конец брюшка у них заостренный, в то время как у самца форма брюшка округлая, так как самец дрозофилы имеет сплошь пигментированные (черные) последние брюшные тергиты. Последние сегменты брюшка у самок пигментированы значительно слабее, чем у самца, кроме того, у самцов имеются так называемые половые гребешки в виде ряда крепких хитиновых щетинок на первом членике передних ног. Однако этот признак можно различить только под бинокулярной лупой, поэтому в практической работе ориентируются преимущественно на форму и пигментацию брюшка.
Инвентарь и оборудование, необходимые при работе с дрозофилой 1. Стаканчики из толстого стекла высотой 5-7 см и диаметром 2,5-3 см. 2. Тонкий глазной пинцет и мягкая кисточка (перышки). 3. Молочно-белое стекло размером 5 ´ 10 см. 4. Бинокулярная лупа или небольшие настольные лупы различных конструкций с увеличением не менее, чем в четыре раза. 5. Часовое стекло. 6. Серный эфир. 7. Эфиризатор, или морилка. 8. Бутыль с небольшим количеством отходов спирта (¼ часть ее объема). В эту бутыль выбрасываются ненужные мухи после анализа. 9. Вата для изготовления пробок. 10. Колба и плитка для приготовления питательной среды. 11. Мензурка, весы, карандаш, этикетки, карандаш по стеклу.
Питательные среды и их приготовление Главные составные части питательных сред для дрозофилы - дрожжи и сахар. В питательную среду обычно добавляют агар-агар. Он придает среде желеобразную консистенцию. Агар-агар должен быть светлым, прозрачным, хорошо очищенным от химических примесей. Ниже приводится ряд наиболее распространенных и доступных рецептов приготовления питательных смесей, рассчитанных на 50 пробирок:
Для приготовления среды по рецепту III (на 14 стаканчиков) - агар-агар предварительно замачивают в дистиллированной холодной воде в течение 30-40 мин. в плоскодонной колбе (в ней будет в дальнейшем вариться питательная среда). Дрожжи тщательно растирают, помещают в эту же колбу и кипятят на плитке постоянно тщательно перемешивая 40 минут. Затем в смесь засыпают манную крупу и сахар и варят еще 10 мин. Из изюма предварительно удаляют косточки, тщательно промывают его, растирают в фарфоровой ступке, кладут в кипящую смесь и варят еще 10-20 минут. Смесь варят на слабом огне при тщательном перемешивании. Готовую среду тут же осторожно, не попадая на стенки, разливают в тщательно вымытые и простерилизованные пробирки, стаканчики или баночки (примерно на 1/5 их высоты), закрывают стерильной ватной пробкой и охлаждают до комнатной температуры. В таком виде среду можно использовать либо сразу после охлаждения, либо через некоторое время. Хорошо приготовленная среда может храниться в холодильнике 3-4 сут. в стаканчиках или пробирках, закрытых ватными пробками. Перед тем как поместить мух на среду в стаканчики, поверхность среды засевают дрожжами. Для этого свежие дрожжи разводят в дистиллированной воде до консистенции сливок (на 20 мл. дистиллированной воды - «горошина» дрожжей), несколько капель переносят на поверхность среды и дают ей постоять 30 минут. Затем дрожжевую воду из стаканчиков сливают. В приготовленные таким образом стаканчики со средой переносят мух либо для размножения, либо специально подобранные пары для скрещивания. При содержании мух среду периодически увлажняют дистиллированной водой, не допуская ее высыхания. По такой же методике готовят среды и по другим рецептам. Дрожжи для приготовления сред должны быть обязательно свежими, среда не слишком твердой (молодые личинки не могут проникнуть в глубь твердой среды и погибают) и не слишком жидкой (в жидкой среде могут погибнуть отложенные яйца).
Наркотизация мух
Анализ и подсчет мух, а также отбор девственных самок и подбор родительских пар для скрещивания проводят на матово-белом стекле под лупой после того, как их усыпят серным эфиром. Для этой цели мух помещают в эфиризатор (морилку) или, если специального эфиризатора нет, в обычную пробирку или стаканчик, в которых их размножают. К этому стаканчику подбирают плотную корковую пробку, в нижней части которой делают углубление. В это углубление вставляют плотный ватный тампончик, смачиваемый из капельницы по мере надобности 1-2 каплями серного эфира (избыток эфира можно отжать, так как при попадании в морилку капли эфира с ваты, мухи моментально погибают). Стаканчик с мухами осторожно постукивают о ладонь (мухи при этом собираются в нижней его части), затем осторожно снимают ватную пробку, накрывают стаканчик эфиризатором и опрокидывают так, чтобы стаканчик с мухами был наверху. Легким постукиванием о ладонь всех мух переводят в эфиризатор и закрывают его пробкой с ватным тампоном, смоченным одной каплей эфира. Эфиризатор можно так же ориентировать к свету, так как мухи положительно фототропичны. Как только все мухи заснут, их осторожно вытряхивают из зфиризатора на молочно-белое стекло и, пользуясь лупой и мягкой кисточкой, быстро подсчитывают, так как в наркотизированном состоянии они могут находиться только около 5 мин. Если наркотизацию следует продлить, мух накрывают большим часовым стеклом, под которое кладут ватный тампон, смоченный одной каплей эфира. Если эти мухи нужны для последующего размножения, их помещают в чистые пробирки с питательной средой. В одну пробирку для размножения следует помещать 2-3 самки и 3-5 самцов. Для того чтобы сонные мухи не упали на дно пробирки и не увязли в среде, их помещают на чистую стенку стаканчика со средой и держат стаканчик в горизонтальном положении до тех пор, пока мухи не проснутся. По окончании работы с мухами их усыпляют и выбрасывают. От большой дозы эфира мухи погибают через 3-5 мин. Об их гибели можно заключить по растопыренным крыльям (вверх и в сторону) и безжизненно вытянутым лапкам. Всю работу с дрозофилой и результаты наблюдений фиксируют в соответствующем журнале (табл. 1). Форма журнала может быть различной, но в нем должны быть точно зафиксированы дата постановки опыта или размножения линии, основные сведения о родительских парах, взятых для гибридизации, результаты анализа и т. д.
Таблица 1 Примерная форма журнала работы с дрозофилой
Подготовка мух и постановка опытов
Жизнеспособная сперма может сохраняться в половых путях самки в течение нескольких суток после спаривания. Поэтому каждая оплодотворенная самка в любой момент может содержать в семяприемнике некоторое количество спермы от предыдущей копуляции. Отсюда возникает необходимость брать для скрещивания заведомо девственных самок не старше 10-12 часов после вылупления. Для этой цели из тех культур, из которых надлежит взять девственных самок, за несколько часов до начала массового вылета мух следует удалить родительских или вообще недевственных мух. После этого культуру просматривают через 8–10 часовые интервалы. Вылупляющихся девственных самок изолируют от самцов и используют для скрещиваний. Получение девственных самок в пределах указанных сроков в особенности рекомендуется начинающим, так как большая часть неудач в их опытах связана с несоблюдением именно этого условия.
Неудачи при постановке опытов и их возможные причины
Неудачи генетического характера, т.е. полное несоответствие результатов опыта ожидаемым. Наиболее частые причины их следующие: - для скрещивания взяты или недевственные самки, или по ошибке вообще не из той культуры, откуда их надлежало взять; - неправильно сделаны надписи или перепутаны этикетки при наклейке их на стаканчики. Неудачи, относящиеся к условиям содержания мух, вследствие чего те или иные культуры развились плохо или не развились вовсе. Возможные причины: - среда не была засеяна дрожжами (в культуре обильно развивалась плесень); - среда изготовлена слишком твердой (агар-агар взят в избытке): молодые личинки не могли проникнуть в глубь среды и погибли; - среда изготовлена слишком жидкой (взято недостаточно агар-агара); в культуре избыток влаги, и отложенные яйца погибли (утонули!); - в культуре избыток дрожжей (толстый беловатый пласт дрожжей на поверхности питательной среды). Возможные причины – стерильность самок или культура поставлена на несвежую среду; - мухи лежат мертвыми в стаканчике. Очевидная причина – мухи не проснулись от слишком большой дозы наркоза. Во всех таких случаях мух следует пересадить на свежую среду или скрещивание поставить заново. Хромосомы дрозофилы
Материал и оборудование. Постоянные препараты кариотипов самцов и самок дрозофилы; 4-5 дневные личинки дрозофилы перед окукливанием; 0,73 %-ный NaCI; ацетоорсеин; предметные и покровные стекла; часовые стекла; препаровальные иглы, пинцет, фильтровальная бумага; 45 %-ная уксусная кислота, сахарный сироп; бинокулярная лупа или микроскоп МБС-10; микроскоп МБР-3 или МБР-1.
Задание
1. Познакомьтесь с кариотипом самца и самки дрозофилы. 2. Приготовьте цитологический препарат политенных хромосом из слюнных желёз. 3. Внимательно рассмотрете и зарисуйте политенные хромосомы дрозофилы.
Пояснения к заданию
В соматических клетках дрозофилы содержится 4 пары хромосом (рис. 2). Первая пара - половые хромосомы. У самки они представлены одинаковыми палочковидными хромосомами (XX). Половые хромосомы самцов имеют различное строение.
Одна половая хромосома гомологична Х-хромосоме, другая — заметно отличается от нее (Y-хромосома). Остальные 3 пары хромосом называются аутосомами. Удобный объект для изучения функциональной морфологии хромосом – политенные хромосомы слюнных желёз. Политенная хромосома – гигантская «канатоподобная» хромосома, состоящая из параллельно расположенных идентичных хроматид. Политения, как частный случай эндомитоза – это репликация каждой хромосомы в интерфазе, без увеличения их числа, за счет того, что реплицированные хроматиды остаются лежать, плотно прилегая, друг к другу.
Выполнение задания 1. Извлеките из стаканчика личинки, ползающие перед окукливанием по его стенкам. 2. Поместите личинку на предметное стекло в каплю физиологического раствора или раствора 0,73 %-ной NaCl. 3. Извлеките из личинки слюнные железы. Для этой цели стекло с личинками установите на столик бинокулярной лупы или микроскопа МБС-10. В обе руки возьмите по препаровальной игле. Иглой, находящейся в левой руке, сильно прижмите к стеклу ротовую часть личинки (она имеет черное хитиновое образование). Второй иглой, находящейся в правой руке, надавите на середину тела и отделите голову. Как только она отделится, можно увидеть 2 слюнные железы (отделяющиеся вместе с головой), состоящие из прозрачных клеток, внутри которых находятся политенные хромосомы. 4. Слюнные железы отделите от лишних тканей, уберите фильтровальной бумагой раствор NaCI и нанести 1-2 капли ацетоорсеина на 10-15 мин. 5. Избыток краски удалите фильтровальной бумагой, нанесите каплю сахарного сиропа, накройте покровным стеклом и осторожно раздавите, для чего поверх покровного стекла положите фильтровальную бумагу и слегка надавите пальцем. Затем очень осторожными круговыми движениями тупого конца препаровальной иглы раздавите железы. Следите за тем, чтобы покровное стекло не сдвигалось, иначе раздавленные клетки могут сместиться. 6. Препарат рассмотрите под микроскопом при малом увеличении 10 ´ 9,7 ´ 8 и зарисуйте политенные хромосомы. Обратите внимание на хромоцентр и расположение хромосом. В центре клетки должен лежать ярко окрашенный узел – хромоцентр. В нем соединяются хромомеры всех хромосом. Их всего шесть, хотя число хромосом в соматических клетках дрозофилы – восемь. Такая картина объясняется тем, что пары гомологичных хромосом в слюнных железах дрозофилы конъюгируют (соматическая конъюгация). Следовательно, вместо восьми можно ожидать только четыре гигантские хромосомы, но так как вторая и третья хромосомы у дрозофилы очень длинные – метацентрические, то от хромоцентра, в котором слиты все центромеры, отходят по два плеча второй и третьей хромосом. Четвертая хромосома очень маленькая, она образует малую, едва выступающую из хромоцентра ленту; первая хромосома – акроцентрическая – также образует одну ленту. Итак, получается всего шесть лент: пять длинных и одна короткая. Хорошо приготовленный препарат окантуйте маникюрным лаком и соответствующим образом оформите. 7. При увеличении 15 ´ 40 зарисуйте участок отдельной хромосомы, тщательно соблюдая последовательность расположения и особенности строения отдельных дисков. Изучение мутантов Drosophila melanogaster
Таблица 2. Таблица 4 Результаты гибридологического анализа при моногибридном и возвратном скрещивании
7. Одновременно можно провести опыт по возвратному скрещиванию. Для этого в F1 отберите девственных самок и поместите их в пробирки вместе с самцами одной из родительских форм (доминантной или рецессивной). Анализ мух от возвратного скрещивания F1 с доминантной родительской формой показывает, что все они имеют лопастные глаза, как и мутанты Lobe. В скрещивании F1 срецессивной родительской формой (анализирующее скрещивание) 1/2часть мух имеет лопастные глаза, a 1/2 – нормальные. Такой результат скрещивания свидетельствует о том, что мухи F1 гетерозиготны. Таким же образом могут быть проведены скрещивания и проанализированы гибриды Normal с любым мутантом, у которого соответствующий ген локализован в I, II, IIIили IV хромосомах. Дигибридное скрещивание
Материалы. Стаканчики со свежеприготовленной средой; мутанты ebony и vestigial
Задание
1.Подберите мутантов, для скрещивания. 2. Отберите девственных самок. 3. Произведите скрещивание. 4. Проанализируйте гибриды F1 . 5. Поставьте на скрещивание гибриды F1 для получения F2. 6. Проанализируйте F2.
Пояснения к заданию
Непременное условие свободной перекомбинации генов в F2 при дигибридном скрещивании — локализация их в разных хромосомах. Для этого скрещивания, например, удобно взять рецессивного мутанта с зачаточными крыльями vestigial (ген vg локализован во II хромосоме). Окраска тела у этого мутанта серая (Normal). Вторым компонентом скрещивания можно взять мутанта с темной окраской тела и нормальными крыльями – ebony. Ген е,определяющий темную окраску тела, локализован в III хромосоме. Кроме того, можно для дигибридных скрещиваний рекомендовать и другие комбинации:
♀ Normal ♀ cinnabar ♀ black
Рассмотрим дигибридное скрещивание, воспользовавшись для этой цели рецессивными мутантами vestigial – зачаточные крылья и ebony – темная окраска тела (табл. 5). Наследственный фактор первого из них (vg) локализован во II хромосоме, второго (е) - III хромосоме. Выше уже сказано, что направление скрещивания не влияет на результаты расщепления, если участвующие в скрещивание гены не сцеплены с половой хромосомой. Поэтому безразлично, взять ли для данного скрещивания самку с зачаточными крыльями или с черным телом.
Схема дигибридного скрещивания (ebony
II III II III
Гаметы РР: ♀ +е F1 : ♀♀ и ♂♂ Таблица 5 Гаметы F1 :
F2 : 9 Normal: 3 vestigial: 3 ebony: 1 vestigial.
В дигибридном скрещивании приходится учитывать уже не одну, а две хромосомы. В соответствии с этим генотипическое строение взятых для скрещивания родительских мух должно быть представлено следующим формулами:
Хромосомы: II III II III
Формулы: ♀
Поясним эти формулы. Каждая муха представлена двумя парами диплоидных хромосом (двумя черточками) с содержащимися в них рецессивными генами или их нормальными аллеломорфами. В формуле самки и самца на первом месте стоит II хромосома, на втором - III хромосома. Эти формулы читаются так: у самки ebony (черное тело) ген этого признака находится в III хромосоме в гомозиготном состоянии. Самец же не обладает этим признаком (геном); поэтому гомологичный локус III хромосомы самца представлен нормальным аллеломорфом гена ebony. В противоположность самке самец обладает зачаточными крыльями, ген которых находится во II хромосоме. У самки же с черным телом этот признак (ген) отсутствует; поэтому гомологичный локус ее II хромосомы обозначен знаком + (т.е. нормальным аллеломорфом гена vestigial). Далее обе исходные мухи гомозиготны. Следовательно, оба рецессивных гена и их нормальные аллеломорфы представлены двумя дозами каждый. У всякой гомозиготы по любому числу генов образуется один сорт гамет. Следовательно, взятые для опыта самки ebony дадут один сорт яиц с геном е в III хромосоме и с нормальным аллеломорфом гена vg во II хромосоме. У самцов vestigial образуется также один сорт спермиев с геном vg во II хромосоме и с нормальным аллеломорфом гена ebony в III хромосоме. Следовательно, гаметы родителей будут иметь следующее строение:
♀ +е
От слияния гамет в процессе оплодотворения возникнут гибриды следующего строения (самки и самцы): ♀♀ и ♂♂
Оба рецессивных гена перешли у гибридов в гетерозиготное состояние и не проявляются во внешности. Поэтому все гибриды F1 будут нормального, дикого типа, т.е. серые с длинными крыльями (рис.15). Как известно, число сортов гамет у гибрида выражается формулой 2n , в которой n равно числу пар участвующих в скрещивании генов. В случае дигибридов это число равно 2. Следовательно, у гибридных самок и самцов первого поколения образуется по четыре сорта гамет следующего строения: ♀♀ и ♂♂: ++, +е, vg+, vgе.
Решая далее решетку Пеннета, получаем требуемые теорией генотипы второго поколения анализируемого скрещивания. Суммируя результаты расщепления по фенотипу, получаем окончательную формулу расщепления (таб. 5): 9 Normal: 3 ebony: 3 vestigial: 1 ebony – vestigial.
Выполнение задания
1. Рассмотрите схему дигибридного скрещивания (табл. 5) и определите теоретически ожидаемое расщепление. 2. Отберите 2-3 девственные самки ebony и поместите в стаканчик со свежей средой с 3-5 самцами vestigial. 3. Через 10-12 сут. после постановки скрещивания, когда в стаканчике начинается массовый вылет мух F1, их следует усыпить и проанализировать. Все они при прямом, так и при обратном скрещивании будут, иметь нормальную серую окраску тела и нормально развитые крылья. Результаты подсчета следует заносить в табл. 6. 4. В каждой комбинации F1 следует отобрать по 2-3 женские особи и по 5-6 мужских и поместить их в пробирки с питательной средой для получения F2 , Желательно для получения F2 в каждой комбинации поставить по 3-5 пробирок на каждого студента. 5. Через 10-12 дней в стаканчиках начинается массовый вылет мух F2 . Их следуетв эфиризаторе и анализировать на матово-белом стекле. При внимательном просмотре отделить и подсчитать мух с нормальными крыльями и серым телом, затем – мух с нормальными крыльями и черным телом, с недоразвитыми крыльями и серым телом и с недоразвитыми крыльями и черным телом. Результаты занести в таблицу (табл. 6). Таблица 6 Сцепленное наследование
Материалы. Стаканчики со свежеприготовленной средой; мухи Normal и black-vestigial
Задание
1. Проведите скрещивание Normal 2. Гибриды первого поколения проанализируйте и скрестите с рецессивным родителем black-vestigial. 3. Составьте схему скрещивания и определите теоретически ожидаемое расщепление. 4. Проанализируйте мух FВ и определите соответствие теоретически ожидаемого расщепления фактически полученному.
Пояснения к заданию Т. Морган сформулировал закон сцепленного наследования, согласно которому гены, локализованные в одной хромосоме, наследуются совместно, так как в мейозе они обязательно попадают в однугамету. Число групп сцепления соответствует гаплоидному числу хромосом данного вида. У дрозофилы изучено более 500 генов. Все они локализованы в 4 парах хромосом. Сцепленное наследование генов, находящихся в одной хромосоме, нарушается вследствие конъюгации гомологичных хромосом и обмена участками между ними (кроссинговера). В результате кроссинговера происходит перегруппировка исходных комбинаций признаков. Так, у мух гены, определяющие черную окраску тела (black) и недоразвитые крылья (vestigial), находятся во II хромосоме и наследуются совместно. Но среди гибридных особей могут появиться мухи с черным телом и нормальными крыльями и мухи с серым телом и недоразвитыми крыльями (рис. 17), что свидетельствует о наличии перекрестка хромосом. Гаметы, зиготы и взрослые особи, возникшие в результате перекреста хромосом кроссинговера (crossing-over), называются кроссоверными, или кроссоверами. Число кроссоверных особей свидетельствует о величине расстояния между данными генами в хромосоме: чем больше кроссоверных особей, тем дальше гены расположены в хромосоме один от другого. Количество наблюдаемых в опыте особей (n1), выраженное в % от общего числа мух F2 (n), является показателем частоты или процентом кроссинговера:
n1
n
Согласно теории линейного расположения генов, в хромосомах частота или процент перекреста между генами это функция их расстояния в хромосоме. Например, на основании показателя частоты кроссинговера между генами равного 1,5 % можно заключить, что эти гены расположены в хромосоме на расстоянии 1,5 единицы (морганиды). Наличие перекрестка между генами принято обозначать вертикальной линией. Например, кроссинговер между генами b и vg обозначают как b/vg. Для проведения занятий по установлению процента перекреста и расстояния между генами в хромосоме удобнее всего взять комбинацию Normal Кроме того, для изучения кроссинговера в половой хромосоме можно взять девственную самку с желтой окраской тела (yellow) с вырезанным краем крыла (cut) и глазами киноварного цвета (vermilion) и скрещивать ее с нормальным самцом (Normal). Для изучения кроссинговера во II хромосоме можно взять комбинацию ♀ black-cinnabar-vestigial
Выполнение задания
Методика та же, что и при дигибридном скрещивании, только гибридные особи F1 следует обязательно скрещивать с соответствующим рецессивньм мутантом, т. е. провести анализирующие скрещивания. Схема теоретически ожидаемого расщепления при предполагаемом полном сцеплении в комбинации ♀ Normal
Рис. 17. Неполное сцепление признаков как результат кроссинговера Таблица 10 Решение генетических задач При решении задач используются сведения о доминантных и рецессивных признаках (табл.12). Таблица 12
Задачи
Тема 1. Моногибридное скрещивание
1. Ген черной масти крупного рогатого скота доминирует над геном красной масти. Какое потомство (F1) получится от скрещивания чистопородного черного быка с красными коровами? Каким будет потомство F2 от скрещивания между собой таких гибридов? Какие телята родятся от красного быка и гибридных коров?
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-17; просмотров: 552; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.141.192.219 (0.132 с.) |
 Составитель: В.В. Петрова – канд. биол. наук, доцент
Составитель: В.В. Петрова – канд. биол. наук, доцент

 Если хромосома, состоящая из двух нитей (хроматид), будет девять раз последовательно удваиваться, то число нитей (хромонем) в политенной хромосоме составит 1024. Так и возникает гигантская хромосома. За счет частичной деспирализации хромонем длина гигантской хромосомы увеличивается в 100 – 200 раз по сравнению с метафазной. Политенные хромосомы обнаружены у небольшого числа организмов. Они присутствуют в макроядре водорослей р. Ciliatа, в синергидах и антиподах семяпочек некоторых покрытосеменных растений, в слюнных железах, клетках кишечника, мальпигиевых сосудов у двукрылых насекомых (личинки мотыля из семейства Chironomidae, личинки дрозофилы из семейства Drosophilidae). При рассмотрении гигантских хромосом, прежде всего, видна их поперечная исчерченность (рис. 3). Исчерченность создается чередованием более свежих и более темных полос – дисков, которые представляют собой сильно спирализованные участки хромонем – хромомеры, плотно прилегающие друг другу (интенсивно прокрашиваются красителями, специфичными по отношению к ДНК). Размер и морфология дисков сильно варьируют, но для каждой хромосомы они постоянны и могут служить маркерами для ее идентификации.
Если хромосома, состоящая из двух нитей (хроматид), будет девять раз последовательно удваиваться, то число нитей (хромонем) в политенной хромосоме составит 1024. Так и возникает гигантская хромосома. За счет частичной деспирализации хромонем длина гигантской хромосомы увеличивается в 100 – 200 раз по сравнению с метафазной. Политенные хромосомы обнаружены у небольшого числа организмов. Они присутствуют в макроядре водорослей р. Ciliatа, в синергидах и антиподах семяпочек некоторых покрытосеменных растений, в слюнных железах, клетках кишечника, мальпигиевых сосудов у двукрылых насекомых (личинки мотыля из семейства Chironomidae, личинки дрозофилы из семейства Drosophilidae). При рассмотрении гигантских хромосом, прежде всего, видна их поперечная исчерченность (рис. 3). Исчерченность создается чередованием более свежих и более темных полос – дисков, которые представляют собой сильно спирализованные участки хромонем – хромомеры, плотно прилегающие друг другу (интенсивно прокрашиваются красителями, специфичными по отношению к ДНК). Размер и морфология дисков сильно варьируют, но для каждой хромосомы они постоянны и могут служить маркерами для ее идентификации. Lobe
Lobe
 РР: ♀
РР: ♀