
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дослід 2. Приготування розчину з вказаною масовою часткою розчиненої речовини в розчинi.
а) З твердої речовини i води: Для приготування певної маси розчину з заданою масовою часткою розчиненої речовини необхiдно розрахувати масу води та масу речовини, яку розчиняють, оскільки m (розчину речовини) = m (розчиненої речовини) + m (води). При розрахунках використовують формулу w(речовини в %) = звідки m (розч.реч.) = m (розчину) ·w(речовини в %)/100%, а m (води) = m (розчину)– m (розч.реч.) і V (води) = m (води). 1г/мл У випадку приготування розчину солі з її кристалогiдрату розрахунок ускладнюється: 1) спочатку розраховують необхідну масу безводної солi – m (розч.реч.); 2) встановлюють, в якій масі кристалогідрату знаходиться ця маса безводної солі (тобто перераховують масу солі на масу кристалогiдрату) – m (кристалогідр.солі); розрахунки проводять в такому порядку: – підраховують молярну масу безводної солi – М (безводної солi); – підраховують молярну масу кристалогiдрату цiєї солi – М (кристалогiдр. солі); – складають вiдношення: М (безводної солi) — М (кристалогiдр. солі) m (розч.реч.) — m (кристалогідр.солі) 3) встановлюють m (води) = m (розчину речовини) – m (кристалогідр.солі), звідки V (води) = m (води). 1г/мл. Порядок виконання дослiду: –Одержати вiд викладача завдання. –Розрахувати масу речовини i об’єм води, необхiднi для приготування розчину з вказаною масовою часткою речовини. –Вiдважити цю масу речовини в попередньо зваженому стаканчику на вагах з точнiстю до 0,1 г. –Вiдмiряти мiрним цилiндром необхiдний об’єм води. Вилити цю воду в стакан i розчинити в нiй зважену сiль. –Довести температуру розчину до 20оС. Вилити розчин в сухий (або сполоснутий цим розчином) високий вузький цилiндр i з допомогою ареометру визначити його густину. Ареометр промити водою, витерти насухо i здати лаборанту. Розчин вилити в склянку. –По знайденiй густинi, користуючись таблицею 1, визначити w(речовини (в %) в розчинi) (при необхiдностi данi iнтерполюють). –Порiвняти одержану величину з заданою. –Розрахувати молярну i нормальну концентрацiї виготовленого розчину. Розрахунок проводити в такому порядку: 1) розрахувати масу 1000 мл виготовленого розчину (m 1): m 1 = 1000× d; 2) розрахувати масу розчиненої речовини в 1000 мл розчину (m 2): m 2 = m 1×w; 3) підрахувати молярну масу розчиненої речовини та визначити кiлькiсть молей, що вiдповiдає m 2, тобто CM розчину: СМ = m 2/ М.
Таблиця 1. Масова частка w (%) i густина ρ г/см3 розчинiв солей (при 20оС)
б) З концентрованого розчину i води: · Одержати вiд викладача завдання, яке полягає у приготуванні розчину сульфатної кислоти вказаної масової частки (у %) iз наявного в лабораторiї розчину. Нехай треба приготувати m г розчину H2SO4 з вказаною w (%). · Вимiряти ареометром густину розчину H2SO4, що є в лабораторiї: ρ (вихiдн.розч.) · Знайти в таблицi 2 значення w (%) розчину H2SO4, що вiдповiдає · Розрахувати, яку масу цього розчину кислоти необхiдно взяти для приготування вказаного розчину, а потiм перерахувати одержану величину наважки на об’єм. Таблиця 2. Масова частка w (%) i ρ (г/мл) розчинiв деяких кислот i лугiв при 15оС
Проведення розрахункiв: Розрахувати, яка m (H2SO4) мiститиметься в m (розчину H2SO4), який треба приготувати: m (H2SO4) = m (розчину H2SO4)×w. Вирахувати, в якiй масi вихiдного розчину H2SO4 знаходиться розрахована m (H2SO4): m (вихідного розчину H2SO4) = m (H2SO4) / w(вихідного розчину H2SO4) Розрахувати об’єм вихiдного розчину кислоти, який займає розрахована m (вихідного розчину H2SO4) (тобто об’єм вихiдного розчину кислоти, необхiдний для приготування розчину): V (вихідного розчину H2SO4) = m (вихідного розчину H2SO4) / d (вихiдного розчину H2SO4) –Розрахувати об’єм води необхiдний для приготування розчину: – m (води) = m (розчину H2SO4)– m (вихідного розчину H2SO4); V (води) = m (води) / 1г/мл –Мiрним цилiндром вiдмiряти необхiдний об’єм води; вилити воду в стакан. –Мiрним цилiндром вiдмiряти розрахований об’єм вихiдного розчину кислоти; кислоту вливати в стакан з водою (тонким струменем при перемiшуваннi); перемiшати виготовлений розчин.
–Привести температуру виготовленого розчину до 15оС, перелити його в сухий вузький цилiндр i визначити густину ареометром. Злити одержаний розчин в склянку (для передачi лаборанту). –Користуючись таблицею 2, визначити w (%) одержаного розчину i перевiрити точнiсть виконання дослiду. –Обчислити молярну i нормальну концентрацiю одержаного розчину.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 391; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.134.104.173 (0.006 с.) |
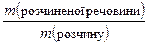 *100%,
*100%,


